一种含Se的新型AIE分子(IV)的合成路线如图:_______ 。
(2)IV中具有孤电子对的原子有_______ 。
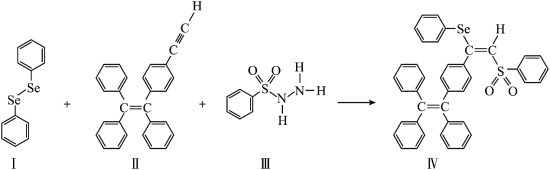
| A.I中仅有σ键 |
| B.I中的Se-Se为非极性共价键 |
| C.II易溶于水 |
| D.II中原子的杂化轨道类型只有sp、sp2、sp3 |
| A.C | B.O | C.S | D.Se |
更新时间:2024-04-10 16:28:23
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素.回答下列问题;
(1)钪(Sc)元素的原子核外电子排布式为_____________ 。钬(Ho)的基态原子电子排布式为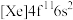 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为_________ 。
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是_____________ 。
几种稀土元素的电离能(单位:kJ/mol)
(3)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+ CH2=CH2;ICH2CH2I中碳原子杂化轨道类型为________ 。
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有___________ 。
(5)1molCH2=CH2中含有的 键数目为:
键数目为:____________ 。
(1)钪(Sc)元素的原子核外电子排布式为
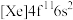 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是
几种稀土元素的电离能(单位:kJ/mol)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有
(5)1molCH2=CH2中含有的
 键数目为:
键数目为:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】碳是形成单质和化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图1、图2所示。
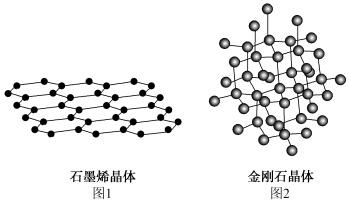
①石墨烯是石墨分离出的单独一层,石墨烯非常稳定,属于厚度只有一个直径大小的“二维材料”,写出一个石墨烯所拥有的特性_____ 。
②求出12g金刚石中含σ键数目为_____ 。
(2)碳的主要氧化物有CO,能与金属Fe形成一种浅黄色液体Fe(CO)5,Fe(CO)5是配合物其熔点为−20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:
①该化合物的晶体中涉及的作用力有_____ 。
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②算出1molFe(CO)5配合物中含有σ键数目_____ 。
(3)CH 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为______ 。
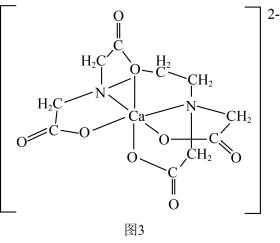
(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图3所示。配位体中碳原子的杂化方式有______ 。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图1、图2所示。

①石墨烯是石墨分离出的单独一层,石墨烯非常稳定,属于厚度只有一个直径大小的“二维材料”,写出一个石墨烯所拥有的特性
②求出12g金刚石中含σ键数目为
(2)碳的主要氧化物有CO,能与金属Fe形成一种浅黄色液体Fe(CO)5,Fe(CO)5是配合物其熔点为−20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:
①该化合物的晶体中涉及的作用力有
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②算出1molFe(CO)5配合物中含有σ键数目
(3)CH
 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图3所示。配位体中碳原子的杂化方式有

您最近一年使用:0次
【推荐3】氯吡苯脲(结构简式如图1所示)是一种膨大剂,具有加速细胞分裂,促进细胞增大、分化,促进果实增大的作用,属于植物生长调节剂中的一类。
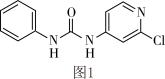
(1)氯元素基态原子核外有_______ 种不同运动状态的电子,核外电子占据的最高能层符号为_______ 。
(2)膨大剂能在动物体内代谢,其产物较为复杂,其中有 、
、 、
、 等。
等。
①请用共价键知识解释 分子比
分子比 分子稳定的原因
分子稳定的原因__________________ 。
② 分子的空间结构是
分子的空间结构是__________________ 。
(3)查文献可知,可用2-氯-4-氨基吡啶与苯酯反应,生成氯吡苯脲,其反应方程式如图2所示:
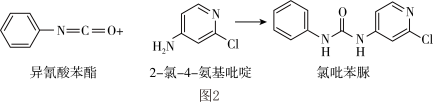
①反应过程中,每生成1 mol氯吡苯脲,断裂σ键和π键个数之比为______ 。
②异氰酸苯酯分子中碳原子的杂化方式为______ ;氮元素的第一电离能大于氧元素的原因是____________ 。
(4)人体必需的抗坏血酸分子结构如图3所示,推测抗坏血酸在水中的溶解性:______ (填“难溶”或“易溶”)于水;抗坏血酸分子中有________ 个手性碳原子。

(1)氯元素基态原子核外有
(2)膨大剂能在动物体内代谢,其产物较为复杂,其中有
 、
、 、
、 等。
等。①请用共价键知识解释
 分子比
分子比 分子稳定的原因
分子稳定的原因②
 分子的空间结构是
分子的空间结构是(3)查文献可知,可用2-氯-4-氨基吡啶与苯酯反应,生成氯吡苯脲,其反应方程式如图2所示:

①反应过程中,每生成1 mol氯吡苯脲,断裂σ键和π键个数之比为
②异氰酸苯酯分子中碳原子的杂化方式为
(4)人体必需的抗坏血酸分子结构如图3所示,推测抗坏血酸在水中的溶解性:

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】某些过渡元素的相关化合物在化工、医药、材料等领域有着极为广泛的应用。回答下列问题:
(1)现有铜锌元素的3种微粒:①锌:[Ar]3d104s1;②铜:[Ar]3d104s1;③铜:[Ar]3d10,失去一个电子需要的最低能量由大到小的顺序是_______(填字母)。
(2)国际权威学术期刊《自然》最近报道,我国科学家选择碲化锆(ZrTes)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应。
①Zr是Ti的同族相邻元素,位于周期表的______ 区。
②Cd2+与NH3可形成配离子[Cd(NH3)4]2+。
i.该离子中不含的化学键类型有______ (填字母)。
A.离子键 B.配位键 C.σ键 D.共价键 E.π键 F.氢键
ii.已知该离子中2个NH3被2个Cl-替代只得到一种结构,则该离子的立体构型为______ 。
(3)二烃基锌(R-Zn-R)分子中烃基R与锌以σ键结合,C2H5-Zn-C2H5分子中原子的杂化方式有______ ,如表是2种二烃基锌的沸点数据,则烃基R1是______ ,推断的依据,是______ 。
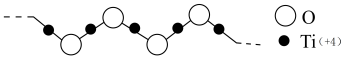
(4)硫酸氧钛(Ti)是一种优良的催化剂,其阳离子为如图所示链状聚合形式的离子,聚合度为n。则该阳离子的化学式为______ 。______ g•cm-3。用Al掺杂TiN后,其晶胞结构如图所示,距离Ti最近的Al有______ 个。(NA为阿伏加德罗常数的值)。
(1)现有铜锌元素的3种微粒:①锌:[Ar]3d104s1;②铜:[Ar]3d104s1;③铜:[Ar]3d10,失去一个电子需要的最低能量由大到小的顺序是_______(填字母)。
| A.①②③ | B.③①② | C.③②① | D.①③② |
(2)国际权威学术期刊《自然》最近报道,我国科学家选择碲化锆(ZrTes)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应。
①Zr是Ti的同族相邻元素,位于周期表的
②Cd2+与NH3可形成配离子[Cd(NH3)4]2+。
i.该离子中不含的化学键类型有
A.离子键 B.配位键 C.σ键 D.共价键 E.π键 F.氢键
ii.已知该离子中2个NH3被2个Cl-替代只得到一种结构,则该离子的立体构型为
(3)二烃基锌(R-Zn-R)分子中烃基R与锌以σ键结合,C2H5-Zn-C2H5分子中原子的杂化方式有
| 物质 | R1-Zn-R1 | C2H5-Zn-C2H5 |
| 沸点(℃) | 46 | 118 |
(4)硫酸氧钛(Ti)是一种优良的催化剂,其阳离子为如图所示链状聚合形式的离子,聚合度为n。则该阳离子的化学式为

您最近一年使用:0次
【推荐2】研究发现,在 低压合成甲醇的反应(
低压合成甲醇的反应(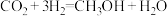 )中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
)中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
(2)基态 原子核外一共有
原子核外一共有___________ 种不同运动状态的电子。
(3) 和
和 分子中
分子中 原子的杂化类型分别为
原子的杂化类型分别为___________ 和___________ 。
(4) 是制备上述反应催化剂的原料,
是制备上述反应催化剂的原料, 的空间构型为
的空间构型为___________ ,与 互为等电子体的分子为
互为等电子体的分子为___________ (任写一种)。
(5)在 、
、 、
、 三种物质中,沸点从高到低的顺序为
三种物质中,沸点从高到低的顺序为___________ ,原因是___________ 。
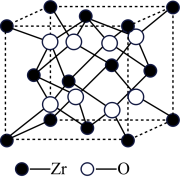
(6)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为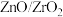 固溶体。四方
固溶体。四方 晶胞如图所示。
晶胞如图所示。 离子在晶胞中的配位数是
离子在晶胞中的配位数是___________ ,晶胞参数为 、
、 、
、 ,该晶体密度为
,该晶体密度为___________  (写出表达式即可)。在
(写出表达式即可)。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为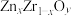 ,则y=
,则y=___________ (用含x的代数式表达)。
 低压合成甲醇的反应(
低压合成甲醇的反应(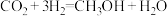 )中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
)中,钴氧化物负载的锰氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)基态
 原子核外一共有
原子核外一共有(3)
 和
和 分子中
分子中 原子的杂化类型分别为
原子的杂化类型分别为(4)
 是制备上述反应催化剂的原料,
是制备上述反应催化剂的原料, 的空间构型为
的空间构型为 互为等电子体的分子为
互为等电子体的分子为(5)在
 、
、 、
、 三种物质中,沸点从高到低的顺序为
三种物质中,沸点从高到低的顺序为(6)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为
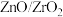 固溶体。四方
固溶体。四方 晶胞如图所示。
晶胞如图所示。 离子在晶胞中的配位数是
离子在晶胞中的配位数是 、
、 、
、 ,该晶体密度为
,该晶体密度为 (写出表达式即可)。在
(写出表达式即可)。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为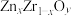 ,则y=
,则y=
您最近一年使用:0次
【推荐3】N,P,As等元素的化合物在生产和研究中有许多重要用途。请回答下列问题:
(1)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子,该分子的空间构型与P4类似,其中氮原子的轨道杂化方式为_______ ,N—N键的键角为____ 。
(2)基态砷原子的价电子排布图为_______ ,砷与同周期相邻元素的第一电离能由大到小的顺序为______ 。
(3)配位原子对孤对电子的吸引力越弱,配体越容易与过渡金属形成配合物。 与
与 的结构相似,和过渡金属更容易形成配合物的是
的结构相似,和过渡金属更容易形成配合物的是__________  填PH4”或“
填PH4”或“ ”
” 。
。
(4)SCl3+和 是等电子体,
是等电子体,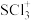 的空间构型是
的空间构型是_________ 。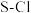 键键长
键键长____ 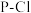 键键长
键键长 填“
填“ ”、“
”、“ ”或“
”或“ ”
” ,原因是
,原因是____________ 。
(1)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子,该分子的空间构型与P4类似,其中氮原子的轨道杂化方式为
(2)基态砷原子的价电子排布图为
(3)配位原子对孤对电子的吸引力越弱,配体越容易与过渡金属形成配合物。
 与
与 的结构相似,和过渡金属更容易形成配合物的是
的结构相似,和过渡金属更容易形成配合物的是 填PH4”或“
填PH4”或“ ”
” 。
。(4)SCl3+和
 是等电子体,
是等电子体,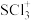 的空间构型是
的空间构型是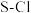 键键长
键键长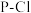 键键长
键键长 填“
填“ ”、“
”、“ ”或“
”或“ ”
” ,原因是
,原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】铁、钴及其化合物在生活、生产中用途广泛。请回答下列问题:
(1)基态Fe2+的核外电子排布式为_______ ;第四周期元素中,基态原子未成对电子数与Co相等的有_______ (填元素符号)。
(2)CoCl3在氨水中能形成多种配合物。取1molCoCl3·4NH3,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为_______ 。
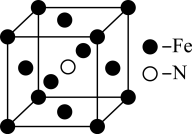
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为_______ 。
(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,设NA为阿伏加德罗常数的值,钴蓝晶体的密度为_______ g/cm3(列计算式)。

(1)基态Fe2+的核外电子排布式为
(2)CoCl3在氨水中能形成多种配合物。取1molCoCl3·4NH3,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为

(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,设NA为阿伏加德罗常数的值,钴蓝晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】铜的单质及其化合物在工农业、国防、科技等领域具有广泛应用。回答下列问题:
(1)基态
 的价层电子排布式为
的价层电子排布式为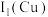
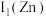
(2)研究发现,阳离子的颜色与未成对电子数有关。例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是(3)合成氨工业中,铜(Ⅰ)氨溶液常用于除去原料气(
 和
和 等)中少量的CO,发生的化学反应为:
等)中少量的CO,发生的化学反应为:
 。
。① 分子中N原子的杂化轨道类型是
分子中N原子的杂化轨道类型是 和
和 中H-N-H键角的大小:
中H-N-H键角的大小:
 (填“>”或“<”)
(填“>”或“<”)
②铜(Ⅰ)氨液吸收CO适宜的生产条件是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③ 配离子中配体是
配离子中配体是
(4)
 与乙二胺
与乙二胺 可形成配离子
可形成配离子 (En是乙二胺的简写),其结构简式如图所示:
(En是乙二胺的简写),其结构简式如图所示: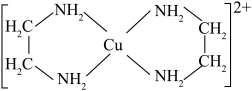
① (乙二胺)和
(乙二胺)和 (三甲胺)均属于胺,二者相对分子质量相近,但乙二胺的沸点比三甲胺的高得多,原因是
(三甲胺)均属于胺,二者相对分子质量相近,但乙二胺的沸点比三甲胺的高得多,原因是
②配合物 中不存在的作用力类型有
中不存在的作用力类型有
A.配位键 B.极性键 C.离子键 D.非极性键
E.范德华力 F.金属键
(5)金属合金
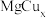 的结构可看作以
的结构可看作以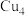 四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置Mg原子(四面体的4个顶点代表Cu原子,圆球代表Mg原子),结构如图所示。
四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置Mg原子(四面体的4个顶点代表Cu原子,圆球代表Mg原子),结构如图所示。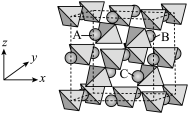
①x=
②若Mg原子A的原子坐标为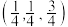 ,则C的原子坐标为
,则C的原子坐标为
③晶胞参数为a nm,则AB原子之间的距离为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】联氨(N2H4)又称肼,在航天、能源等领域具有广泛应用。
Ⅰ.N2H4分子中所有原子均达到稀有气体原子的稳定结构。
(1)写出N2H4的电子式。___________
(2)N2H4晶体受热熔化时,破坏的作用力有___________。
(3)酸碱质子理论提出:凡是能给出质子的分子或离子称为酸,凡是能接受质子的分子或离子称为碱。
①由N2H4+H2O N2H
N2H +OH- 可知N2H4是
+OH- 可知N2H4是___________ 。
A.酸 B.碱
②选择足量的盐酸或NaOH溶液与N2H4充分反应,生成盐的化学式为___________ 。
Ⅱ.肼具有强还原性,可作火箭推进剂燃料,反应的热化学方程式表示为:2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H<0。
(4)①结合化学反应原理分析,该反应可自发进行的原因是___________ 。
②N2H4和N2O4作为火箭推进剂的主要原因是___________ 。
Ⅲ.肼可还原钴离子制备纳米金属钴,纳米金属钴具有特殊的物理、化学和表面性质。
(5)下列状态的钴中,电离最外层一个电子所需能量最小的是_______ 。
A.[Ar]3d74s2 B.[Ar]3d74s14p1 C.[Ar]3d74s1
(6)Co2+被N2H4还原的离子方程式如下,完成方程式并配平_______ 。
 Co2++
Co2++ N2H4+
N2H4+ ___________=
___________= Co↓+
Co↓+ N2↑+
N2↑+ H2O
H2O
当转移7.224×1024个电子数时,生成金属钴___________ 克。
(7)金属钴可以形成多种配合物。一种配合物由Co3+、NH3、Cl-、H2O组成,实验显示Co3+、NH3、Cl-、H2O的物质的量之比为1∶3∶3∶1.向该配合物的水溶液加入AgNO3溶液,只能沉淀出三分之一的Cl-。
①该配合物的化学式是___________ 。
A.[Co(NH3)3ClH2O]Cl2 B.[Co(NH3)3Cl2H2O]Cl C.[Co(NH3)3H2O]Cl3
②该配合物的配体有___________ 。
Ⅰ.N2H4分子中所有原子均达到稀有气体原子的稳定结构。
(1)写出N2H4的电子式。
(2)N2H4晶体受热熔化时,破坏的作用力有___________。
| A.范德华力 | B.氢键 | C.共价键 | D.离子键 |
①由N2H4+H2O
 N2H
N2H +OH- 可知N2H4是
+OH- 可知N2H4是A.酸 B.碱
②选择足量的盐酸或NaOH溶液与N2H4充分反应,生成盐的化学式为
Ⅱ.肼具有强还原性,可作火箭推进剂燃料,反应的热化学方程式表示为:2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H<0。
(4)①结合化学反应原理分析,该反应可自发进行的原因是
②N2H4和N2O4作为火箭推进剂的主要原因是
Ⅲ.肼可还原钴离子制备纳米金属钴,纳米金属钴具有特殊的物理、化学和表面性质。
(5)下列状态的钴中,电离最外层一个电子所需能量最小的是
A.[Ar]3d74s2 B.[Ar]3d74s14p1 C.[Ar]3d74s1
(6)Co2+被N2H4还原的离子方程式如下,完成方程式并配平
 Co2++
Co2++ N2H4+
N2H4+ ___________=
___________= Co↓+
Co↓+ N2↑+
N2↑+ H2O
H2O当转移7.224×1024个电子数时,生成金属钴
(7)金属钴可以形成多种配合物。一种配合物由Co3+、NH3、Cl-、H2O组成,实验显示Co3+、NH3、Cl-、H2O的物质的量之比为1∶3∶3∶1.向该配合物的水溶液加入AgNO3溶液,只能沉淀出三分之一的Cl-。
①该配合物的化学式是
A.[Co(NH3)3ClH2O]Cl2 B.[Co(NH3)3Cl2H2O]Cl C.[Co(NH3)3H2O]Cl3
②该配合物的配体有
您最近一年使用:0次



