1 . 下列有关超分子的说法错误的是
| A.超分子具有“分子识别”和“自组装”的特性 |
| B.分子以共价键聚合形成超分子 |
| C.超分子是由两种或多种分子形成的聚集体 |
| D.分子形成超分子的作用可能是分子间作用力 |
您最近一年使用:0次
名校
解题方法
2 . 同学们使用的涂改液中含有很多有害的挥发性物质,二氯甲烷就是其中的一种,吸入会引起慢性中毒,有关二氯甲烷的说法正确的是
| A.含有非极性共价键 | B.键角均为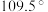 |
| C.有两种同分异构体 | D.分子属于极性分子 |
您最近一年使用:0次
2024-04-10更新
|
45次组卷
|
3卷引用:清单02 分子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
(已下线)清单02 分子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期1月期末化学试题甘肃省定西市临洮中学2023-2024学年高二下学期3月第一次考试化学试题
3 . 下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
| A.氟化氢分子的极性强于氯化氢分子的极性 |
B. 键的键能小于 键的键能小于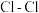 键的键能 键的键能 |
C.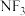 的键角比 的键角比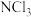 的小 的小 |
D.气态氟化氢中存在 ,而气态氯化氢中是 ,而气态氯化氢中是 分子 分子 |
您最近一年使用:0次
2024-02-19更新
|
183次组卷
|
4卷引用:清单02 分子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
(已下线)清单02 分子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)河北正定中学本部2023-2024学年高二上学期期末考试化学试题河北省石家庄市河北正定中学2023-2024年高二上学期期末考试化学试题黑龙江省哈尔滨市双城区兆麟中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
4 . 价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 和 和 的空间构型均为直线型 的空间构型均为直线型 | B. 和 和 的价层电子对互斥模型均为四面体 的价层电子对互斥模型均为四面体 |
C. 和 和 均为非极性分子 均为非极性分子 | D. 与 与 的键角相等 的键角相等 |
您最近一年使用:0次
名校
解题方法
5 . 现有部分短周期元素的性质或原子结构如下表:
下列说法不正确的是
| 元素编号 | 元素性质或原子结构 |
| T | 基态原子的最外层电子数是次外层电子数的2倍 |
| X | 基态原子的L层有3个未成对电子 |
| Y | 基态原子的L层p电子数比L层s电子数多2个 |
| Z | 元素的最高正价为 价 价 |
A. 分子中 分子中 键与π键之比为 键与π键之比为 |
B. 分子的空间结构为直线形 分子的空间结构为直线形 |
C. 在 在 中的溶解度大于 中的溶解度大于 在 在 中的溶解度 中的溶解度 |
D. 为极性分子, 为极性分子, 为非极性分子 为非极性分子 |
您最近一年使用:0次
2024-02-18更新
|
272次组卷
|
4卷引用:清单02 分子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
(已下线)清单02 分子结构与性质(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)安徽省六安第一中学2023-2024学年高二上学期期末考试化学试题浙江省台州市书生中学2023-2024学年高二下学期起始考化学试卷安徽省淮北市第一中学2023-2024学年高二下学期第一次月考化学试题
6 . 下列各组物质都是由极性键构成的非极性分子的是
A. 和 和 | B. 和HCl 和HCl | C. 和 和 | D. 和 和 |
您最近一年使用:0次
7 . 回答下列问题
(1)蔗糖和氨易溶于水,难溶于四氯化碳;而萘和碘却易溶于四氯化碳,难溶于水。分析原因。___________
(2)比较NH3和CH4在水中的溶解度。怎样用“相似相溶”规律理解它们的溶解度不同?___________
(3)为什么在日常生活中用有机溶剂(如乙酸乙酯等)溶解油漆而不用水?___________
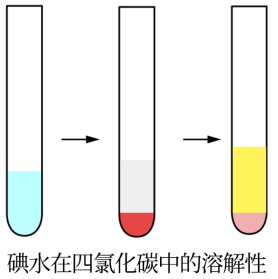
(4)在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,观察碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约1 mL四氯化碳(CCl4),振荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。再向试管里加入1 mL浓碘化钾(KI)水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里可发生如下反应:I2+I-=I 。实验表明碘在纯水还是在四氯化碳中溶解性较好?为什么?
。实验表明碘在纯水还是在四氯化碳中溶解性较好?为什么?___________
(5)利用相似相溶原理解释下表数据。___________
气体的溶解度(气体的压强为1.01×105pa,温度为293K,在100g水中的溶解度)
(6)乙醇、戊醇都是极性分子,为什么乙醇可以与水任意比例互溶,而戊醇的溶解度小?___________
(1)蔗糖和氨易溶于水,难溶于四氯化碳;而萘和碘却易溶于四氯化碳,难溶于水。分析原因。
(2)比较NH3和CH4在水中的溶解度。怎样用“相似相溶”规律理解它们的溶解度不同?
(3)为什么在日常生活中用有机溶剂(如乙酸乙酯等)溶解油漆而不用水?
(4)在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,观察碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约1 mL四氯化碳(CCl4),振荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。再向试管里加入1 mL浓碘化钾(KI)水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里可发生如下反应:I2+I-=I
 。实验表明碘在纯水还是在四氯化碳中溶解性较好?为什么?
。实验表明碘在纯水还是在四氯化碳中溶解性较好?为什么?
(5)利用相似相溶原理解释下表数据。
气体的溶解度(气体的压强为1.01×105pa,温度为293K,在100g水中的溶解度)
| 气体 | 溶解度/g | 气体 | 溶解度/g |
| 乙炔 | 0.117 | 乙烯 | 0.0149 |
| 氨气 | 52.9 | 氢气 | 0.00016 |
| 二氧化碳 | 0.169 | 甲烷 | 0.0023 |
| 一氧化碳 | 0.0028 | 氮气 | 0.0019 |
| 氯气 | 0.729 | 氧气 | 0.0043 |
| 乙烷 | 0.0062 | 二氧化硫 | 11.28 |
您最近一年使用:0次
8 . 键的极性与分子的极性关系
(1)只含有非极性键的双原子分子或多原子分子大多是___________ ,如O2、H2、P4、C60。
(2)含有极性键的双原子分子都是___________ ,如HCl、HF、HBr。
(3)含有极性键的多原子分子,立体构型对称的是___________ ;立体构型不对称的是___________ 。
(1)只含有非极性键的双原子分子或多原子分子大多是
(2)含有极性键的双原子分子都是
(3)含有极性键的多原子分子,立体构型对称的是
您最近一年使用:0次
2022-02-16更新
|
171次组卷
|
2卷引用:课前-2.3.1共价键的极性-人教版2019选择性必修2
9 . 极性分子和非极性分子的定义
(1)极性分子:分子的正电中心和负电中心___________ ,使分子的某一部分呈正电性,另一部分呈负电性,这样的分子是极性分子。如HCl、H2O等。
(2)非极性分子:分子的正电中心和负电中性___________ ,使分子没有带正电和带负电的两部分,这样的分子是非极性分子。如P4、CO2等。
(1)极性分子:分子的正电中心和负电中心
(2)非极性分子:分子的正电中心和负电中性
您最近一年使用:0次
2022-02-16更新
|
140次组卷
|
2卷引用:课前-2.3.1共价键的极性-人教版2019选择性必修2
名校
10 . 化合物NH3与BF3可以通过配位键形成NH3·BF3,下列说法正确的是( )
| A.NH3与BF3都是三角锥形 | B.NH3与BF3都是极性分子 |
| C.NH3·BF3中各原子都达到8电子稳定结构 | D.NH3·BF3中,NH3提供孤电子对,BF3提供空轨道 |
您最近一年使用:0次
2019-04-21更新
|
756次组卷
|
14卷引用:2.3离子键、配位键与金属键(课前)-鲁科版选择性必修2
2.3离子键、配位键与金属键(课前)-鲁科版选择性必修2【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题福建省永春县第一中学2018-2019学年高二下学期期中考试化学试题沪科版高中化学拓展课程第2章《化学键与晶体结构》检测题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题江苏省苏州市相城区陆慕高级中学2019-2020高二下学期4月质量检测化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省福州第一中学2019-2020学年高二下学期期末考试化学试题福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题2021年山东高考化学试题变式题1-10山西省太原市英才学校2022-2023学年高二下学期3月阶段测试化学试题四川省广元市苍溪中学校2022-2023学年高二下学期5月期中考试化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题



