名校
解题方法
1 . 下列说法正确的是
①由非金属元素组成的化合物一定是共价化合物
②离子化合物一定含离子键,可能含极性键或非极性键
③非极性键既可能存在于单质和共价化合物中,也可能存在于离子化合物中
④所有化合物都含有化学键
⑤元素形成化合物时,不一定都达到稀有气体元素原子的电子层结构
⑥任何元素的原子都是由核外电子和核内中子、质子组成的
⑦冰的密度比水的密度小,这与氢键有关
⑧质子数相同的微粒一定属于同种元素
①由非金属元素组成的化合物一定是共价化合物
②离子化合物一定含离子键,可能含极性键或非极性键
③非极性键既可能存在于单质和共价化合物中,也可能存在于离子化合物中
④所有化合物都含有化学键
⑤元素形成化合物时,不一定都达到稀有气体元素原子的电子层结构
⑥任何元素的原子都是由核外电子和核内中子、质子组成的
⑦冰的密度比水的密度小,这与氢键有关
⑧质子数相同的微粒一定属于同种元素
| A.②③④⑤⑦ | B.②③⑤⑦⑧ | C.①③④⑥⑦ | D.①②④⑤⑥ |
您最近一年使用:0次
2021-04-20更新
|
102次组卷
|
2卷引用:黑龙江省绥化一中2020-2021学年高一下学期第一阶段考试化学试题
名校
解题方法
2 . 下列各物质的相关性质与氢键无关的是
| A.氨气的沸点高于砷化氢的沸点 |
| B.乙醇可以与水以任意比例互溶 |
| C.冰的密度小于水的密度 |
| D.氟化氢的稳定性强于氯化氢 |
您最近一年使用:0次
11-12高一下·吉林长春·期末
名校
解题方法
3 . 有X、Y、Z三种短周期元素,原子半径由大到小的顺序为Y>X>Z,原子序数之和为16。三种元素的常见单质在适当条件下可发生如图所示的变化,其中B和C均为10电子分子,以下说法不正确的是
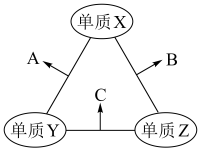

| A.A和C不可能发生氧化还原反应 |
| B.X元素位于ⅥA族 |
| C.A不能溶解于B中 |
| D.B的沸点高于C的沸点 |
您最近一年使用:0次
2020-06-25更新
|
334次组卷
|
32卷引用:黑龙江省肇东市第一中学2016-2017学年高一下学期期中考试化学试题
黑龙江省肇东市第一中学2016-2017学年高一下学期期中考试化学试题(已下线)2011-2012学年吉林省长春市十一高中高一下学期期末考试化学试卷山东省寿光现代中学2016-2017学年高一3月月考化学试题2016-2017学年河北省辛集中学高一下学期第二次月考化学试卷广西南宁市第三中学2016-2017学年高一下学期期中考试(理)化学试题(已下线)狂刷05 元素周期表和元素周期律的应用—《小题狂刷》2017-2018学年高一化学人教必修2河南省豫西名校2017-2018学年高一下学期第一次联考化学试题江西省南康中学2017-2018学年高一下学期第一次月考化学试题(已下线)2019年3月3日 《每日一题》人教(必修2)-每周一测【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第一次月考化学试题【全国百强校】四川省成都外国语学校2018-2019学年高一下学期3月月考化学试题(已下线)【南昌新东方】2019 南昌二中 高一下 第一次月考福建省连城县第一中学2019-2020学年高一下学期期中考试化学试题江西省赣州市南康中学2019-2020学年高一下学期第二次大考化学试题(已下线)4.2.2 元素周期表和元素周期律的应用(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)4.2.2 元素周期表和元素周期律的应用-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)江西省赣州市石城县石城中学2020-2021学年高一下学期3月月考化学试题(已下线)4.2.2 元素周期表和元素周期律的应用-2021-2022学年高一化学10分钟课前预习练(人教版2019必修第一册)(附参考答案)(已下线)2013届山西省忻州市高三第一次联考化学试卷(已下线)2013届上海市普陀区高三下学期二模化学试卷(已下线)2014届福建省四地六校高三上学期第三次月考化学试卷(已下线)2014高考化学名师选择题专练 元素周期表元素周期律练习卷(已下线)2014届高考化学二轮复习必做训练 物质结构、元素周期律练习卷(已下线)2012届北京市人大附中高三5月高考三模理综化学试卷2015届福建省养正中学高三上学期第二次月考化学试卷(已下线)2012届北京市人大附中高三5月高考(三模)化学试卷2016届江西省南昌市第二中学高三上学期第四次考试化学试卷百所名校联考-物质结构 元素周期律2020届高三化学选修三二轮专题复习——微粒半径大小的比较(已下线)上海市普陀区2013届高三4月质量调研(二模)化学试题(已下线)第五章能力提升检测卷-2021年高考化学一轮复习讲练测湖南省常德市临澧县一中2021届高三第四次检测(期中)考试化学试题
名校
解题方法
4 . 下列说法不正确的是
| A.化学反应的实质是旧键的断裂,同时新键的生成 |
| B.CH4、CF4、CCl4、CBr4熔、沸点逐渐升高,原因是分子间作用力逐渐增大 |
| C.NH3和H2O间可以形成氢键,这也是氨极易溶于水的原因之一 |
| D.NH5中含有离子键、极性键、非极性键 |
您最近一年使用:0次
2020-06-04更新
|
197次组卷
|
8卷引用:黑龙江省大庆实验中学2017-2018学年高一4月月考化学试题
名校
解题方法
5 . 类推是一种重要的学习方法,但如果不具体问题具体分析就会得出错误结论。下列类推结论正确的是( )
| A.SiH4的熔沸点比CH4高,则PH3的熔沸点比NH3高 |
| B.H2O比NH3稳定,则H2S也比NH3稳定 |
| C.Al既能与盐酸反应,又能与氢氧化钠反应,则同主族的铟(In)也都能与二者反应 |
| D.同族元素有Ca(OH)2的碱性强于Mg(OH)2,Pb(OH)4的碱性也应强于Sn(OH)4 |
您最近一年使用:0次
11-12高二下·河南鹤壁·阶段练习
名校
解题方法
6 . 关于氢键,下列说法中正确的是( )
| A.每个水分子内含有两个氢键 |
| B.在水蒸气、水和冰中都含有氢键 |
| C.分子间若形成氢键,则物质的熔点和沸点较高 |
| D.HF的稳定性很强,是因为其分子间能形成氢键 |
您最近一年使用:0次
2019-05-06更新
|
212次组卷
|
9卷引用:黑龙江省哈尔滨市第六中学校2019-2020学年高一下学期返校适应训练化学试题
黑龙江省哈尔滨市第六中学校2019-2020学年高一下学期返校适应训练化学试题(已下线)2011-2012学年安徽省铜陵市一中高一下学期期中考试化学试卷甘肃省天水市第三中学2016-2017学年高一下学期第一次月考化学试题内蒙古自治区北京八中乌兰察布分校2018-2019学年高一下学期第一次月考化学试题(已下线)2011-2012学年河南省淇县高级中学高二下学期第一次月考化学试卷吉林省辽源市田家炳高级中学2018-2019学年高二下学期期中考试化学试题第4节 分子间作用力与物质性质——A学习区 夯实基础(鲁科版选修3)(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 课时2 分子间的作用力2.3.2 分子间作用力 分子的手性-随堂练习
7 . 下列说法正确的是
| A.原子最外层电子数为2的元素一定位于周期表第ⅡA族 |
| B.向氢硫酸溶液中滴入氯水有单质硫生成,说明硫元素的非金属性比氯元素弱 |
| C.氯化氢的沸点比氟化氢的沸点高 |
| D.第三周期元素的离子半径从左到右逐渐减小 |
您最近一年使用:0次
8 . 下列排列顺序正确的是
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③酸性:H3PO4>H2SO4>HClO4 ④得电子能力:C<N<O<F ⑤沸点:H2S> H2O>HF
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③酸性:H3PO4>H2SO4>HClO4 ④得电子能力:C<N<O<F ⑤沸点:H2S> H2O>HF
| A.①③④ | B.②④ | C.①④⑤ | D.②⑤ |
您最近一年使用:0次
9-10高二下·吉林·期末
名校
9 . 下列说法正确的是
| A.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| B.ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| C.同周期非金属的氧化物对应水化物的酸性从左到右依次增强 |
| D.第三周期元素的离子半径从左到右逐渐减小 |
您最近一年使用:0次
2016-12-09更新
|
635次组卷
|
22卷引用:2010年黑龙江省哈六中高一下学期期中考试化学试题
(已下线)2010年黑龙江省哈六中高一下学期期中考试化学试题(已下线)09~10年大连23中高一下学期期末考试化学卷(已下线)2011-2012学年山西省忻州一中高一下学期期中考试理科化学试卷(已下线)2011-2012学年湖北武汉部分重点中学高一下学期期末考试化学题(已下线)2012-2013学年云南省昆明三中滇池中学高一下学期期中考试化学文科卷(本部)(已下线)2014年高一化学人教版必修2 期中测试练习卷2014-2015辽宁师大附中高一下学期第一次月考化学试卷2014-2015学年山西省山西大学附中高一4月月考化学试卷2015-2016学年辽宁沈阳市第二中学高一下期末考试化学卷2016-2017学年湖南省长沙一中高一上第二次月考化学卷河南省鹤壁市淇滨高级中学2017-2018学年高一3月月考化学试题人教版2017-2018学年高一化学必修2:第一章 第二节 难度偏大尖子生题吉林省白山市第十九中学2018-2019学年高一下学期期中考试化学试题吉林省蛟河市一中2018-2019学年高一下学期第三次测试化学试题黑龙江省哈尔滨市第六中学校2019-2020学年高二下学期期中考试化学试题(已下线)吉林一中2009--2010学年度下学期期末考试第一次质量检测高二化学试卷(已下线)2010年内蒙古赤峰市田家炳中学高二上学期期中考试化学试卷(已下线)2013-2014学年山东济宁市曲阜师大附中高二上学期期中考试化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1吉林省延边市第二中学2017-2018学年高二下学期第一次月考化学试题河北省博野中学2019-2020学年高二下学期开学考试化学试题福建省龙海市第二中学2019-2020学年高二下学期期末考试化学试题
9-10高一下·黑龙江·期中
10 . 关于卤族元素从F到I的递变规律正确的是
| A.氢化物稳定性逐渐增强 | B.最高价氧化物水化物的酸性逐渐增强 |
| C.氢化物的还原性逐渐增强 | D.氢化物的溶沸点逐渐升高 |
您最近一年使用:0次



