真题
解题方法
1 . ⅣA族元素具有丰富的化学性质,其化合物有着广泛的应用。回答下列问题:
(1)该族元素基态原子核外未成对电子数为_____ ,在与其他元素形成化合物时,呈现的最高化合价为_____ 。
(2) 俗称电石,该化合物中不存在的化学键类型为
俗称电石,该化合物中不存在的化学键类型为_____ (填标号)。
a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)一种光刻胶薄膜成分为聚甲基硅烷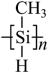 ,其中电负性最大的元素是
,其中电负性最大的元素是_____ ,硅原子的杂化轨道类型为_____ 。
(4)早在青铜器时代,人类就认识了锡。锡的卤化物熔点数据如下表,结合变化规律说明原因:_____ 。
(5)结晶型 可作为放射性探测器元件材料,其立方晶胞如图所示。其中
可作为放射性探测器元件材料,其立方晶胞如图所示。其中 的配位数为
的配位数为_____ 。设 为阿伏加德罗常数的值,则该晶体密度为
为阿伏加德罗常数的值,则该晶体密度为_____  (列出计算式)。
(列出计算式)。
(1)该族元素基态原子核外未成对电子数为
(2)
 俗称电石,该化合物中不存在的化学键类型为
俗称电石,该化合物中不存在的化学键类型为a.离子键 b.极性共价键 c.非极性共价键 d.配位键
(3)一种光刻胶薄膜成分为聚甲基硅烷
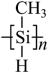 ,其中电负性最大的元素是
,其中电负性最大的元素是(4)早在青铜器时代,人类就认识了锡。锡的卤化物熔点数据如下表,结合变化规律说明原因:
| 物质 | 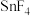 |  |  | 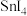 |
熔点/ | 442 | 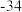 | 29 | 143 |
 可作为放射性探测器元件材料,其立方晶胞如图所示。其中
可作为放射性探测器元件材料,其立方晶胞如图所示。其中 的配位数为
的配位数为 为阿伏加德罗常数的值,则该晶体密度为
为阿伏加德罗常数的值,则该晶体密度为 (列出计算式)。
(列出计算式)。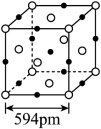
您最近一年使用:0次
2 . 下列各组物质的鉴别方法中,不可行 的是
| A.过氧化钠和硫黄:加水,振荡 | B.水晶和玻璃:X射线衍射实验 |
| C.氯化钠和氯化钾:焰色试验 | D.苯和甲苯:滴加溴水,振荡 |
您最近一年使用:0次
名校
3 . 下列有关物质的组成、结构、性质与转化,说法正确的是
| A.醛、酮分子间可形成氢键,其沸点比相应的烷烃要高 |
| B.苯、甲苯、苯酚都能与溴单质发生取代反应,苯酚更容易进行 |
| C.冠醚是不同大小空穴的超分子,可以识别不同大小的碱金属离子 |
| D.缺角的氯化钠晶体在饱和溶液中慢慢变为完美的立方体块,表现了晶体的各向异性 |
您最近一年使用:0次
解题方法
4 . 构成离子液体的阴、阳离子由于体积较大,其熔点较低,是一种熔点低于或接近室温的盐。使用离子液体催化剂催化合成 -巯基丙酸(
-巯基丙酸(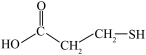 )的流程如图所示:
)的流程如图所示:
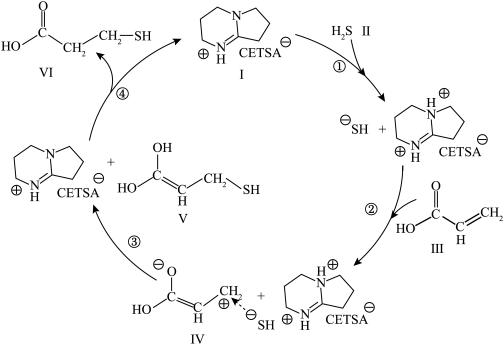
A.总反应是 与 与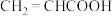 发生取代反应 发生取代反应 |
B.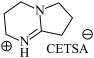 和 和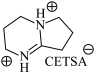 均是该反应的催化剂 均是该反应的催化剂 |
C.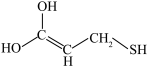 是一种不稳定结构,容易转化为 是一种不稳定结构,容易转化为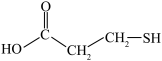 |
| D.该反应流程中的离子液体催化剂属于离子晶体,其中的阳离子含有共价键和配位键 |
您最近一年使用:0次
5 . 硼及其化合物在科研、工业等方面用途广泛。
(1)基态B原子价层电子排布式是______ 。
(2)硼原子与氮原子结合可以形成多种晶体。其中六方氮化硼与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,耐磨性高。它们的晶体结构如图1所示。下列关于这两种晶体的说法正确的是______ (填序号)。
b.六方氮化硼结构与石墨相似却不导电
c.两种晶体中的B和N之间的作用力均为共价键
d.立方氮化硼含有σ键和π键,属于共价晶体,所以硬度大
(3) 是一种重要的储氢材料,其晶胞结构由Ⅰ、Ⅱ两部分组成,如图2所示。
是一种重要的储氢材料,其晶胞结构由Ⅰ、Ⅱ两部分组成,如图2所示。______ 。
②已知阿伏加德罗常数为 ,该晶体的密度为
,该晶体的密度为______  。(
。( )
)
(4)氨硼烷(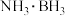 )可由
)可由 制备,方法如下:
制备,方法如下:
已知:ⅰ.元素的电负性:H-2.1、B-2.0;ⅱ.卤化物水解,需先与水分子配位。
①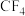 不能水解,但
不能水解,但 能水解。原因是
能水解。原因是______ 。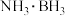 会继续与THF·BH3反应生成副产物
会继续与THF·BH3反应生成副产物 。过程如下:
。过程如下:______ 能量(填“吸收”或“放出”)。
(1)基态B原子价层电子排布式是
(2)硼原子与氮原子结合可以形成多种晶体。其中六方氮化硼与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,耐磨性高。它们的晶体结构如图1所示。下列关于这两种晶体的说法正确的是
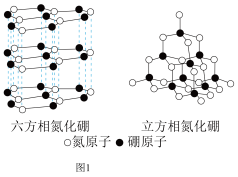
b.六方氮化硼结构与石墨相似却不导电
c.两种晶体中的B和N之间的作用力均为共价键
d.立方氮化硼含有σ键和π键,属于共价晶体,所以硬度大
(3)
 是一种重要的储氢材料,其晶胞结构由Ⅰ、Ⅱ两部分组成,如图2所示。
是一种重要的储氢材料,其晶胞结构由Ⅰ、Ⅱ两部分组成,如图2所示。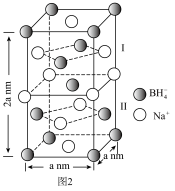
②已知阿伏加德罗常数为
 ,该晶体的密度为
,该晶体的密度为 。(
。( )
)(4)氨硼烷(
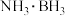 )可由
)可由 制备,方法如下:
制备,方法如下:已知:ⅰ.元素的电负性:H-2.1、B-2.0;ⅱ.卤化物水解,需先与水分子配位。
①
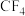 不能水解,但
不能水解,但 能水解。原因是
能水解。原因是②在水中的溶解性:THF(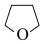 )>环戊烷,原因是
)>环戊烷,原因是
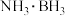 会继续与THF·BH3反应生成副产物
会继续与THF·BH3反应生成副产物 。过程如下:
。过程如下: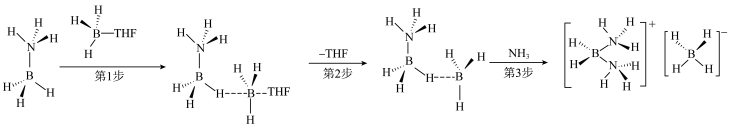
④可用 和DMA(二甲胺
和DMA(二甲胺 )代替THF(
)代替THF(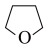 )进行氨硼烷的制备,
)进行氨硼烷的制备, 、DMA和THF分别与B原子的结合能力由大到小的顺序为
、DMA和THF分别与B原子的结合能力由大到小的顺序为
您最近一年使用:0次
6 . 砷及其化合物在农业,制药、木材防腐、半导体产业等方面发挥着重要作用。晶体砷是层状结构,与石墨的结构相似,其结构如图。下列说法错误的是
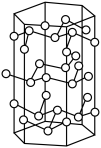
| A.砷是由距离较近的两层组成的双层结构 |
| B.双层结构中的同层内原子间不形成化学键 |
| C.1mol砷形成3mol共价键 |
| D.此砷晶体属于混合型晶体 |
您最近一年使用:0次
名校
7 . 下面内容描述存在因果关系不正确的是
| A.SOCl2遇水反应,需要在制备装置前后加装干燥装置 |
| B.Fe3+易水解,需要将FeCl3固体溶解在浓盐酸中在加水稀释 |
| C.P2O5具有吸水性,可用干燥管盛装P2O5用于干燥氨气 |
| D.雪花六边形的形成,体现了晶体的自范性 |
您最近一年使用:0次
解题方法
8 . 新材料产业是战略性、先导性产业,事关现代化经济体系建设大局。下列说法正确的是
| A.集成电路产业基础原料电子级多晶硅属于分子晶体 |
| B.超级钢是一种新型合金,其熔点和强度均低于纯铁 |
| C.离子液体在室温或稍高于室温下能导电,呈离子化合物的性质 |
| D.高分子分离膜可用于海水淡化,淡化原理利用的是海水和淡水沸点不同 |
您最近一年使用:0次
解题方法
9 . 下列有关物质性质差异的解释不合理的是
| 选项 | 性质差异 | 解释 |
| A | 硬度:金刚石>晶体硅 | 键能: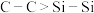 |
| B | 熔点:石墨> | 石墨是共价晶体, 是分子晶体 是分子晶体 |
| C | 沸点: |  分子间存在氢键 分子间存在氢键 |
| D | 酸性: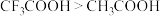 | 电负性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 晶态 的晶胞如图。
的晶胞如图。___________ 。
②晶态 中1个Si原子周围有
中1个Si原子周围有___________ 个紧邻的O原子。
(2)碳与硅属同族元素,其氧化物二氧化碳固态下又称干冰,熔点为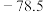 ℃,远低于二氧化硅,其原因为
℃,远低于二氧化硅,其原因为___________ 。
(3)某种硅玻璃可近似看做 晶体。在硅玻璃中常常出现晶体缺陷:在应该有O的位置上少了一些O,旁边的Si原子只能形成
晶体。在硅玻璃中常常出现晶体缺陷:在应该有O的位置上少了一些O,旁边的Si原子只能形成 键保持稳定。当硅玻璃的组成为
键保持稳定。当硅玻璃的组成为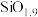 时,其中
时,其中 键与
键与 键的个数比为
键的个数比为___________ 。
(4)无机硅胶(化学式用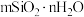 表示)是一种高活性吸附材料,可由硅元素最高价氧化物对应的水化物原硅酸(
表示)是一种高活性吸附材料,可由硅元素最高价氧化物对应的水化物原硅酸( )发生分子间脱水获得。
)发生分子间脱水获得。
①原硅酸钠( )溶液可吸收空气中的
)溶液可吸收空气中的 生成
生成 ,结合元素周期律解释该反应发生的原因:
,结合元素周期律解释该反应发生的原因:___________ 。
②从结构的角度分析 脱水后溶解度降低的原因:
脱水后溶解度降低的原因:___________ 。
③ 脱水过程中能量变化很小,结合化学键变化分析其原因可能是
脱水过程中能量变化很小,结合化学键变化分析其原因可能是___________ 。
 的晶胞如图。
的晶胞如图。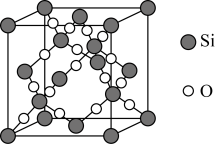
②晶态
 中1个Si原子周围有
中1个Si原子周围有(2)碳与硅属同族元素,其氧化物二氧化碳固态下又称干冰,熔点为
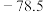 ℃,远低于二氧化硅,其原因为
℃,远低于二氧化硅,其原因为(3)某种硅玻璃可近似看做
 晶体。在硅玻璃中常常出现晶体缺陷:在应该有O的位置上少了一些O,旁边的Si原子只能形成
晶体。在硅玻璃中常常出现晶体缺陷:在应该有O的位置上少了一些O,旁边的Si原子只能形成 键保持稳定。当硅玻璃的组成为
键保持稳定。当硅玻璃的组成为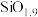 时,其中
时,其中 键与
键与 键的个数比为
键的个数比为(4)无机硅胶(化学式用
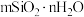 表示)是一种高活性吸附材料,可由硅元素最高价氧化物对应的水化物原硅酸(
表示)是一种高活性吸附材料,可由硅元素最高价氧化物对应的水化物原硅酸( )发生分子间脱水获得。
)发生分子间脱水获得。①原硅酸钠(
 )溶液可吸收空气中的
)溶液可吸收空气中的 生成
生成 ,结合元素周期律解释该反应发生的原因:
,结合元素周期律解释该反应发生的原因:②从结构的角度分析
 脱水后溶解度降低的原因:
脱水后溶解度降低的原因:③
 脱水过程中能量变化很小,结合化学键变化分析其原因可能是
脱水过程中能量变化很小,结合化学键变化分析其原因可能是
您最近一年使用:0次
2024-06-06更新
|
97次组卷
|
2卷引用:北京市第二中学2023-2024学年高三下学期三模化学试题



