名校
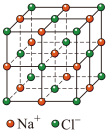
1 . 钙钛矿具有独特的晶体结构,广泛应用于太阳能电池材料、传感器等诸多领域。图1、2均为钙钛矿型化合物,图1中另两种离子为 、
、 ,图2中另两种离子为
,图2中另两种离子为 和
和 ,晶胞参数
,晶胞参数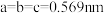 ,
, a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示:
a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示:
 、
、 ,图2中另两种离子为
,图2中另两种离子为 和
和 ,晶胞参数
,晶胞参数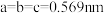 ,
, a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示:
a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示: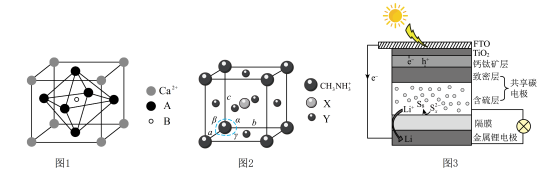
A.钛酸钙的化学式为 | B.图2中Y为 |
C. 中存在配位键 中存在配位键 | D.图2晶体的密度为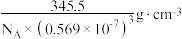 |
您最近一年使用:0次
2 . 二氧化铈(CeO2)作为一种脱硝催化剂,能在Ce4+和Ce3+之间改变氧化状态,将NO氧化为NO2,并引起氧空位的形成,得到新的铈氧化物[Cex(Ⅲ)Cey(Ⅳ)Oz]。当二氧化铈晶胞发生如下图变化时,有关说法错误的是
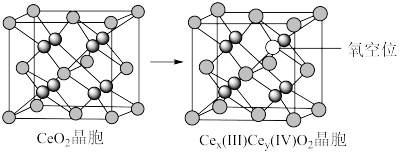
| A.铈位于氧原子形成的八面体空隙中 |
| B.生成新的铈氧化物中x、y、z的最简整数比为2:2:7,当1 mol CeO2发生变化时,可吸收标况下NO的体积为5.6 L |
C.晶胞的俯视图为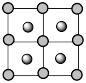 |
D.若晶胞边长为a pm,则CeO2晶体的密度为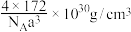 (NA表示阿伏加德罗常数的值) (NA表示阿伏加德罗常数的值) |
您最近一年使用:0次
名校
解题方法
3 . 铁与镁组成的储氢合金的立方晶胞结构如图所示。铁原子位于顶点和面心的位置,镁原子位于将晶胞平分为8个立方单位的体心位置,NA为阿伏加德罗常数的值。下列说法正确的是
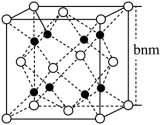
| A.该晶体中存在金属阳离子,所以该合金属于离子晶体 |
B.该晶体密度为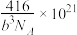 g·cm-3 g·cm-3 |
| C.距离Fe原子最近的Mg原子数为4 |
| D.晶体储氢时,H2在晶胞的体心和棱的中心位置,则储氢后化学式为FeMg2H |
您最近一年使用:0次
名校
解题方法
4 . 科学家研发出一种新型储氢材料,晶胞结构如下图所示,晶胞参数为apm,下列说法正确的是
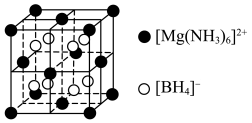
| A.所含非金属元素的电负性N>B>H |
B.该晶体的化学式为 |
C.阴、阳离子的最小距离为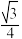 apm apm |
| D.若晶胞以[BH4]-为顶点,所得晶胞结构与NaCl晶胞相同 |
您最近一年使用:0次
解题方法
5 . 钛酸钙是一种典型的钙钛矿型半导体材料,其晶胞结构如图所示。下列关于钛酸钙说法不正确的是

| A.每个晶胞中含有3个O2﹣ |
| B.化学式为CaTiO3 |
| C.含有离子键 |
| D.晶体具有良好的导电性和延展性 |
您最近一年使用:0次
6 . 由 、
、 、
、 等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是
等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是
 、
、 、
、 等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是
等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是
A.钒基笼目金属的化学式为 | B. 分布在由 分布在由 构成的八面体空隙中 构成的八面体空隙中 |
C.可以通过 射线衍射实验测定晶体结构 射线衍射实验测定晶体结构 | D.1号、2号 原子间的距离为 原子间的距离为 |
您最近一年使用:0次
7 . 几种晶体的晶胞(或晶体结构)如图所示,下列说法正确的是
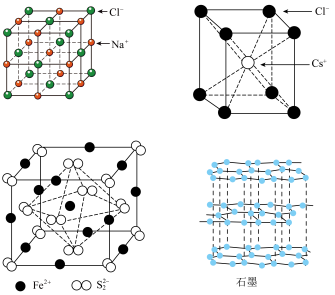
A. 中 中 的配位数大于干冰中 的配位数大于干冰中 分子的配位数 分子的配位数 |
B. 晶胞中,若 晶胞中,若 作顶点,则 作顶点,则 应在面心处 应在面心处 |
C.若 的晶胞边长为apm,其中S原子的半径为 的晶胞边长为apm,其中S原子的半径为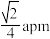 |
| D.石墨晶体层内作用力是共价键,层间作用力是范德华力,所以石墨是一种混合型晶体 |
您最近一年使用:0次
8 .  的晶胞示意图如图甲所示。存在“缺陷”的氧化镍晶体
的晶胞示意图如图甲所示。存在“缺陷”的氧化镍晶体 如图乙所示(一个
如图乙所示(一个 空缺,另有两个
空缺,另有两个 被两个
被两个 所取代,其晶体仍呈电中性)。下列说法正确的是
所取代,其晶体仍呈电中性)。下列说法正确的是
 的晶胞示意图如图甲所示。存在“缺陷”的氧化镍晶体
的晶胞示意图如图甲所示。存在“缺陷”的氧化镍晶体 如图乙所示(一个
如图乙所示(一个 空缺,另有两个
空缺,另有两个 被两个
被两个 所取代,其晶体仍呈电中性)。下列说法正确的是
所取代,其晶体仍呈电中性)。下列说法正确的是
A. 元素位于元素周期表的 元素位于元素周期表的 区 区 |
B. 晶体中每个 晶体中每个 周围与它距离相等且最近的 周围与它距离相等且最近的 有6个 有6个 |
C.某氧化镍 晶体中 晶体中 与 与 的个数比为 的个数比为 ,则 ,则 |
D. 晶体中与一个 晶体中与一个 距离相等且最近的 距离相等且最近的 构成的空间几何形状为正四面体 构成的空间几何形状为正四面体 |
您最近一年使用:0次
9 . 下列关于各晶体模型示意图的分析不正确的是
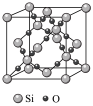
| 名称 |  的晶胞 的晶胞 |  的晶胞 的晶胞 |
| 模型示意图 |
|
|
| 分析 | A.1个 晶胞内含有4个 晶胞内含有4个 和4个 和4个 | B.Si原子的配位数为2 |
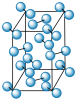
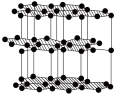
| 名称 | 晶体碘的晶胞 | 石墨晶体的结构 |
| 模型示意图 |
|
|
| 分析 | C. 在晶胞中的排列有2种取向 在晶胞中的排列有2种取向 | D. 石墨中含有共价键的数目为 石墨中含有共价键的数目为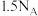 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示(晶胞边长为a pm,晶胞高为c pm, 为阿伏加德罗常数的值)。下列说法正确的是
为阿伏加德罗常数的值)。下列说法正确的是

 为阿伏加德罗常数的值)。下列说法正确的是
为阿伏加德罗常数的值)。下列说法正确的是
| A.一个晶胞中含有3个Mg原子 |
B.硼原子间最近距离为 |
| C.Mg的配位数为6 |
D.晶胞的密度为 |
您最近一年使用:0次