解题方法
1 . 下列说法错误的是
A. 晶体中每种离子的配位数为8 晶体中每种离子的配位数为8 |
| B.某金属晶体具有体心立方结构,那么该金属的配位数为12 |
| C.一个离子晶体的单胞与其他邻近单胞共享一些离子 |
D. 晶体的晶胞边长为 晶体的晶胞边长为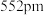 (已知 (已知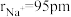 , ,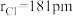 ) ) |
您最近一年使用:0次
2 . 金是一种贵重金属,抗腐蚀,是延展性最好的金属之一。负载型金纳米材料在催化动态催化理论、光学、电子学等方面有重要作用。
Ⅰ.金的结构
(1)金元素位于元素周期表第6周期ⅠB族,金的价电子排布式为_______ 。
(2)金晶体的晶胞为面心立方晶胞,Au在晶胞中的配位数是_______ 。
Ⅱ.金的提取
硫脲(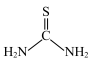 )液相提金原理:
)液相提金原理:
(3)硫脲易溶于水,原因是_______ 。
Ⅲ.金的应用
一种最稳定的负载型纳米金团簇,具有最完美的对称性,其结构如图所示:
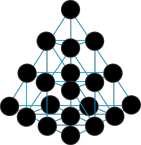
(4)该金团簇的化学式为_______ (填字母)。
a.Au b.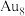 c.
c.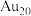
(5)该金团簇中有_______ 种不同化学环境的金原子。
Ⅰ.金的结构
(1)金元素位于元素周期表第6周期ⅠB族,金的价电子排布式为
(2)金晶体的晶胞为面心立方晶胞,Au在晶胞中的配位数是
Ⅱ.金的提取
硫脲(
 )液相提金原理:
)液相提金原理:
(3)硫脲易溶于水,原因是
Ⅲ.金的应用
一种最稳定的负载型纳米金团簇,具有最完美的对称性,其结构如图所示:

(4)该金团簇的化学式为
a.Au b.
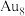 c.
c.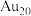
(5)该金团簇中有
您最近一年使用:0次
3 . 立方晶系二元合金
有一立方晶系二元合金,单胞参数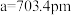 。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体
。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体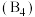 ,已知晶胞中
,已知晶胞中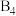 的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
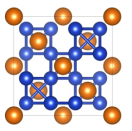
(1)写出二元合金的化学式_______ 。
(2)已知金属A和B的原子量分别为24.31和53.55,计算合金的理论密度_______ 。
(3)晶胞的单位点阵型式_______ 。
(4)实际上,大部分该类结构二元合金的原子半径比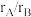 处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和
处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和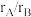 值
值_______ 、_______ 。
有一立方晶系二元合金,单胞参数
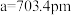 。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体
。单胞中的金属A原子与金刚石中碳原子位置相同,原子处于密堆积状态。在单胞中有若干金属B原子,每4个B原子构成一个正四面体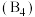 ,已知晶胞中
,已知晶胞中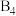 的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
的位置可看成填充于A原子堆积形成的四面体孔隙中,沿轴向的单胞投影示意图如图所示:
(1)写出二元合金的化学式
(2)已知金属A和B的原子量分别为24.31和53.55,计算合金的理论密度
(3)晶胞的单位点阵型式
(4)实际上,大部分该类结构二元合金的原子半径比
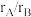 处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和
处于1.1~1.4之间,假设沿单胞面对角线方向上的B原子在整个结构紧密接触,计算金属B的原子半径和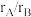 值
值
您最近一年使用:0次
4 . 铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途,如二茂铁可用作火箭燃料添加剂,含铁等磁性材料被广泛应用于电子信息、军事技术等领域。根据题目信息回答下列问题:
(1)基态Fe原子的电子排布式为_______ 。
(2)二茂铁(C5H5)2Fe是一种浅黄色难溶于水的液体,其熔点-20℃,沸点103℃。依据以上信息可推断二茂铁属于_______ (“离子晶体”、“分子晶体”或“原子晶体”)。
(3)独立的NH3分子中,H-N-H键键角为107.3,下图是[Zn(NH3)6]2+离子的部分结构以及其中H-N-H键键角。
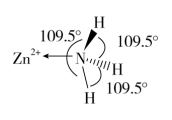
请解释[Zn(NH3)6]2+离子中H-N-H键角变为109.5的原因是_______ 。
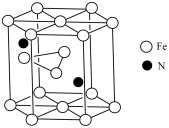
(4)某种磁性氮化铁的结构如下图所示,Fe的堆积方式为_______ ,则该化合物的化学式为_______ ;氮化铁晶胞底边长为a pm,高为b pm,则这种磁性氮化铁的晶体密度为_______ g·cm-3 (用含a、b和NA的计算式表示)。
(1)基态Fe原子的电子排布式为
(2)二茂铁(C5H5)2Fe是一种浅黄色难溶于水的液体,其熔点-20℃,沸点103℃。依据以上信息可推断二茂铁属于
(3)独立的NH3分子中,H-N-H键键角为107.3,下图是[Zn(NH3)6]2+离子的部分结构以及其中H-N-H键键角。

请解释[Zn(NH3)6]2+离子中H-N-H键角变为109.5的原因是
(4)某种磁性氮化铁的结构如下图所示,Fe的堆积方式为

您最近一年使用:0次
解题方法
5 . (1)钛铁合金具有吸氢特性,工业在制造以氢为能源的热泵和蓄电池等方面有广阔的应用前景,金属Ti(六方最密堆积)的原子空间利用率约为_______ ,基态Ti原子核外有_______ 个运动状态不同的电子,在基态Ti2+中,电子占据的能量最高的轨道为_______ 。
(2)已知Si-Si键能为176 kJ/mol,Si-O键能为460 kJ/mol,O=O键能为497.3 kJ/mol,则可计算出1 mol硅与足量氧气反应时将放出_______ kJ的热量。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般为d0或d10排布时,无颜色;为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色,据此判断 [Mn(H2O)6]2+_______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。COCl2分子的空间构型为_______ ;Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______ 。
(5)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(如图),则该晶体中镁、碳、镍三种元素的原子个数比是_______ ,晶体中每个镁原子周围距离最近的镍原子有_______ 个。
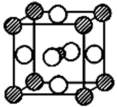
(图中:碳原子用小 球在晶体的体心,镍原子用大
球在晶体的体心,镍原子用大 球,镁原子用大
球,镁原子用大 球)
球)
(2)已知Si-Si键能为176 kJ/mol,Si-O键能为460 kJ/mol,O=O键能为497.3 kJ/mol,则可计算出1 mol硅与足量氧气反应时将放出
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般为d0或d10排布时,无颜色;为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色,据此判断 [Mn(H2O)6]2+
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。COCl2分子的空间构型为
(5)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(如图),则该晶体中镁、碳、镍三种元素的原子个数比是

(图中:碳原子用小
 球在晶体的体心,镍原子用大
球在晶体的体心,镍原子用大 球,镁原子用大
球,镁原子用大 球)
球)
您最近一年使用:0次



