解题方法
1 . 图1为某 晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。
晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。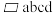 为所取晶胞的下底面,为锐角等于
为所取晶胞的下底面,为锐角等于 的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
 晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。
晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。 为所取晶胞的下底面,为锐角等于
为所取晶胞的下底面,为锐角等于 的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
| A.befc | B.kecb | C.jkba | D.dchg |
您最近一年使用:0次
名校
解题方法
2 . 按照要求回答下列问题。
(1)高温下,Cu2O比CuO稳定,原因是___________ 。
(2)过渡元素的原子或者离子很容易形成配合物,Fe(CO)5就是其一,它相当活泼,在一定条件下可生成Fe(CO)3(CH3OH)。1.5 mol Fe(CO)5中所含配位键的个数为___________ ,Fe(CO)3(CH3OH)的配位原子为___________ 。(填元素符号)
(3)第四周期第一电离能数值介于Ga和As之间的主族元素有:___________ 。(填名称)
(4)金属钛重量轻、强度高,航空发动机用的高温钛合金和机体用的结构钛合金是钛合金的主要发展方向。钛原子的外围电子排布图为___________ 。已知金属Be的堆积方式与金属钛相同,则堆积方式为___________ ,Be与NaOH溶液反应的离子方程式为___________ 。
(5)Sr晶体堆积方式与Cu相似,设Sr的原子直径为a,则Sr晶体的空间利用率为___________ 。(请用含有a的表达式表示,不要化简)
(1)高温下,Cu2O比CuO稳定,原因是
(2)过渡元素的原子或者离子很容易形成配合物,Fe(CO)5就是其一,它相当活泼,在一定条件下可生成Fe(CO)3(CH3OH)。1.5 mol Fe(CO)5中所含配位键的个数为
(3)第四周期第一电离能数值介于Ga和As之间的主族元素有:
(4)金属钛重量轻、强度高,航空发动机用的高温钛合金和机体用的结构钛合金是钛合金的主要发展方向。钛原子的外围电子排布图为
(5)Sr晶体堆积方式与Cu相似,设Sr的原子直径为a,则Sr晶体的空间利用率为
您最近一年使用:0次
解题方法
3 . 下列叙述错误的是
| A.金属键无方向性和饱和性,原子配位数较高 |
| B.晶体尽量采取紧密堆积方式,以使其变得比较稳定 |
| C.因共价键有饱和性和方向性,所以原子晶体不遵循“紧密堆积”原理 |
| D.金属铜和镁均以ABAB…方式堆积 |
您最近一年使用:0次
解题方法
4 . (1)钛铁合金具有吸氢特性,工业在制造以氢为能源的热泵和蓄电池等方面有广阔的应用前景,金属Ti(六方最密堆积)的原子空间利用率约为_______ ,基态Ti原子核外有_______ 个运动状态不同的电子,在基态Ti2+中,电子占据的能量最高的轨道为_______ 。
(2)已知Si-Si键能为176 kJ/mol,Si-O键能为460 kJ/mol,O=O键能为497.3 kJ/mol,则可计算出1 mol硅与足量氧气反应时将放出_______ kJ的热量。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般为d0或d10排布时,无颜色;为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色,据此判断 [Mn(H2O)6]2+_______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。COCl2分子的空间构型为_______ ;Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g),反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______ 。
(5)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(如图),则该晶体中镁、碳、镍三种元素的原子个数比是_______ ,晶体中每个镁原子周围距离最近的镍原子有_______ 个。
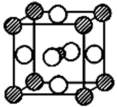
(图中:碳原子用小 球在晶体的体心,镍原子用大
球在晶体的体心,镍原子用大 球,镁原子用大
球,镁原子用大 球)
球)
(2)已知Si-Si键能为176 kJ/mol,Si-O键能为460 kJ/mol,O=O键能为497.3 kJ/mol,则可计算出1 mol硅与足量氧气反应时将放出
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般为d0或d10排布时,无颜色;为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色,据此判断 [Mn(H2O)6]2+
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。COCl2分子的空间构型为
(5)最近,由镁、镍和碳三种元素组成的化合物引起了科学家的注意。据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积(如图),则该晶体中镁、碳、镍三种元素的原子个数比是

(图中:碳原子用小
 球在晶体的体心,镍原子用大
球在晶体的体心,镍原子用大 球,镁原子用大
球,镁原子用大 球)
球)
您最近一年使用:0次
5 . 金属原子在二维空间的排列方式
(1)金属晶体中的原子可以看成直径相等的球体,在平面上(即二维空间),有两种堆积方式:
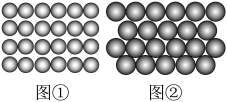
图①的堆积方式为___________ ,原子的配位数为___________ ;图②的堆积方式为___________ ,原子的配位数为___________ 。
(2)金属晶体的配位数:指距离某个原子___________ 且距离___________ 的原子个数。
(1)金属晶体中的原子可以看成直径相等的球体,在平面上(即二维空间),有两种堆积方式:

图①的堆积方式为
(2)金属晶体的配位数:指距离某个原子
您最近一年使用:0次
名校
解题方法
6 . 下表为长式周期表的一部分,其中的序号代表对应的元素。
(1)写出上表中元素⑨的三价离子的结构示意图_______ 。
(2)元素⑩的晶体中原子堆积方式是_______ ,晶体中原子的空间利用率是_______
(3)元素②的第二电离能_______ Na(填写“>”“=”或“<”)的第二电离能;元素⑨的氧化物MXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,若晶体中的M分别为M2﹢、M3﹢,此晶体中M2﹢与M3﹢的最简整数比为_______
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是_______ 。
(5)用惰性电极电解足量的由元素⑦与元素⑧形成的化合物的水溶液,写出电解反应的离子方程式为_______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |
(2)元素⑩的晶体中原子堆积方式是
(3)元素②的第二电离能
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是
(5)用惰性电极电解足量的由元素⑦与元素⑧形成的化合物的水溶液,写出电解反应的离子方程式为
您最近一年使用:0次
7 . 填写下列空白:
(1)某金属既有ccp堆积,又有hcp堆积的晶体。若ccp堆积的晶胞参数为ac,则hcp堆积的晶胞参数为:a=__________ ac,c=_________ ac。
(2)一些金属间化合物结构可看作由CsCl结构堆叠而成,例如Cr2Al。试分别以Cr原子和Al原子为顶点,画出两种晶胞___________ ,写出晶胞中原子的分数坐标___________ 、___________ 。
(1)某金属既有ccp堆积,又有hcp堆积的晶体。若ccp堆积的晶胞参数为ac,则hcp堆积的晶胞参数为:a=
(2)一些金属间化合物结构可看作由CsCl结构堆叠而成,例如Cr2Al。试分别以Cr原子和Al原子为顶点,画出两种晶胞
您最近一年使用:0次
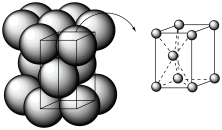
8 . 结合课本金属镁晶胞,计算镁晶胞中包含的微粒数_______ 。

您最近一年使用:0次
9 . 金属晶体类型:面心立方常见金属_______ ;体心立方常见金属_______ ;Mg、Zn、Ti等金属晶体晶胞为_______ 或者_______ ,底面中棱的夹角不是_______ 。
您最近一年使用:0次
名校
10 . 有一立方晶系的离子晶体,其结构如图所示,已知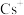 、
、 半径半径分别为
半径半径分别为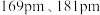 ,此两种离子联合组成的堆积型式为
,此两种离子联合组成的堆积型式为
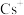 、
、 半径半径分别为
半径半径分别为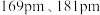 ,此两种离子联合组成的堆积型式为
,此两种离子联合组成的堆积型式为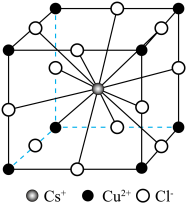
| A.简单立方 | B.面心立方 | C.体心立方 | D.六方 |
您最近一年使用:0次



