名校
1 . 如图所示为金属原子的四种基本堆积(分别为:简单立方堆积、六方最密堆积、面心立方最密堆积、体心立方堆积、)模型,请回答以下问题:
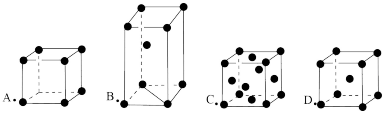
(1)图中原子堆积方式中,空间利用率最低 的是____ (在图中选择,填字母),由非密置层互相错位堆积而成的是_____ 。
(2)金属钛的晶胞为B型,其堆积方式的名称 为_____ 。
(3)某金属R的晶胞为D型,已知R原子半径为rcm,相对原子质量为M,阿佛加得德罗常数为NA,则R金属的密度____ 。(用含r、M、NA字母的式子表示)

(1)图中原子堆积方式中,空间利用率最
(2)金属钛的晶胞为B型,其堆积方式的
(3)某金属R的晶胞为D型,已知R原子半径为rcm,相对原子质量为M,阿佛加得德罗常数为NA,则R金属的密度
您最近一年使用:0次
2 . 下列说法正确的是
A. 和 和 两种晶体中, 两种晶体中, 的晶格能大 的晶格能大 |
| B.任何晶体中,若含有阳离子也一定含有阴离子 |
| C.固态不导电,熔融状态下能导电的晶体不一定是离子晶体 |
| D.分子的形状、极性以及分子之间是否存在氢键等,都会影响分子的堆积方式 |
您最近一年使用:0次
名校
3 . 根据下列示意图回答问题:

(1)①中 与
与 之间的相互作用是
之间的相互作用是___________ ,___________ (填“有”或“无”)饱和性与方向性。
(2)②、③、④是碳元素形成的不同单质,彼此互为___________ ,其中属于共价晶体的是___________ (填序号),配位数为___________ 。
(3)⑤为干冰晶胞结构示意图,解释常温常压下 为气体的原因
为气体的原因___________ 。
(4)⑥为石英晶体结构的一部分,平均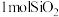 中含有
中含有___________  键,
键, 与
与 化学式相似,但熔沸点、硬度、溶解性等物理性质却有很大不同,主要原因是二者的
化学式相似,但熔沸点、硬度、溶解性等物理性质却有很大不同,主要原因是二者的___________ 不同。
(5)⑦为金属铜的晶胞结构示意图,其中含___________ 个Cu原子,铜晶体中,每个Cu原子周围最近且距离相等的Cu原子的个数为___________ 。

(1)①中
 与
与 之间的相互作用是
之间的相互作用是(2)②、③、④是碳元素形成的不同单质,彼此互为
(3)⑤为干冰晶胞结构示意图,解释常温常压下
 为气体的原因
为气体的原因(4)⑥为石英晶体结构的一部分,平均
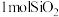 中含有
中含有 键,
键, 与
与 化学式相似,但熔沸点、硬度、溶解性等物理性质却有很大不同,主要原因是二者的
化学式相似,但熔沸点、硬度、溶解性等物理性质却有很大不同,主要原因是二者的(5)⑦为金属铜的晶胞结构示意图,其中含
您最近一年使用:0次
2021高三·全国·专题练习
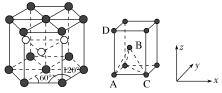
4 . 某金属晶体中原子的堆积方式如图所示,已知该金属的原子半径为a cm,晶胞的高为b cm,A、C、D三点原子的坐标参数分别为A(0,0,0)、C(2a,0,0)、D(0,0,b),则B点原子的坐标参数为___________ 。

您最近一年使用:0次
名校
5 . 金属铁因生产工艺和温度不同,会有不同的晶体结构。α-Fe和γ-Fe的晶体结构如图所示,下列说法正确的是
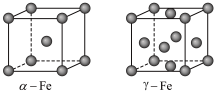
| A.金属铁因为有自由移动的离子而具有导电性 | B.1个γ-Fe晶胞的质量约为(4×56)g |
| C.γ-Fe中铁原子的配位数为12 | D.α-Fe与γ-Fe的性质相同 |
您最近一年使用:0次
2024-05-17更新
|
105次组卷
|
2卷引用: 河北省邢台市2023-2024学年高二下学期期中考试化学试卷
6 . 硼、铝、镓、铟、铊位于元素周期表第ⅢA族,统称为硼族元素,它们的单质及化合物在工农业生产中有着重要的应用。
(1)基态镓原子的外围电子排布式为_______ 。
(2)硼酸晶体具有层状结构,每一层的平面层状结构如图1所示。硼酸分子中B原子采取_______ 杂化;晶体平面层内所含有作用力类型有_______ 。
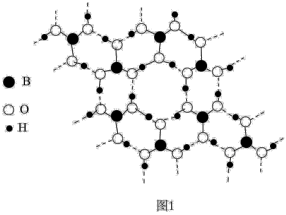
(3)工业上通常用电解法冶炼铝。已知Al2O3熔点为2054℃、AlCl3熔点为194℃,冶炼铝时应选择电解熔融_______ (填化学式),理由是_______ 。
(4)冰晶石(Na3AlF6)是炼铝的助熔剂,由两种离子构成,其中阴离子具有正八面体结构,写出该阴离子的化学式_______ ,与该阴离子互为等电子体的分子有_______ 。
(5)铊具有三种晶体结构:低于230℃时为六方最密堆积(α-Tl),230℃以上转化为体心立方堆积(β-Tl),在高压下形成面心立方最密堆积(γ-Tl),晶胞结构如图2所示。
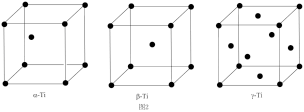
三种铊的晶体中,铊的配位数之比(α:β:γ)为_______ .若铊原子半径为a pm,则β-Tl中铊原子间最短距离为_______ pm (用含a的式子表示,下同),γ-Tl晶体的密度计算式为ρ=_______ g/cm3(设NA为阿伏加德罗常数的值)。
(1)基态镓原子的外围电子排布式为
(2)硼酸晶体具有层状结构,每一层的平面层状结构如图1所示。硼酸分子中B原子采取

(3)工业上通常用电解法冶炼铝。已知Al2O3熔点为2054℃、AlCl3熔点为194℃,冶炼铝时应选择电解熔融
(4)冰晶石(Na3AlF6)是炼铝的助熔剂,由两种离子构成,其中阴离子具有正八面体结构,写出该阴离子的化学式
(5)铊具有三种晶体结构:低于230℃时为六方最密堆积(α-Tl),230℃以上转化为体心立方堆积(β-Tl),在高压下形成面心立方最密堆积(γ-Tl),晶胞结构如图2所示。

三种铊的晶体中,铊的配位数之比(α:β:γ)为
您最近一年使用:0次
名校
解题方法
7 . 下列有关晶体堆积模型和晶胞的说法错误的是


| A.图①、图②和图③都是最密堆积,图④的空间占有率是图中最小的 |
| B.从左至右的配位数依次为12、12、12、6、8 |
| C.图①可以表示氯化钠晶胞中氯离子的堆积方式 |
| D.铜晶体、碳化硅晶体中的硅原子、硫化锌晶体中的硫离子都采用图③中的最密堆积 |
您最近一年使用:0次
8 . 某晶体由a,b两种元素组成,可看作a作简单立方堆积,b有序地填入一半的立方体空隙,每当一个立方体空隙填入b后,与之相邻的立方体空隙均不填原子,则下列说法错误的是
| A.a可以看作填入b堆积的八面体空隙中 | B.该化合物的化学式为a2b |
| C.该化合物具有萤石型结构 | D.若b将全部立方体空隙填满,则为CsCl型结构 |
您最近一年使用:0次
2023-05-25更新
|
241次组卷
|
2卷引用:2023年广西高中学生竞赛(高一、高二同卷)化学试题
2021高三·全国·专题练习
解题方法
9 . 钛晶体中配位数为___________ ,
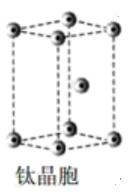

您最近一年使用:0次
10 . 铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途,如二茂铁可用作火箭燃料添加剂,含铁等磁性材料被广泛应用于电子信息、军事技术等领域。根据题目信息回答下列问题:
(1)基态Fe原子的电子排布式为_______ 。
(2)二茂铁(C5H5)2Fe是一种浅黄色难溶于水的液体,其熔点-20℃,沸点103℃。依据以上信息可推断二茂铁属于_______ (“离子晶体”、“分子晶体”或“原子晶体”)。
(3)独立的NH3分子中,H-N-H键键角为107.3,下图是[Zn(NH3)6]2+离子的部分结构以及其中H-N-H键键角。
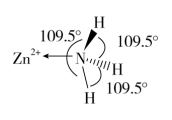
请解释[Zn(NH3)6]2+离子中H-N-H键角变为109.5的原因是_______ 。
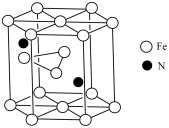
(4)某种磁性氮化铁的结构如下图所示,Fe的堆积方式为_______ ,则该化合物的化学式为_______ ;氮化铁晶胞底边长为a pm,高为b pm,则这种磁性氮化铁的晶体密度为_______ g·cm-3 (用含a、b和NA的计算式表示)。
(1)基态Fe原子的电子排布式为
(2)二茂铁(C5H5)2Fe是一种浅黄色难溶于水的液体,其熔点-20℃,沸点103℃。依据以上信息可推断二茂铁属于
(3)独立的NH3分子中,H-N-H键键角为107.3,下图是[Zn(NH3)6]2+离子的部分结构以及其中H-N-H键键角。

请解释[Zn(NH3)6]2+离子中H-N-H键角变为109.5的原因是
(4)某种磁性氮化铁的结构如下图所示,Fe的堆积方式为

您最近一年使用:0次



