硼、铝、镓、铟、铊位于元素周期表第ⅢA族,统称为硼族元素,它们的单质及化合物在工农业生产中有着重要的应用。
(1)基态镓原子的外围电子排布式为_______ 。
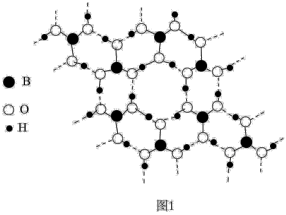
(2)硼酸晶体具有层状结构,每一层的平面层状结构如图1所示。硼酸分子中B原子采取_______ 杂化;晶体平面层内所含有作用力类型有_______ 。
(3)工业上通常用电解法冶炼铝。已知Al2O3熔点为2054℃、AlCl3熔点为194℃,冶炼铝时应选择电解熔融_______ (填化学式),理由是_______ 。
(4)冰晶石(Na3AlF6)是炼铝的助熔剂,由两种离子构成,其中阴离子具有正八面体结构,写出该阴离子的化学式_______ ,与该阴离子互为等电子体的分子有_______ 。
(5)铊具有三种晶体结构:低于230℃时为六方最密堆积(α-Tl),230℃以上转化为体心立方堆积(β-Tl),在高压下形成面心立方最密堆积(γ-Tl),晶胞结构如图2所示。
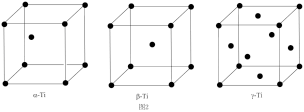
三种铊的晶体中,铊的配位数之比(α:β:γ)为_______ .若铊原子半径为a pm,则β-Tl中铊原子间最短距离为_______ pm (用含a的式子表示,下同),γ-Tl晶体的密度计算式为ρ=_______ g/cm3(设NA为阿伏加德罗常数的值)。
(1)基态镓原子的外围电子排布式为
(2)硼酸晶体具有层状结构,每一层的平面层状结构如图1所示。硼酸分子中B原子采取

(3)工业上通常用电解法冶炼铝。已知Al2O3熔点为2054℃、AlCl3熔点为194℃,冶炼铝时应选择电解熔融
(4)冰晶石(Na3AlF6)是炼铝的助熔剂,由两种离子构成,其中阴离子具有正八面体结构,写出该阴离子的化学式
(5)铊具有三种晶体结构:低于230℃时为六方最密堆积(α-Tl),230℃以上转化为体心立方堆积(β-Tl),在高压下形成面心立方最密堆积(γ-Tl),晶胞结构如图2所示。

三种铊的晶体中,铊的配位数之比(α:β:γ)为
更新时间:2022-01-13 08:23:03
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】工业级氯化钙(CaCl2)通常用作道路的融雪除冰和干燥剂,主要利用纯碱工业废液生产。完成下列填空:
(1)氯原子的核外电子排布式_______ ;氯化钙的电子式_______ ;比较构成CaCl2的微粒半径大小(用微粒符号表示)_______
(2)纯碱生产的工业方法有多种,其中废液含有大量氯化钙的是_______ 制碱法
(3)氯化钙不能干燥NH3,因为CaCl2(s)+8NH3(g)⇌CaCl2·8NH3(s)+Q(Q>0),该反应的平衡常数K=_______ ;向2L装有CaCl2的密闭容器中,通入2molNH3,反应10分钟,固体增重17g,则0~10分钟内,NH3的平均反应速率v=_______ ;若要将已吸收的CaCl2重新恢复吸收NH3的能力,写出一种可采取的措施_______
(1)氯原子的核外电子排布式
(2)纯碱生产的工业方法有多种,其中废液含有大量氯化钙的是
(3)氯化钙不能干燥NH3,因为CaCl2(s)+8NH3(g)⇌CaCl2·8NH3(s)+Q(Q>0),该反应的平衡常数K=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

(1)X原子的价电子排布式是:______________________________________ ;
(2)M元素在周期表中的位置是第______ 周期第_______ 族;
(3)Q、R、M的第一电离能由大到小的顺序是_______________ (用元素符号表示);
(4)E与Q所形成的化合物含________ 键,属________ 分子。(填“极性”或“非极性”)
(5)Fe2+与Mn2+两种离子,________ 更容易再失去1个电子,原因是______________________________________________________________________________________________________ 。
(6)用氢键表示式写出W的氢化物溶液中存在的所有氢键______________________ 。

(1)X原子的价电子排布式是:
(2)M元素在周期表中的位置是第
(3)Q、R、M的第一电离能由大到小的顺序是
(4)E与Q所形成的化合物含
(5)Fe2+与Mn2+两种离子,
(6)用氢键表示式写出W的氢化物溶液中存在的所有氢键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】第四次工业革命(工业4.0)开启了智能化时代,高质量的单晶硅是“芯片”的基础,“芯片”是智能的心脏。
(1)下列对于基态硅原子的叙述正确的是___________ (填标号)。
a.原子轨道电子排布半充满时体系能量最低,电子排布式为
b. 轨道的电子总是比
轨道的电子总是比 轨道的电子在离核更远的区域运动
轨道的电子在离核更远的区域运动
c.电负性比 高,原子对键合电子的吸引力比
高,原子对键合电子的吸引力比 大
大
(2)近年来美国为了遏制中国发展,对我国发起了以封锁“芯片”为核心的全方位打压,此举激发了中国科技人员自研的决心。2022年10月宁波南大光电 光刻胶生产线正式投产,国内
光刻胶生产线正式投产,国内 芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:
芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:

①该聚碳酸酯中碳原子的杂化方式为___________ ;
②聚碳酸酯膜曝光后的产物加热可汽化或溶于水,加热汽化或溶于水克服的作用力有___________ 。
(3)有机高分子聚合物中掺杂氧化锆等可导电的固体电解质可以提高光刻胶的性能。
①锆是第5周期ⅣB元素,则基态锆原子的价电子排布式为___________ ;
②氟化钙 (CaF2)和氧化锆(ZrO2)的晶体结构如下图,氧化锆的熔点(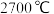 )高于氟化钙(
)高于氟化钙( ),原因是
),原因是___________ 。

(1)下列对于基态硅原子的叙述正确的是
a.原子轨道电子排布半充满时体系能量最低,电子排布式为

b.
 轨道的电子总是比
轨道的电子总是比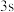 轨道的电子在离核更远的区域运动
轨道的电子在离核更远的区域运动c.电负性比
 高,原子对键合电子的吸引力比
高,原子对键合电子的吸引力比 大
大(2)近年来美国为了遏制中国发展,对我国发起了以封锁“芯片”为核心的全方位打压,此举激发了中国科技人员自研的决心。2022年10月宁波南大光电
 光刻胶生产线正式投产,国内
光刻胶生产线正式投产,国内 芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:
芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:
①该聚碳酸酯中碳原子的杂化方式为
②聚碳酸酯膜曝光后的产物加热可汽化或溶于水,加热汽化或溶于水克服的作用力有
(3)有机高分子聚合物中掺杂氧化锆等可导电的固体电解质可以提高光刻胶的性能。
①锆是第5周期ⅣB元素,则基态锆原子的价电子排布式为
②氟化钙 (CaF2)和氧化锆(ZrO2)的晶体结构如下图,氧化锆的熔点(
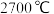 )高于氟化钙(
)高于氟化钙( ),原因是
),原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A、B、C、D、E为周期表前四周期原子序数依次增大的五种元素。其中A的基态原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍,它的一种单质是天然存在硬度最大的物质;C的基态原子2p能级上的未成对电子数与A原子的相同;D和C位于同一主族,E3+ 离子3d轨道半充满。
(1)E在元素周期表的位置:______________________ 。
(2)在A、B、C三种元素中,第一电离能由大到小的顺序是___________ (用元素符号回答)。
(3)元素B的简单气态氢化物极易溶于水,原因是_____________________ 。
(4)元素C与D所形成的高价化合物分子的立体构型为___________________ 。
(5)化合物X是元素A和C形成的三原子分子,与其互为等电子体的微粒有__________ 。(只写一个)
(6)从原子结构的角度解释E3+比E2+稳定的原因________________________________ 。
(1)E在元素周期表的位置:
(2)在A、B、C三种元素中,第一电离能由大到小的顺序是
(3)元素B的简单气态氢化物极易溶于水,原因是
(4)元素C与D所形成的高价化合物分子的立体构型为
(5)化合物X是元素A和C形成的三原子分子,与其互为等电子体的微粒有
(6)从原子结构的角度解释E3+比E2+稳定的原因
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:

(1)元素p为26号元素,请写出其基态原子的电子排布式___________ ,该元素的价电子排布图___________ 。
(2)d与a的单质反应生成的产物分子中,中心原子的杂化形式为___________ ,分子空间构型为___________ 。d、e元素分别形成的两种简单氢化物中键角较大的是___________ ,原因是___________ 。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:___________ 。
(4)o、p两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此你的解释是___________ 。
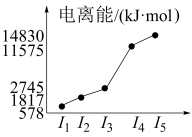
(5)表中所列的某主族元素的电离能情况如图所示,则该元素是___________ (填元素符号)。

(1)元素p为26号元素,请写出其基态原子的电子排布式
(2)d与a的单质反应生成的产物分子中,中心原子的杂化形式为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
(5)表中所列的某主族元素的电离能情况如图所示,则该元素是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)③和①形成的一种5核10电子分子,其立体构型为_______ ,中心原子杂化方式为_______ ,属于_______ 分子(填“极性”或“非极性”)。
(2)元素③和⑦的最高价氧化物对应水化物中酸性较强的是:_______ (填化学式),元素⑥的电负性_______ 元素⑦(选填“>”、“=”、“<”=)的电负性。
(3)根据元素周期表分区,元素⑨位于_______ 区,其基态原子电子排布式为_______ 。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的离子方程式_______ 。
(5)⑩的离子与4个H2O分子形成的阳离子中含的化学键有_______ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
| ⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)③和①形成的一种5核10电子分子,其立体构型为
(2)元素③和⑦的最高价氧化物对应水化物中酸性较强的是:
(3)根据元素周期表分区,元素⑨位于
(4)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的离子方程式
(5)⑩的离子与4个H2O分子形成的阳离子中含的化学键有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】R、X、Y、Z是周期表前四周期元素,原子序数依次增大。R是宇宙中含量最多的元素,X、Y、Z三种元素的基态原子内层所有能级均已填满电子。X元素的基态原子的核外电子分布在三个能级上,且每个能级上排布了相同的电子数。Y与X同周期,且Y与X的基态原子中未成对电子数相同。Z的周期数比X的周期数多2,Z的基态原子最外层只有1个电子。回答下列问题:
(1)Z元素的价电子排布式为____________ 。
(2)R2Y可与Z的正二价离子形成一种复杂离子[Z(R2Y)4]2+,[Z(R2Y)4]2+的几何构型是______ ;将[Z(R2Y)4]2+与硫酸根形成的盐溶液装入试管中,逐滴加入氨水直至过量,出现的实验现象是______________ 。
(3)X与R可形成一种化学式为X3R4的不稳定化合物,是一种活性中间体,X3R4分子中3个X原子成直线排列,中间的X原子的杂化轨道类型为_____ 杂化。当X3R4分子中的4个R原子被其他4个不同种类元素的原子取代时,形成的新分子___ (填“具有“或”不具有”)手性。
(4)下列排列方式中,通常条件下Z的晶体的堆积方式是______ (填序号)。Z的晶体中,Z原子的配位数为________ 。
A.ABCABCABC B.ABABABABAB C.ABBAABBA D.ABCCBCABCCBA
(5)Z与F(氟)形成的一种化合物的晶胞结构如右图所示,若晶体密度为ag.cm-3,则Z与F(氟)最近距离为______ pm(阿伏伽德罗常数用NA表示,列出计算表达式,不用化简,1 pm=1. 0×10-12 m)。

(1)Z元素的价电子排布式为
(2)R2Y可与Z的正二价离子形成一种复杂离子[Z(R2Y)4]2+,[Z(R2Y)4]2+的几何构型是
(3)X与R可形成一种化学式为X3R4的不稳定化合物,是一种活性中间体,X3R4分子中3个X原子成直线排列,中间的X原子的杂化轨道类型为
(4)下列排列方式中,通常条件下Z的晶体的堆积方式是
A.ABCABCABC B.ABABABABAB C.ABBAABBA D.ABCCBCABCCBA
(5)Z与F(氟)形成的一种化合物的晶胞结构如右图所示,若晶体密度为ag.cm-3,则Z与F(氟)最近距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硅材料和铝材料在生产生活中应用广泛。回答下列问题:
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a.([Ne]3s23p2)、b.([Ne]3s23p1)、c.([Ne]3s23p14s1),半径由大到小的顺序为_______ (填标号);第三周期元素中,第一电离能介于Al和P之间的元素有_______ 种。
(2)N(SiH3)3是一种高介电常数材料。已知:N(SiH3)3中Si-N-Si键角120°,N(CH3)3中C-N-C键角111°。共价键的极性Si-N_______ C-N(填“>”、“=”或“<”)。下列划线原子与N(SiH3)3中N原子杂化类型相同的是_______ (填标号)。
A.Al(OCH3)3 B.NH3BH3 C.N(CH3)3 D.NH4NO3
(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝的原因是_______ 。
(4)已知合金Na2AlAu3的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入Au3Al四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。
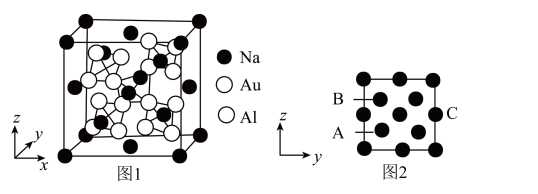
每个Na周围距离其最近的Na有_______ 个;以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点的分数坐标为( ,
, ,
, ),则B点的分数坐标为
),则B点的分数坐标为_______ ;设NA为阿伏加德罗常数的值,Na2AlAu3的摩尔质量为Mg•mol-1,晶体的密度为ρg•cm-3,则A、C两原子间的距离为_______ pm(列出计算表达式)。
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a.([Ne]3s23p2)、b.([Ne]3s23p1)、c.([Ne]3s23p14s1),半径由大到小的顺序为
(2)N(SiH3)3是一种高介电常数材料。已知:N(SiH3)3中Si-N-Si键角120°,N(CH3)3中C-N-C键角111°。共价键的极性Si-N
A.Al(OCH3)3 B.NH3BH3 C.N(CH3)3 D.NH4NO3
(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝的原因是
(4)已知合金Na2AlAu3的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入Au3Al四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。

每个Na周围距离其最近的Na有
 ,
, ,
, ),则B点的分数坐标为
),则B点的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】如图是超导化合物——钙钛矿晶体中最小重复单元(晶胞)的结构。请回答:

(1)该化合物的化学式为_______ 。
(2)在该化合物晶体中,与某个钛原子距离最近且相等的其他钛原子共有______ 个。
(3)设该化合物的相对分子质量为M,密度为ag•cm-3,阿伏加德罗常数的值为NA,则晶体中钙原子与钛原子之间的最短距离为______ 。
(4)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示。处于顶角位置的是______ 原子。设Cr和Al原子半径分别为rCr和rAl,则金属原子空间占有率为_______ %(列出计算表达式)。
(5)体心灰球的空间坐标为_______ 。


(1)该化合物的化学式为
(2)在该化合物晶体中,与某个钛原子距离最近且相等的其他钛原子共有
(3)设该化合物的相对分子质量为M,密度为ag•cm-3,阿伏加德罗常数的值为NA,则晶体中钙原子与钛原子之间的最短距离为
(4)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示。处于顶角位置的是
(5)体心灰球的空间坐标为

您最近一年使用:0次
【推荐1】金属晶体中金属原子主要有三种常见的堆积方式:体心立方堆积、面心立方堆积和六方堆积,其结构单元分别如下图中甲、乙、丙所示,则甲、乙、丙三种结构单元中,金属原子个数比为________ 。


您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知X、Y、Z、W、R都是周期表中前四周期的元素,它们的核电荷数依次增大。X原子有1个2p空轨道,Y原子最外层电子数等于X原子核外电子总数,Z与X同主族,W原子3p轨道只有一个单电子,R3+的3d轨道为半充满状态。回答下列问题:
(1)元素X、Y、Z的电负性由大到小的顺序是__ (用元素符号表示)。
(2)元素X、Z的最简单气态氢化物的沸点由高到低的顺序是__ (用化学式表示)。
(3)元素X、Y形成的一种化合物在高温高压下所形成的晶体其晶胞如图所示,则该晶体类型属于__ 晶体,1个晶胞中含有__ 个X原子。

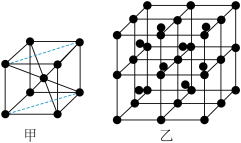
(4)R的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的图A~D中正确的是__ (填字母标号)。
A.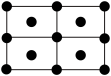 B.
B.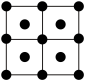 C.
C.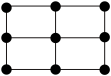 D.
D.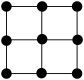
假设R原子的半径是apm,则该晶体的密度的计算式是__ g·cm-3(用含a的式子表示,设阿伏加 德罗常数的值为NA)。
(1)元素X、Y、Z的电负性由大到小的顺序是
(2)元素X、Z的最简单气态氢化物的沸点由高到低的顺序是
(3)元素X、Y形成的一种化合物在高温高压下所形成的晶体其晶胞如图所示,则该晶体类型属于

(4)R的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的图A~D中正确的是

A.
 B.
B. C.
C. D.
D.
假设R原子的半径是apm,则该晶体的密度的计算式是
您最近一年使用:0次
【推荐3】氮元素可形成很多重要的化合物,其中叠氮化钠(NaN3)被广泛应用于汽车安全气囊。叠氮化钠的制取方法是:①金属钠与液态氨反应得NaNH2②NaNH2与N2O按物质的量2:1反应可生成NaN3、NaOH和一种气体。
(1)请写出反应②的化学方程式为:____________ 。
(2)与N3-互为等电子体的分子有:______ (写一种)由此可推知N3-的空间构型是:_________ ; 比较NH2-和NH3的键角∠HNH的大小:NH2-____ NH3(填“>”或“<”或“=”),请用价层电子对互斥规律解释_______ 。
(3)叠氮化钠(NaN3)分解可得纯N2,有关说法正确的是:________ (选填代号)
A.氮气常温下很稳定,是因为氮元素的电负性大
B.NaN3与KN3结构类似,前者晶格能较小
C.第一电离能(I1):N>P>S
D.热稳定性NH3强于PH3和H2S是因为NH3分子间有氢键
(4)小汽车的防撞气囊中叠氮化钠的工作原理是基于反应:6NaN3+ Fe2O3 = 3Na2O + 2Fe+ 9N2;铁晶体有三种堆积方式,其中两种堆积方式分别如图甲、图乙所示(其晶胞特征如下图所示):

晶胞甲中铁原子的配位数为:_______ ,晶胞乙中铁原子的堆积方式为:________ 。晶胞乙中铁原子半径为a cm,NA表示阿伏加 德罗常数,摩尔质量为M g/mol。则该晶体的密度可表示为:___________ g/cm3。
(1)请写出反应②的化学方程式为:
(2)与N3-互为等电子体的分子有:
(3)叠氮化钠(NaN3)分解可得纯N2,有关说法正确的是:
A.氮气常温下很稳定,是因为氮元素的电负性大
B.NaN3与KN3结构类似,前者晶格能较小
C.第一电离能(I1):N>P>S
D.热稳定性NH3强于PH3和H2S是因为NH3分子间有氢键
(4)小汽车的防撞气囊中叠氮化钠的工作原理是基于反应:6NaN3+ Fe2O3 = 3Na2O + 2Fe+ 9N2;铁晶体有三种堆积方式,其中两种堆积方式分别如图甲、图乙所示(其晶胞特征如下图所示):

晶胞甲中铁原子的配位数为:
您最近一年使用:0次



