名校
1 . 已知某离子晶体的晶胞示意图如图所示,其摩尔质量为Mg/mol,阿伏加德罗常数的值为NA,晶体的密度为dg/cm3,下列说法中正确的是
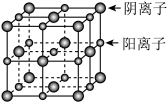

| A.晶体晶胞中阴、阳离子的个数都为1 |
| B.晶体中阴、阳离子的配位数都是4 |
| C.该晶胞可能是CsCl的晶胞 |
D.该晶体中两个距离最近的阳离子的核间距为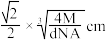 |
您最近一年使用:0次
2 . F、K和Ni三种元素组成的一种化合物的晶胞如图所示。下列说法错误的是
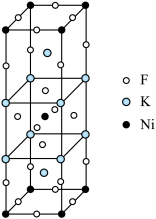

| A.Ni位于元素周期表d区 | B.该物质的化学式为K2NiF4 |
| C.Ni的配位数为6 | D.该晶体属于分子晶体 |
您最近一年使用:0次
2022-01-13更新
|
500次组卷
|
3卷引用:吉林省长春外国语学校2022-2023学年高二下学期7月期末考试化学试题
3 . 过渡金属元素铬 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是_______ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s轨道上电子能量较高,总是在比3s轨道上电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是_______ ,中心离子的配位数为_______ 。
(3) 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。
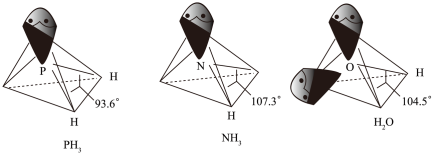
 中P的杂化类型是
中P的杂化类型是_______ 。 的沸点比
的沸点比 的
的_______ ,原因是_______ , 的键角小于
的键角小于 的,分析原因
的,分析原因_______ 。
(4)在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示,处于顶角位置的是
具有体心四方结构,如图所示,处于顶角位置的是_______ 原子。设Cr和Al原子半径分别为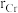 和
和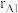 ,则金属原子空间占有率为
,则金属原子空间占有率为_______ %(列出计算表达式)。

 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:(1)对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为

B.4s轨道上电子能量较高,总是在比3s轨道上电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(3)
 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。
 中P的杂化类型是
中P的杂化类型是 的沸点比
的沸点比 的
的 的键角小于
的键角小于 的,分析原因
的,分析原因(4)在金属材料中添加
 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示,处于顶角位置的是
具有体心四方结构,如图所示,处于顶角位置的是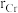 和
和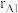 ,则金属原子空间占有率为
,则金属原子空间占有率为
您最近一年使用:0次
2021-06-09更新
|
20277次组卷
|
19卷引用:吉林省汪清县汪清四中2020-2021学年高二下学期期末考试化学试题
吉林省汪清县汪清四中2020-2021学年高二下学期期末考试化学试题吉林省长春外国语学校2020-2021学年高二下学期第二次月考化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二下学期期末考试化学试题2021年高考全国乙卷化学真题(已下线)专题14 物质结构与性质-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国乙卷化学试题变式题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)广东省茂名市电白区2021-2022学年高二下学期期中(选择性)考试化学试题(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)广东省广州市真光中学2022-2023学年高二下学期期中考试化学试题(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)
4 . 下列关于氯化铯晶体的叙述不正确的是( )
| A.1 mol氯化铯中有6.02×1023个CsCl分子 |
| B.氯化铯晶体中,每个Cs+周围与它最近且等距离的Cs+有6个 |
| C.氯化铯晶体中,Cs+和Cl-的配位数都是8 |
| D.每个晶胞中平均含有1个Cs+和1个Cl- |
您最近一年使用:0次
2020-08-28更新
|
227次组卷
|
4卷引用:吉林省通化县综合高级中学2019-2020学年高二下学期期末考试化学试题
5 . 下列说法正确的是
| A.Na2O2晶体中,阴、阳离子个数比是1∶1 |
| B.NaCl晶胞中有1个Na+和1个Cl- |
| C.CaF2晶体中,Ca2+和F-的配位数之比为1∶2 |
| D.CsCl晶胞中,Cl-的配位数是8 |
您最近一年使用:0次
2018-12-26更新
|
141次组卷
|
3卷引用:吉林省汪清县汪清四中2020-2021学年高二下学期期末考试化学试题
6 . 元素及其化合物的应用研究是目前科学研究的前沿之一。试回答下列问题:
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出A 在基态时的外围电子排布式为______________ 。
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。水分子中心原子价层电子对数为_______ ,苯分子中碳原子的杂化类型为________ 。
(3)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+ 等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。该盐中铑离子的配位数为____ 。
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出A 在基态时的外围电子排布式为
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。水分子中心原子价层电子对数为
(3)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+ 等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。该盐中铑离子的配位数为
您最近一年使用:0次
2017-07-21更新
|
26次组卷
|
2卷引用:吉林省扶余一中2016-2017学年高二下学期期末考试化学试题



