解题方法
1 . 下列有关物质的说法正确的是
| A.HCl溶解于水,离子键被破坏 |
| B.碘升华中断裂的化学键是非极性共价键 |
| C.氢氧化钠溶于水破坏了离子键和极性共价键 |
| D.卤素单质的熔沸点随原子序数增大而增大和分子间作用力有关 |
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
2 . 下列说法不正确的是
| A.硅晶体和二氧化硅晶体中都含共价键 |
| B.Cl2、Br2、I2 的沸点逐渐升高,是因为分子间作用力越来越大 |
| C.硫酸和硫酸钠均属于离子化合物 |
| D.氯气和氯化氢分子中的氯原子的最外电子层都形成了具有8个电子的稳定结构 |
您最近一年使用:0次
3 . 有下列说法:①分子间作用力越大,分子越稳定;②离子化合物中只含有离子键;③共价化合物一定不含离子键;④氯化钠溶解于水时离子键未被破坏;⑤冰融化时水分子 中的共价键发生了断裂;⑥所有离子化合物中都含有金属元素;⑦由分子构成的物质 一定含有共价键;其中正确的有几项
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
21-22高一上·浙江·阶段练习
4 . 下列说法不正确的是
| A.NaHSO4晶体溶于水和受热熔化时破坏的化学键类型不完全相同 |
| B.干冰和碘单质易升华,都是因为分子内原子间作用力较小 |
| C.氧化钠晶体和氟化镁晶体均属于离子化合物 |
| D.氯气中的氯原子和氯化钙中的氯离子,最外电子层都具有8电子的稳定结构 |
您最近一年使用:0次
名校
解题方法
5 . 下列关于晶体的说法正确的个数是
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、 、
、 晶体的熔点依次降低
晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤形成氢键的三个原子不一定在同一条直线上
⑥ 晶体中每个硅原子与两个氧原子以共价键相结合
晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、
 、
、 晶体的熔点依次降低
晶体的熔点依次降低④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤形成氢键的三个原子不一定在同一条直线上
⑥
 晶体中每个硅原子与两个氧原子以共价键相结合
晶体中每个硅原子与两个氧原子以共价键相结合⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
2022-07-18更新
|
241次组卷
|
2卷引用:重庆市西南大学附属中学校2021-2022学年高一广延班下学期期末考试化学试题
解题方法
6 . 下列说法不正确的是
①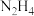 分子中既含极性键又含非极性键
分子中既含极性键又含非极性键
②只要有化学键断裂的过程就是化学变化
③干冰升华会破坏共价键
④水分子很稳定是由于水分子之间存在共价键
⑤ 、
、 、
、 、
、 分子中各原子最外层均达到8电子稳定结构
分子中各原子最外层均达到8电子稳定结构
⑥ 固体中的阴离子和阳离子个数比是1:2
固体中的阴离子和阳离子个数比是1:2
①
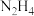 分子中既含极性键又含非极性键
分子中既含极性键又含非极性键②只要有化学键断裂的过程就是化学变化
③干冰升华会破坏共价键
④水分子很稳定是由于水分子之间存在共价键
⑤
 、
、 、
、 、
、 分子中各原子最外层均达到8电子稳定结构
分子中各原子最外层均达到8电子稳定结构⑥
 固体中的阴离子和阳离子个数比是1:2
固体中的阴离子和阳离子个数比是1:2| A.②④⑤ | B.①③④ | C.②③④ | D.③④⑥ |
您最近一年使用:0次
7 . 有关晶体的下列说法中错误的是
| A.氯化钠熔化时破坏了离子键 | B.水汽化时主要破坏了分子间作用力 |
| C.原子晶体中共价键越强,熔点越高 | D.分子晶体中分子间作用力越大,分子越稳定 |
您最近一年使用:0次
解题方法
8 . 下列说法错误的是
| A.凡是含有离子键的晶体一定是离子晶体 |
| B.离子晶体中可能含有共价键 |
| C.分子晶体的本质特征是熔,沸点较低 |
| D.共价化合物形成的晶体不一定是分子晶体 |
您最近一年使用:0次
名校
9 . 下列说法不正确的是
| A.碘单质的升华过程中,只需克服分子间作用力 |
| B.化学键的断裂与形成一定伴随着电子的转移和能量变化. |
| C.BaCl2属于离子化合物,该晶体中只存在离子键 |
| D.NaHSO4和 NaHCO3两种晶体溶于水时,被破坏的作用力既有离子键又有共价键 |
您最近一年使用:0次
名校
解题方法
10 . 下列说法不正确的是
| A.氯化铵固体受热分解破坏了离子键 |
| B.由于H-O键比H-S键牢固,所以水的熔沸点比H2S高 |
| C.F2、Cl2、Br2、I2熔沸点逐渐升高,是因为它们的组成结构相似,分子间的范德华力增大 |
| D.金属元素的最高价氧化物对应水化物的碱性越强,金属性就越强 |
您最近一年使用:0次



