1 . 化学与生产、生活、科技密切相关。下列说法错误的是
A.《淮南子》最早记载,熟石膏可作为制作豆腐时的凝固剂,其化学式为 |
| B.将石油裂化为轻质汽油后燃烧比直接燃烧石油更有利于实现碳中和 |
C.《本草经集注》中区分硝石 和朴消 和朴消 的方法:“以火烧之,紫青烟起,乃真硝石也”,这是利用了焰色试验 的方法:“以火烧之,紫青烟起,乃真硝石也”,这是利用了焰色试验 |
| D.《肘后备急方》载:“青蒿一握,以水二升渍,绞取汁”,现代基于此法提取青蒿中的青蒿素所代表的操作中,使用的玻璃仪器为分液漏斗和烧杯 |
您最近一年使用:0次
名校
解题方法
2 . 以工业废铜泥[主要成分为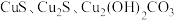 ,含少量
,含少量 ]为主要原料制备
]为主要原料制备 产品的工艺流程如下。下列说法错误的是
产品的工艺流程如下。下列说法错误的是
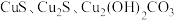 ,含少量
,含少量 ]为主要原料制备
]为主要原料制备 产品的工艺流程如下。下列说法错误的是
产品的工艺流程如下。下列说法错误的是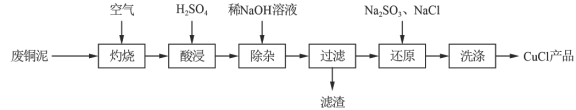
A.除杂时,应在加入稀 溶液前加入稍过量的过氧化氢溶液 溶液前加入稍过量的过氧化氢溶液 |
| B.在“除杂”后、“过滤”前应适当加热以保证除杂效果 |
C.由核外电子排布知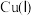 比 比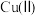 稳定,但水相中少见 稳定,但水相中少见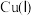 化合物的原因是 化合物的原因是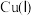 在水相中易歧化 在水相中易歧化 |
D.洗涤时,应当用浓盐酸洗涤以减少 产品在洗涤过程中的损失 产品在洗涤过程中的损失 |
您最近一年使用:0次
名校
解题方法
3 . 合成甲基橙( ,分子量为327,变色范围
,分子量为327,变色范围 值为
值为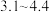 )的实验步骤如下:
)的实验步骤如下:
①在一支试管中加入 对氨基苯磺酸(分子量为173),
对氨基苯磺酸(分子量为173),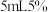 的氢氧化钠溶液,使其溶解,另加入
的氢氧化钠溶液,使其溶解,另加入 亚硝酸钠溶于
亚硝酸钠溶于 水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有
水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有 水和
水和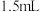 浓盐酸的烧杯中,温度始终保持在
浓盐酸的烧杯中,温度始终保持在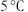 以下,直至产生白色沉淀(已知此反应大量放热)。
以下,直至产生白色沉淀(已知此反应大量放热)。
②在试管中将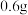 的N,N-二甲基苯胺(分子量为121)和
的N,N-二甲基苯胺(分子量为121)和 冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌
冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌 ,此时溶液为深红色。在搅拌下,慢慢加入
,此时溶液为深红色。在搅拌下,慢慢加入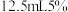 氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约
氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约 。
。
③将粗产品用0.4%的氢氧化钠水溶液进行重结晶,得到橙黄色明亮的小叶片状晶体。
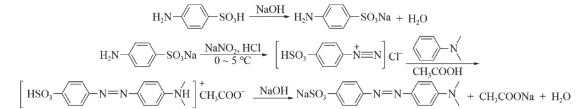
根据上述实验原理,下列说法错误的是
 ,分子量为327,变色范围
,分子量为327,变色范围 值为
值为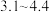 )的实验步骤如下:
)的实验步骤如下:①在一支试管中加入
 对氨基苯磺酸(分子量为173),
对氨基苯磺酸(分子量为173),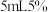 的氢氧化钠溶液,使其溶解,另加入
的氢氧化钠溶液,使其溶解,另加入 亚硝酸钠溶于
亚硝酸钠溶于 水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有
水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有 水和
水和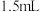 浓盐酸的烧杯中,温度始终保持在
浓盐酸的烧杯中,温度始终保持在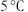 以下,直至产生白色沉淀(已知此反应大量放热)。
以下,直至产生白色沉淀(已知此反应大量放热)。②在试管中将
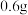 的N,N-二甲基苯胺(分子量为121)和
的N,N-二甲基苯胺(分子量为121)和 冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌
冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌 ,此时溶液为深红色。在搅拌下,慢慢加入
,此时溶液为深红色。在搅拌下,慢慢加入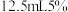 氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约
氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约 。
。③将粗产品用0.4%的氢氧化钠水溶液进行重结晶,得到橙黄色明亮的小叶片状晶体。

根据上述实验原理,下列说法错误的是
| A.实验中得到的N,N-二甲基苯胺需要在蒸馏后才能使用 |
| B.使用乙醚洗涤的目的是为了除去产物中残留的乙醇和水 |
| C.重结晶操作时需要加入过量水使甲基橙溶解 |
| D.N,N-二甲基苯胺的蒸馏应当在通风橱中进行 |
您最近一年使用:0次
2024-02-19更新
|
480次组卷
|
2卷引用:浙江省宁波市镇海中学2023-2024学年高三上学期新高考调研卷化学试题
名校
解题方法
4 . 我国科学家屠呦呦因成功提取青蒿素而获得2015年诺贝尔生理学或医学奖。研究发现青蒿素分子中的某结构在提取过程中对热不稳定,青蒿素分子结构和双氢青蒿素分子结构如图所示,下列说法不正确的是

| A.双氢青蒿素比青蒿素水溶性好,且青蒿素碱性条件下不稳定 |
| B.根据结构分析青蒿素能与碘化钠作用生成碘单质 |
| C.可采用低温、乙醇冷浸等方法,萃取出青蒿素 |
| D.青蒿素分子中所有碳原子不可能处于同一平面上 |
您最近一年使用:0次
5 . 下列说法正确的是
A.碳的非金属性大于硅,可发生 |
| B.碘单质易溶于乙醇,可用乙醇作碘水的萃取剂 |
| C.常温下铁与浓硝酸不反应,可用铁容器盛装浓硝酸 |
| D.苯甲酸和氯化钠溶解度随温度变化趋势不同,可用冷却结晶法提纯含有少量氯化钠的苯甲酸 |
您最近一年使用:0次
6 . 某研究小组制备纳米ZnO,再与金属有机框架MOF)材料复合制备荧光材ZnO@MOF,流程如下:
①含锌组分间的转化关系:
② 是
是 的一种晶型,39℃以下稳定。
的一种晶型,39℃以下稳定。
下列有关说法正确的是

①含锌组分间的转化关系:

②
 是
是 的一种晶型,39℃以下稳定。
的一种晶型,39℃以下稳定。下列有关说法正确的是
| A.纳米ZnO属于胶体 |
B.步骤Ⅰ,为提高产率应将过量NaOH溶液滴入 溶液制备 溶液制备 |
| C.步骤Ⅱ,为了更好地除去杂质,可用50℃的热水洗涤 |
D.用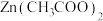 和过量 和过量 反应,得到的沉淀无需洗涤可直接控温煅烧得纳米ZnO 反应,得到的沉淀无需洗涤可直接控温煅烧得纳米ZnO |
您最近一年使用:0次
名校
解题方法
7 . 硼氢化钠 是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析
是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析 纯度的步骤如下。
纯度的步骤如下。
Ⅰ. 的制备
的制备
利用如图甲装置(加热及夹持装置略)进行操作: ,鼓入
,鼓入 ,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;
,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;
(ⅱ)升温到200℃,关闭 ,打开
,打开 通入
通入 ,充分反应后制得
,充分反应后制得 ;
;
(ⅲ)升温到240℃,持续搅拌下通入 ,打开
,打开 滴入硼酸三甲酯[分子式为
滴入硼酸三甲酯[分子式为 ];
];
(ⅳ)降温后,分离得到 和
和 的固体混合物。
的固体混合物。
已知:
 :可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在
:可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在
 :难溶于异丙胺
:难溶于异丙胺
异丙胺:有机溶剂,沸点:33℃
Ⅱ. 的提纯
的提纯
 可采用索氏提取法提纯,其装置如图乙所示,实验时将
可采用索氏提取法提纯,其装置如图乙所示,实验时将 和
和 的固体混合物放入滤纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回烧瓶,从而实现连续萃取。
的固体混合物放入滤纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回烧瓶,从而实现连续萃取。
步骤1:取m g产品(杂质不参加反应)溶于 溶液后配成
溶液后配成 溶液,取
溶液,取 置于碘量瓶中,加入
置于碘量瓶中,加入 的
的 溶液充分反应。(
溶液充分反应。( )
)
步骤2:向步骤1反应后溶液中加入过量的KI溶液,用稀硫酸调节pH,使过量 转化为
转化为 ,冷却后于暗处放数分钟。
,冷却后于暗处放数分钟。
步骤3:将步骤2所得混合液调pH约为5.0,加入几滴淀粉,用 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液 。(
。( )
)
回答下列问题:
(1)仪器a的名称是__________ 。
(2)写出 与
与 反应的化学方程式
反应的化学方程式__________ 。
(3)下列有关说法不正确的是__________。
(4)按照先后顺序对本实验的滴定操作排序
检查是否漏水→蒸馏水洗涤→__________ →__________→a→__________→__________→__________。
a.加液至“0”刻度以上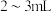 处
处
b.调整液面至“0”刻度或“0”刻度下方,记录读数
c.倾斜转动滴定管,使标准液润湿滴定管内壁,将润洗液从下口排出
d.赶出尖嘴部分气泡
e.向碱式滴定管中加 标准液
标准液
f.向酸式滴定管中加 标准液
标准液
g.左手控制活塞(或挤压玻璃珠),右手振荡锥形瓶
h.左手振荡锥形瓶,右手控制活塞(或挤压玻璃珠)
(5)产品中 的纯度为
的纯度为__________ %。
 是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析
是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析 纯度的步骤如下。
纯度的步骤如下。Ⅰ.
 的制备
的制备利用如图甲装置(加热及夹持装置略)进行操作:
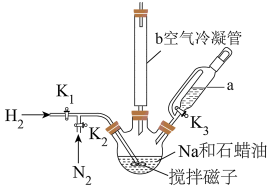
 ,鼓入
,鼓入 ,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;
,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;(ⅱ)升温到200℃,关闭
 ,打开
,打开 通入
通入 ,充分反应后制得
,充分反应后制得 ;
;(ⅲ)升温到240℃,持续搅拌下通入
 ,打开
,打开 滴入硼酸三甲酯[分子式为
滴入硼酸三甲酯[分子式为 ];
];(ⅳ)降温后,分离得到
 和
和 的固体混合物。
的固体混合物。已知:
 :可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在
:可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在 :难溶于异丙胺
:难溶于异丙胺异丙胺:有机溶剂,沸点:33℃
Ⅱ.
 的提纯
的提纯 可采用索氏提取法提纯,其装置如图乙所示,实验时将
可采用索氏提取法提纯,其装置如图乙所示,实验时将 和
和 的固体混合物放入滤纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回烧瓶,从而实现连续萃取。
的固体混合物放入滤纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回烧瓶,从而实现连续萃取。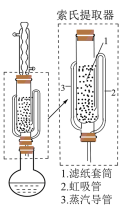
步骤1:取m g产品(杂质不参加反应)溶于
 溶液后配成
溶液后配成 溶液,取
溶液,取 置于碘量瓶中,加入
置于碘量瓶中,加入 的
的 溶液充分反应。(
溶液充分反应。( )
)步骤2:向步骤1反应后溶液中加入过量的KI溶液,用稀硫酸调节pH,使过量
 转化为
转化为 ,冷却后于暗处放数分钟。
,冷却后于暗处放数分钟。步骤3:将步骤2所得混合液调pH约为5.0,加入几滴淀粉,用
 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液 。(
。( )
)回答下列问题:
(1)仪器a的名称是
(2)写出
 与
与 反应的化学方程式
反应的化学方程式(3)下列有关说法不正确的是__________。
A. 和 和 中氢化合价相同 中氢化合价相同 | B.装置甲应该处于无水、无氧的反应环境 |
| C.装置乙中异丙胺蒸汽沿导管2上升 | D.萃取完全后, 在圆底烧瓶中 在圆底烧瓶中 |
(4)按照先后顺序对本实验的滴定操作排序
检查是否漏水→蒸馏水洗涤→
a.加液至“0”刻度以上
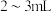 处
处b.调整液面至“0”刻度或“0”刻度下方,记录读数

c.倾斜转动滴定管,使标准液润湿滴定管内壁,将润洗液从下口排出
d.赶出尖嘴部分气泡
e.向碱式滴定管中加
 标准液
标准液f.向酸式滴定管中加
 标准液
标准液g.左手控制活塞(或挤压玻璃珠),右手振荡锥形瓶
h.左手振荡锥形瓶,右手控制活塞(或挤压玻璃珠)
(5)产品中
 的纯度为
的纯度为
您最近一年使用:0次
解题方法
8 . 纳米 被广泛的用于结构陶瓷、催化材料、光、电、磁和热等功能材料。某兴趣小组利用废弃的含有
被广泛的用于结构陶瓷、催化材料、光、电、磁和热等功能材料。某兴趣小组利用废弃的含有 的
的 溶液制备纳米
溶液制备纳米 :
:

已知:在较高的盐酸浓度下, 与
与 、乙醚形成化合物而溶于乙醚,当盐酸浓度降低时,化合物解离。请回答:
、乙醚形成化合物而溶于乙醚,当盐酸浓度降低时,化合物解离。请回答:
(1)操作B的名称是______ ,试剂X为______ 。
(2)步骤Ⅳ中发生反应的离子方程式为______ 。
(3)下列有关萃取和分液的说法正确______ 。

A.进行操作A时,溶液中加入乙醚后转移至分液漏斗中,塞上玻璃塞,如图振荡
B.振荡几次后需打开分液漏斗上口玻璃塞放气
C.一次萃取后若在水相检测到 ,需加入乙醚再次萃取
,需加入乙醚再次萃取
D.为了加快反应速率,Ⅳ应将 溶液一次性加入溶液Ⅱ中,有利于
溶液一次性加入溶液Ⅱ中,有利于 沉淀的生成
沉淀的生成
E.分液漏斗中液体的总体积不超过其容量的
(4)市售PAC是由 水解产生的一系列中间产物脱水聚合而成,其中稳定存在形态为聚十三铝
水解产生的一系列中间产物脱水聚合而成,其中稳定存在形态为聚十三铝 ,简称
,简称 。
。 含量的高低直接影响PAC的净水效能。向
含量的高低直接影响PAC的净水效能。向 溶液中缓慢滴加一定量
溶液中缓慢滴加一定量 溶液,若只生成
溶液,若只生成 ,则理论上
,则理论上
_______ 。
(5)为了发挥PAC净水的最佳效能,一般要将水的 调节在
调节在 。若在强酸或强碱环境下使用PAC,净水效果不佳,结合铝元素的存在形式分析原因
。若在强酸或强碱环境下使用PAC,净水效果不佳,结合铝元素的存在形式分析原因_______ 。
 被广泛的用于结构陶瓷、催化材料、光、电、磁和热等功能材料。某兴趣小组利用废弃的含有
被广泛的用于结构陶瓷、催化材料、光、电、磁和热等功能材料。某兴趣小组利用废弃的含有 的
的 溶液制备纳米
溶液制备纳米 :
:
已知:在较高的盐酸浓度下,
 与
与 、乙醚形成化合物而溶于乙醚,当盐酸浓度降低时,化合物解离。请回答:
、乙醚形成化合物而溶于乙醚,当盐酸浓度降低时,化合物解离。请回答:(1)操作B的名称是
(2)步骤Ⅳ中发生反应的离子方程式为
(3)下列有关萃取和分液的说法正确

A.进行操作A时,溶液中加入乙醚后转移至分液漏斗中,塞上玻璃塞,如图振荡
B.振荡几次后需打开分液漏斗上口玻璃塞放气
C.一次萃取后若在水相检测到
 ,需加入乙醚再次萃取
,需加入乙醚再次萃取D.为了加快反应速率,Ⅳ应将
 溶液一次性加入溶液Ⅱ中,有利于
溶液一次性加入溶液Ⅱ中,有利于 沉淀的生成
沉淀的生成E.分液漏斗中液体的总体积不超过其容量的

(4)市售PAC是由
 水解产生的一系列中间产物脱水聚合而成,其中稳定存在形态为聚十三铝
水解产生的一系列中间产物脱水聚合而成,其中稳定存在形态为聚十三铝 ,简称
,简称 。
。 含量的高低直接影响PAC的净水效能。向
含量的高低直接影响PAC的净水效能。向 溶液中缓慢滴加一定量
溶液中缓慢滴加一定量 溶液,若只生成
溶液,若只生成 ,则理论上
,则理论上
(5)为了发挥PAC净水的最佳效能,一般要将水的
 调节在
调节在 。若在强酸或强碱环境下使用PAC,净水效果不佳,结合铝元素的存在形式分析原因
。若在强酸或强碱环境下使用PAC,净水效果不佳,结合铝元素的存在形式分析原因
您最近一年使用:0次
解题方法
9 . 工业制备茉莉醛( )的流程如图所示。下列说法正确的是
)的流程如图所示。下列说法正确的是
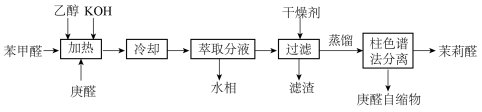
| A.乙醇只作溶剂,苯甲醛和庚醛直接混合后保温反应 |
| B.萃取分液过程中需酸洗、水洗,干燥剂可选用浓硫酸 |
| C.可将最后两步“分馏”和“柱色谱分离”合并为“真空减压分馏” |
| D.可采用质谱法测定茉莉醛部分结构信息 |
您最近一年使用:0次
名校
10 . 下列玻璃仪器在相应实验中选用合理的是
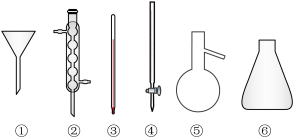
| A.重结晶法提纯苯甲酸:①②③ |
B.蒸馏法分离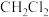 和 和 :②③⑤⑥ :②③⑤⑥ |
| C.浓硫酸催化乙醇制备乙烯:③⑤ |
D. 滴定待测液中 滴定待测液中 的含量:④⑥ 的含量:④⑥ |
您最近一年使用:0次
2023-12-24更新
|
556次组卷
|
4卷引用:浙江省三校2023-2024学年高三上学期联考选考模拟化学试题
浙江省三校2023-2024学年高三上学期联考选考模拟化学试题(已下线)专题03 化学实验基础(3大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)重庆市第八中学校2024届高三下学期强化考试(一模)化学试卷(已下线)压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)



