名校
解题方法
1 . 为完成下列相关实验,所选玻璃仪器和试剂均准确、完整的是(不考虑试剂存放容器)
| 实验目的 | 玻璃仪器 | 试剂 | |
| A | 配制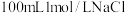 溶液 溶液 |  容量瓶、烧杯、量筒、玻璃棒 容量瓶、烧杯、量筒、玻璃棒 | 蒸馏水、 固体 固体 |
| B | 制备 胶体 胶体 | 烧杯、酒精灯、胶头滴管 | 蒸馏水、饱和 溶液 溶液 |
| C | 测定 待测液测定 待测液测定 待测液 待测液 | 烧杯、锥形瓶、胶头滴管、酸式滴定管 | 待测 溶液、盐酸标准液、紫色石蕊试液 溶液、盐酸标准液、紫色石蕊试液 |
| D | 实验室制氯气 | 分液漏斗、圆底烧瓶、导气管、洗气瓶(多个)、集气瓶 | 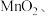 浓盐酸、掖、浓硫酸溶液、浓硫酸 浓盐酸、掖、浓硫酸溶液、浓硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 草酸钠( )常用作还原剂。已知常温下,草酸的电离常数
)常用作还原剂。已知常温下,草酸的电离常数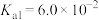 ,
,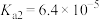 ,碳酸的电离常数
,碳酸的电离常数 ,
, 。回答下列问题:
。回答下列问题:
(1) 发生第一步水解的离子方程式为
发生第一步水解的离子方程式为___________ 。
(2)相同条件下,同浓度的① ,②
,② ,③
,③ ,④
,④ 四种溶液的pH由大到小的顺序为
四种溶液的pH由大到小的顺序为___________ (用编号表示)。
(3)将等浓度、等体积的 溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是
溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是___________ 。
a.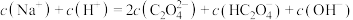
b.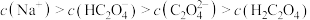
c.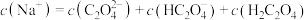
d.
(4) 溶液常用作氧化还原滴定的标准液。实验室欲配制250mL0.10mol⋅L-1的
溶液常用作氧化还原滴定的标准液。实验室欲配制250mL0.10mol⋅L-1的 溶液。
溶液。
①需称取 固体
固体___________ g。
②配制溶液时,需要的玻璃仪器除烧杯、玻璃棒、量筒外还应有___________ 。
(5)用 标准液测定某高锰酸钾样品的纯度:
标准液测定某高锰酸钾样品的纯度:
步骤I:称取2.0g高锰酸钾样品,配成100mL溶液,取20mL溶液于锥形瓶中,并加入少量硫酸酸化。
步骤Ⅱ:用(4)中配制的 标准液进行滴定,平行滴定三次,记录消耗
标准液进行滴定,平行滴定三次,记录消耗 溶液的体积如下表:
溶液的体积如下表:
①滴定终点判断的依据是___________ 。
②平均消耗 溶液的体积为
溶液的体积为_________ mL,样品中 的质量分数为
的质量分数为_________ 。
③若(4)中称取的 固体已部分吸水潮解,会使测得的样品中
固体已部分吸水潮解,会使测得的样品中 的质量分数
的质量分数_________ (填“偏高”、“偏低”或“不变”)。
 )常用作还原剂。已知常温下,草酸的电离常数
)常用作还原剂。已知常温下,草酸的电离常数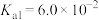 ,
,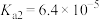 ,碳酸的电离常数
,碳酸的电离常数 ,
, 。回答下列问题:
。回答下列问题:(1)
 发生第一步水解的离子方程式为
发生第一步水解的离子方程式为(2)相同条件下,同浓度的①
 ,②
,② ,③
,③ ,④
,④ 四种溶液的pH由大到小的顺序为
四种溶液的pH由大到小的顺序为(3)将等浓度、等体积的
 溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是
溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是a.
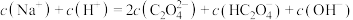
b.
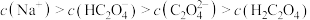
c.
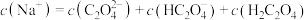
d.

(4)
 溶液常用作氧化还原滴定的标准液。实验室欲配制250mL0.10mol⋅L-1的
溶液常用作氧化还原滴定的标准液。实验室欲配制250mL0.10mol⋅L-1的 溶液。
溶液。①需称取
 固体
固体②配制溶液时,需要的玻璃仪器除烧杯、玻璃棒、量筒外还应有
(5)用
 标准液测定某高锰酸钾样品的纯度:
标准液测定某高锰酸钾样品的纯度:步骤I:称取2.0g高锰酸钾样品,配成100mL溶液,取20mL溶液于锥形瓶中,并加入少量硫酸酸化。
步骤Ⅱ:用(4)中配制的
 标准液进行滴定,平行滴定三次,记录消耗
标准液进行滴定,平行滴定三次,记录消耗 溶液的体积如下表:
溶液的体积如下表:| 第1次 | 第2次 | 第3次 | |
消耗 溶液的体积/mL 溶液的体积/mL | 49.80 | 46.75 | 50.20 |
②平均消耗
 溶液的体积为
溶液的体积为 的质量分数为
的质量分数为③若(4)中称取的
 固体已部分吸水潮解,会使测得的样品中
固体已部分吸水潮解,会使测得的样品中 的质量分数
的质量分数
您最近一年使用:0次
解题方法
3 . 某实验小组用0.50 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。
(一)配制0.50 NaOH溶液。
NaOH溶液。
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体_______ g。
(2)从下图中选择称量NaOH固体所需要的仪器_______ (填字母)。
(二)测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示。
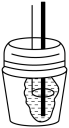
(3)写出该反应的热化学方程式(中和热 ):
):_______ 。
(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
①请填写表中的空白:
②近似认为0.50 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液的密度都是1
硫酸溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容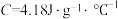 。则测得中和热
。则测得中和热 =
=_______  (取小数点后一位)。
(取小数点后一位)。
③上述实验数值结果与57.3 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是_______ (填字母)。
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
C.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
溶液的温度
 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。(一)配制0.50
 NaOH溶液。
NaOH溶液。(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体
(2)从下图中选择称量NaOH固体所需要的仪器
| 序号 | a | b | c | d | e | f |
| 仪器 | 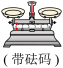 |  |  |  |  |  |
(二)测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示。

(3)写出该反应的热化学方程式(中和热
 ):
):(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
①请填写表中的空白:
| 实验次数 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温度差平均值 (  - - )/℃ )/℃ | ||
 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液的密度都是1
硫酸溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容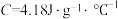 。则测得中和热
。则测得中和热 =
= (取小数点后一位)。
(取小数点后一位)。③上述实验数值结果与57.3
 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
C.用温度计测定NaOH溶液起始温度后直接测定
 溶液的温度
溶液的温度
您最近一年使用:0次
2022-12-31更新
|
209次组卷
|
3卷引用:河南省鹤壁市第一中学2022-2023学年高二上学期期末检测化学试题
解题方法
4 . 某化学兴趣小组利用0.2000 mol∙L 的
的 溶液测定某NaCl、KCl混合溶液中
溶液测定某NaCl、KCl混合溶液中 的物质的量浓度。已知25℃时,以下五种物质的
的物质的量浓度。已知25℃时,以下五种物质的 如下表所示:
如下表所示:
(1)配制250 mL 0.2000 mol∙L 的
的 溶液所需的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还需要
溶液所需的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还需要_________ (填仪器名称),需用托盘天平称取固体硝酸银的质量为______ g。
(2)取一定体积的待测液于锥形瓶中,滴加几滴_______(填字母)溶液作指示剂。
(3)用_____________ (填仪器名称)盛装标准 溶液进行滴定,滴定终点的实验现象为
溶液进行滴定,滴定终点的实验现象为_______ 。
(4)实验数据记录如下表所示:
则该待测液中, 的物质的量浓度为
的物质的量浓度为_______ mol/L(保留四位有效数字)。
(5)下列操作中可导致测定的 浓度偏低的是_______(填字母)。
浓度偏低的是_______(填字母)。
 的
的 溶液测定某NaCl、KCl混合溶液中
溶液测定某NaCl、KCl混合溶液中 的物质的量浓度。已知25℃时,以下五种物质的
的物质的量浓度。已知25℃时,以下五种物质的 如下表所示:
如下表所示:| 物质 | AgCl | AgSCN |  | AgBr | AgI |
 |  | 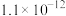 | 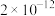 |  | 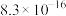 |
| 颜色 | 白色 | 白色 | 砖红色 | 淡黄色 | 黄色 |
 的
的 溶液所需的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还需要
溶液所需的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还需要(2)取一定体积的待测液于锥形瓶中,滴加几滴_______(填字母)溶液作指示剂。
| A.KSCN | B. | C.KBr | D.KI |
 溶液进行滴定,滴定终点的实验现象为
溶液进行滴定,滴定终点的实验现象为(4)实验数据记录如下表所示:
| 滴定次数 | 待测溶液体积/mL | 标准 溶液体积 溶液体积 | |
| 滴定前的刻度/mL | 滴定后的刻度/mL | ||
| 第一次 | 50.00 | 0.00 | 25.05 |
| 第二次 | 50.00 | 4.10 | 29.10 |
| 第三次 | 50.00 | 0.40 | 25.35 |
 的物质的量浓度为
的物质的量浓度为(5)下列操作中可导致测定的
 浓度偏低的是_______(填字母)。
浓度偏低的是_______(填字母)。A.盛装标准 溶液的滴定管,未经润洗就直接注入溶液进行实验 溶液的滴定管,未经润洗就直接注入溶液进行实验 |
| B.盛装标准液的滴定管在滴定前有气泡,滴定后气泡消失 |
C.读取 溶液体积时,开始时仰视读数,滴定结束时俯视读数 溶液体积时,开始时仰视读数,滴定结束时俯视读数 |
| D.锥形瓶内有少量蒸馏水 |
您最近一年使用:0次
2022-12-29更新
|
393次组卷
|
2卷引用:辽宁省大连市2022-2023学年高二上学期期末考试化学试题
解题方法
5 . 配制500 mL 1mol / L 的硫酸铜溶液,用托盘天平称取胆矾8.0克,会导致所配溶液浓度偏大。_______
您最近一年使用:0次
名校
6 . 根据题目要求,回答以下相关问题。
(1)配制240mL1.0mol/LNaOH标准溶液。步骤如下:1.0mol/LNaOH标准溶液配制:称取_______ gNaOH固体,用蒸馏水在烧杯中溶解,冷却至室温后,转移至_______ 中,洗涤烧杯和玻璃棒2~3次,也转移到容器中,最后进行定容。若定容时俯视刻度线,则所配溶液的浓度_______ ;若定容时平视刻度线(使凹液面最低处与刻度线相平),盖好瓶塞,倒转摇匀,发现液面有所下降,则所配溶液的浓度_______ (填偏大、偏小或不变)。
(2)聚合硫酸铁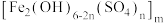 广泛用于水的净化。以
广泛用于水的净化。以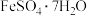 为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
①将一定量的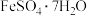 溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的
溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的 溶液,继续反应一段时间,得到红棕色黏稠液体。
溶液,继续反应一段时间,得到红棕色黏稠液体。 氧化
氧化 的离子方程式为
的离子方程式为_______ ;水解聚合反应会导致溶液的pH_______ 。
②测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的 溶液(
溶液( 将
将 还原为
还原为 ),充分反应后,除去过量的
),充分反应后,除去过量的 。用
。用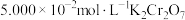 溶液滴定至终点(滴定过程中
溶液滴定至终点(滴定过程中 与
与 反应生成
反应生成 和
和 ),消耗
),消耗 溶液20.00mL。上述实验中若不除去过量的
溶液20.00mL。上述实验中若不除去过量的 ,样品中铁元素的质量分数的测定结果将
,样品中铁元素的质量分数的测定结果将_______ (填“偏大”或“偏小”或“无影响”);该样品中铁元素的质量分数为_______ 。
(1)配制240mL1.0mol/LNaOH标准溶液。步骤如下:1.0mol/LNaOH标准溶液配制:称取
(2)聚合硫酸铁
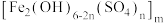 广泛用于水的净化。以
广泛用于水的净化。以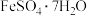 为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。①将一定量的
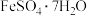 溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的
溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的 溶液,继续反应一段时间,得到红棕色黏稠液体。
溶液,继续反应一段时间,得到红棕色黏稠液体。 氧化
氧化 的离子方程式为
的离子方程式为②测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的
 溶液(
溶液( 将
将 还原为
还原为 ),充分反应后,除去过量的
),充分反应后,除去过量的 。用
。用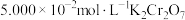 溶液滴定至终点(滴定过程中
溶液滴定至终点(滴定过程中 与
与 反应生成
反应生成 和
和 ),消耗
),消耗 溶液20.00mL。上述实验中若不除去过量的
溶液20.00mL。上述实验中若不除去过量的 ,样品中铁元素的质量分数的测定结果将
,样品中铁元素的质量分数的测定结果将
您最近一年使用:0次
名校
解题方法
7 . 下图是某同学用500mL容量瓶配制 NaOH溶液的过程:
NaOH溶液的过程:
 NaOH溶液的过程:
NaOH溶液的过程:
| A.如图所示,用托盘直接称量2.0g烧碱 |
| B.配制的正确顺序为①④③⑤②⑥ |
| C.②中定容时仰视刻线会导致溶液浓度偏高 |
| D.能用容量瓶贮存配制好的溶液 |
您最近一年使用:0次
2022-07-07更新
|
2444次组卷
|
16卷引用:四川省成都市2021-2022学年高二下学期摸底考试化学试题
四川省成都市2021-2022学年高二下学期摸底考试化学试题山东省淄博市临淄中学2022-2023学年高一上学期期末考试化学试题湖南省长沙市实验中学2022-2023学年高一上学期期末考试化学试题陕西省宝鸡市渭滨区2022-2023学年高一年级上学期期末考试化学试题四川省成都经济技术开发区实验中学校2022-2023学年高二下学期5月月考化学试题内蒙古巴彦淖尔市第一中学2022-2023学年高一上学期1月期末考试化学试题(已下线)第13讲 物质的量浓度-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )河南省宋基信阳实验中学2022-2023学年高三上学期9月月考化学试题(已下线)海水中的重要元素—钠和氯——课时7物质的量浓度天津市天津中学2022-2023学年高一上学期期中考试化学试题内蒙古乌兰浩特第一中学2022-2023学年高一上学期第三次月考化学试题广东省揭阳市惠来县第一中学2022-2023学年高一下学期第一次月考化学试题福建省厦门第一中学2023-2024学年高一上学期12月月考化学试题福建省厦门第一中学2023-2024学年高一上学期第二次月考化学试卷云南师范大学附属中学2023-2024学年高一下学期第一次月考化学试题福建省厦门大学附属实验中学2023—2024学年高一上学期第二次月考化学试卷
8 . 准确称取1.00 g不纯的苛性钠样品(主要成分NaOH)配成250 mL溶液,取出10.00mL,用已知浓度为0.040 mol·L-l的盐酸进行滴定(杂质不与盐酸反应),达到滴定终点时共消耗盐酸20.00mL。
(1)本实验称取苛性钠时,能否用托盘天平?___________ (填写“能”或“否”)。
(2)① 配制上述溶液,定容时俯视刻度线,所配得溶液的浓度___________ (填“偏高”、“偏低”或“无影响”)。
②取用10.00mL苛性钠溶液所用的仪器名称是___________ 。
(3)操作过程中,用蒸馏水洗净酸式滴定管后,未用盐酸润洗酸式滴定管,会使滴定结果___________ (填“偏高”或“偏低”)。
(4)①本实验如果用酚酞为指示剂,滴定终点的操作和现象是______ 。
②滴定过程中,眼睛应注视___________ 。
(5)根据滴定结果,求得该样品中苛性钠的质量分数为_______ 。
(6)滴定前,盛装盐酸的滴定管尖嘴有气泡,滴定后气泡消失,会使滴定结果_______ (填“偏高”或“偏低”)。
(1)本实验称取苛性钠时,能否用托盘天平?
(2)① 配制上述溶液,定容时俯视刻度线,所配得溶液的浓度
②取用10.00mL苛性钠溶液所用的仪器名称是
(3)操作过程中,用蒸馏水洗净酸式滴定管后,未用盐酸润洗酸式滴定管,会使滴定结果
(4)①本实验如果用酚酞为指示剂,滴定终点的操作和现象是
②滴定过程中,眼睛应注视
(5)根据滴定结果,求得该样品中苛性钠的质量分数为
(6)滴定前,盛装盐酸的滴定管尖嘴有气泡,滴定后气泡消失,会使滴定结果
您最近一年使用:0次
名校
9 . 在疫情防控中,常使用次氯酸钠溶液对环境消毒。已知某“84消毒液”瓶体部分标签如图所示。请回答下列问题:
(1)该“84消毒液”的物质的量浓度为_______ 。
(2)小明某次实验需要NaClO溶液95mL,配制该浓度的“84消毒液”时,小明需用托盘天平称量该固体的质量为_______ g。
(3)配制过程中需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、_______ 。
(4)以下有关配制该溶液的说法正确的是_______(填字母)。
(5)下列情况会导致所配制的“84消毒液”的物质的量浓度偏高的是_______(填字母)。
| 84消毒液 【有效成分】NaClO 【规格】1000mL 【质量分数】12% 【密度】 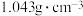 |
(2)小明某次实验需要NaClO溶液95mL,配制该浓度的“84消毒液”时,小明需用托盘天平称量该固体的质量为
(3)配制过程中需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
(4)以下有关配制该溶液的说法正确的是_______(填字母)。
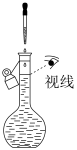 | 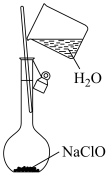 | 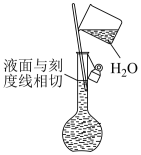 |
| ① | ② | ③ |
| A.定容时的操作如图①所示 |
| B.溶解NaClO固体不能用如图②所示的操作 |
| C.定容操作可以用图③表示 |
| D.定容过程向容量瓶加蒸馏水至接近刻度线1—2cm时,改胶头滴管滴加蒸馏水至刻度线 |
| A.容量瓶用蒸馏水洗后未干燥 | B.配制过程中未洗涤烧杯和玻璃棒 |
| C.定容时俯视刻度线 | D.称量NaClO固体时所用的砝码生锈了 |
您最近一年使用:0次
10 . 某学生欲配制1000mL6.0mol·L-1的H2SO4,实验室有三种不同浓度的硫酸:
①480mL0.5mol·L-1的硫酸;②150mL25%的硫酸(ρ=1.18g·mL-1);③足量的18mol·L-1的硫酸。有三种规格的容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为___ mol·L-1(保留1位小数)。
(2)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol·L-1的浓硫酸___ mL,沿玻璃棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.___ ;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(3)进行操作C前还需注意___ 。
(4)如果省略操作D,对所配溶液浓度有何影响?___ (填“偏大”、“偏小”或“无影响”)。
①480mL0.5mol·L-1的硫酸;②150mL25%的硫酸(ρ=1.18g·mL-1);③足量的18mol·L-1的硫酸。有三种规格的容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为
(2)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol·L-1的浓硫酸
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(3)进行操作C前还需注意
(4)如果省略操作D,对所配溶液浓度有何影响?
您最近一年使用:0次



