名校
1 . 高锰酸钾生产过程中产生的废锰渣(主要成分为 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
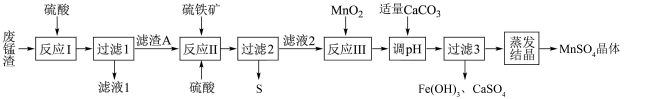
已知:硫铁矿的主要成分为二硫化亚铁( ,杂质不参与反应)。
,杂质不参与反应)。
回答下列问题:
(1)二硫化亚铁中S元素的化合价为_______ 。
(2)①滤渣A的主要成分是_______ (填化学式);
②“反应II”生成 、
、 等物质的离子方程式为
等物质的离子方程式为_______ 。
③“反应III”中还原剂和氧化剂物质的量之比为_______ ;
④“调 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为_______ 。
 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
已知:硫铁矿的主要成分为二硫化亚铁(
 ,杂质不参与反应)。
,杂质不参与反应)。回答下列问题:
(1)二硫化亚铁中S元素的化合价为
(2)①滤渣A的主要成分是
②“反应II”生成
 、
、 等物质的离子方程式为
等物质的离子方程式为③“反应III”中还原剂和氧化剂物质的量之比为
④“调
 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为
您最近一年使用:0次
名校
2 . 化工产品中,含氯物质众多,其用途广泛。回答下列问题:
(1)如图为氯及其化合物的“价-类”二维图。缺失的物质B为_______ (填化学式)。

(2)次氯酸钠是一种含氯物质,取含次氯酸钠14.9g/L的“84”消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为_______ mol/L。
(3)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知:Ca(ClO3)2易溶于水。
①“一系列操作”为_______ 、_______ 。
②“转化”发生反应的离子方程式为_______ 。
(1)如图为氯及其化合物的“价-类”二维图。缺失的物质B为

(2)次氯酸钠是一种含氯物质,取含次氯酸钠14.9g/L的“84”消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
(3)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知:Ca(ClO3)2易溶于水。
①“一系列操作”为
②“转化”发生反应的离子方程式为
您最近一年使用:0次
名校
3 . 废旧金属的综合利用有利于节约资源、保护环境。现有废弃物(含 、FeO、CuO),实验室要回收三种金属,工艺流程如图所示:
、FeO、CuO),实验室要回收三种金属,工艺流程如图所示:

已知: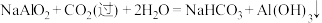
回答下列问题:
(1)“碱溶”时发生反应的离子方程式为_______ 。
(2)“操作1”用到的玻璃仪器有_______ 、玻璃棒。
(3)“沉铝”时加入适量盐酸,该步骤为避免因盐酸控制不当(过量)而导致 溶解,实际操作中可用过量
溶解,实际操作中可用过量_______ (填化学式)气体代替。
(4)“沉铁”时通入空气的目的是_____ ;证明“沉铁”的溶液中没有 的操作为
的操作为_______ 。
(5)“灼烧”时可在_______ (填仪器名称)中进行,写出该反应的化学方程式:_______ 。
 、FeO、CuO),实验室要回收三种金属,工艺流程如图所示:
、FeO、CuO),实验室要回收三种金属,工艺流程如图所示:
已知:
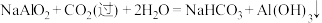
回答下列问题:
(1)“碱溶”时发生反应的离子方程式为
(2)“操作1”用到的玻璃仪器有
(3)“沉铝”时加入适量盐酸,该步骤为避免因盐酸控制不当(过量)而导致
 溶解,实际操作中可用过量
溶解,实际操作中可用过量(4)“沉铁”时通入空气的目的是
 的操作为
的操作为(5)“灼烧”时可在
您最近一年使用:0次
2023-03-06更新
|
241次组卷
|
2卷引用:内蒙古乌兰浩特市第四中学2022-2023学年高一下学期开学考试化学试题
解题方法
4 . 氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如图:

(1)“滤液1”中的离子除Na+、SO 外,还存在较多的离子是
外,还存在较多的离子是___ (写一种离子符号)。
(2)“反应”中发生的化学变化是2CuCl2+Na2SO3═2CuCl↓+2NaCl+SO3,其中属于氧化物的是___ 。
(3)“操作a”的名称是___ 。本流程中可以循环利用的物质(水除外)是___ (写化学式)。
(4)CuCl粗品先“水洗”再“醇洗”,“醇洗”的目的是___ 。

(1)“滤液1”中的离子除Na+、SO
 外,还存在较多的离子是
外,还存在较多的离子是(2)“反应”中发生的化学变化是2CuCl2+Na2SO3═2CuCl↓+2NaCl+SO3,其中属于氧化物的是
(3)“操作a”的名称是
(4)CuCl粗品先“水洗”再“醇洗”,“醇洗”的目的是
您最近一年使用:0次



