名校
解题方法
1 . 现有含有少NaCl、 、
、 等杂质的
等杂质的 溶液,选择适当的试剂除去杂质,得到纯净的
溶液,选择适当的试剂除去杂质,得到纯净的 固体,实验流程如下图所示。
固体,实验流程如下图所示。

(1)沉淀A的主要成分是___________ (填化学式)。
(2)③加入过量的Y的目的是___________ 。
(3)溶液3中肯定含有的杂质是___________ ,为除去杂质可向溶液3中加入过量的___________ 。
 、
、 等杂质的
等杂质的 溶液,选择适当的试剂除去杂质,得到纯净的
溶液,选择适当的试剂除去杂质,得到纯净的 固体,实验流程如下图所示。
固体,实验流程如下图所示。 
(1)沉淀A的主要成分是
(2)③加入过量的Y的目的是
(3)溶液3中肯定含有的杂质是
您最近一年使用:0次
解题方法
2 . 回答下列问题
(1)A、B、C、D为中学常见的混合物分离或提纯的基本装置,请回答:

①分离植物油和水,选择装置_______ (填序号),主要使用仪器名称_______ ;
②分离乙二醇和丙三醇的混合溶液,选择装置_______ (填序号)。
(2)实验室需配制250mL0.1mol·L-1的Na2CO3溶液,填空并回答下列问题:
①配制250mL0.1mol·L-1的Na2CO3溶液,实际应称取Na2CO3的质量是_______ g,实验过程中所需的玻璃仪器有玻璃棒、烧杯、胶头滴管和 _______ 。
②若在溶液配制过程中出现如下情况,对所配溶液浓度将有何影响(填“偏高”“偏低”或“无影响”),若容量瓶中有少量蒸馏水_______ ;若定容时俯视刻度线_______ 。
(3)Cl2通入一定浓度NaOH溶液后生成了三种含氯化合物,其中n(NaClO):n(NaClO3)=5:1,写出Cl2 与NaOH溶液反应的化学方程式:_______ 。
(1)A、B、C、D为中学常见的混合物分离或提纯的基本装置,请回答:

①分离植物油和水,选择装置
②分离乙二醇和丙三醇的混合溶液,选择装置
| 物质 | 熔点(℃) | 沸点(摄氏度) | 密度(g/cm-3) | 溶解性 |
| 乙二醇 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比例互溶 |
①配制250mL0.1mol·L-1的Na2CO3溶液,实际应称取Na2CO3的质量是
②若在溶液配制过程中出现如下情况,对所配溶液浓度将有何影响(填“偏高”“偏低”或“无影响”),若容量瓶中有少量蒸馏水
(3)Cl2通入一定浓度NaOH溶液后生成了三种含氯化合物,其中n(NaClO):n(NaClO3)=5:1,写出Cl2 与NaOH溶液反应的化学方程式:
您最近一年使用:0次
名校
3 . 某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:

普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)填写标号仪器的名称Ⅰ:__ 。
(2)操作②玻璃棒的作用是__ ;操作②中有一处明显错误请改正__ 。
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为__ (填化学式)。
(4)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为__ (填化学式)。
(5)该同学要对滤液的成分进行检验,以确认是否含有Cl-,下面是他做实验后所写的实验报告,请你写出其空白处的内容:

普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)填写标号仪器的名称Ⅰ:
(2)操作②玻璃棒的作用是
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为
(4)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为
(5)该同学要对滤液的成分进行检验,以确认是否含有Cl-,下面是他做实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 检验Cl- | 取少许滤液于试管中,加入 | 含有Cl- |
您最近一年使用:0次
名校
4 . 下列从混合物中分离出其中的一种成分,所采取的分离方法正确的是
| A.对含Ca2+、Mg2+的自来水,可采取沉淀法得到蒸馏水 |
| B.水和酒精的混合物,可用蒸馏的方法,使含水的酒精变为无水酒精 |
| C.要提取碘水中的碘,可用四氯化碳萃取后,分离出下层,再采用蒸馏法得到 |
| D.可用冷却结晶的方法从热的含少量KNO3的NaCl溶液中分离得到纯净的NaCl |
您最近一年使用:0次
5 . 草木灰主要成分是 K2CO3、KCl、K2SO4和不溶于水的杂质。实验小组为了制取 KCl晶体,设计了如下流程。以下说法错误的是
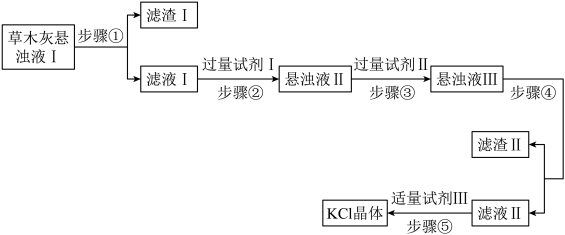

| A.步骤①中用到的玻璃仪器为:烧杯、漏斗、玻璃棒 |
| B.试剂Ⅰ是过量 Ba(NO3)2溶液除去 K2CO3、K2SO4 |
| C.适量试剂III是盐酸,除去过量试剂II |
| D.步骤⑤的方法是蒸发结晶 |
您最近一年使用:0次
2021-11-15更新
|
147次组卷
|
2卷引用:内蒙古喀喇沁旗锦山蒙古族中学2021-2022学年高一上学期第二次调研(期中)考试化学试题
名校
解题方法
6 . 为了将混有硫酸钠、碳酸氢铵的氯化钠提纯,某同学设计实验流程如下:

回答下列问题:
(1)操作①的目的是___________ 。操作②能否用硝酸钡溶液?___________ (填“能”或“不能”)。
(2)进行操作②后,如何判断 已除尽,方法是
已除尽,方法是___________ 。
(3)操作③中发生反应的化学方程式为___________ 。操作④的名称是___________ 。
(4)此设计方案是否严密?___________ (填“严密”或“不严密”),理由是___________ 。
(5)原固体样品中含NaCl m1g,最后得到的NaCl固体m2 g,则m1___________ m2(填“>”“<”或“=”)。

回答下列问题:
(1)操作①的目的是
(2)进行操作②后,如何判断
 已除尽,方法是
已除尽,方法是(3)操作③中发生反应的化学方程式为
(4)此设计方案是否严密?
(5)原固体样品中含NaCl m1g,最后得到的NaCl固体m2 g,则m1
您最近一年使用:0次
2021-05-20更新
|
183次组卷
|
6卷引用:内蒙古翁牛特旗乌丹第一中学2019-2020学年高一上学期期中考试化学试题
内蒙古翁牛特旗乌丹第一中学2019-2020学年高一上学期期中考试化学试题内蒙古赤峰学院附属中学2021-2022学年高一上学期期中考试化学试题辽宁省朝阳市建平县实验中学2020-2021学年高一下学期期中考试化学试题(已下线)第08讲 元素与物质的分类-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)湖北省巴东第三高级中学2021-2022学年高一下学期第一次月考化学试题湖南省攸县第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
7 . 除去粗盐中的杂质CaCl2、MgCl2和Na2SO4,过程如下:

下列有关说法正确的是

下列有关说法正确的是
| A.除去Mg2+的主要反应:MgCl2+2NaOH=Mg(OH)2↓+2NaCl |
| B.试剂①一定是Na2CO3溶液 |
C.检验 是否除净:取少量滤液,先加BaCl2溶液再加稀盐酸 是否除净:取少量滤液,先加BaCl2溶液再加稀盐酸 |
| D.滤液加稀盐酸时只发生反应:HCl+NaOH=H2O+NaCl |
您最近一年使用:0次
2021-03-25更新
|
98次组卷
|
2卷引用:内蒙古包头市第四中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
8 . Ⅰ.(1)我国的青海省有许多盐湖盛产食盐,人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用。粗盐中含Ca2+、Mg2+、 以及泥沙等杂质,为了除去可溶性杂质,有以下实验步骤进行提纯:
以及泥沙等杂质,为了除去可溶性杂质,有以下实验步骤进行提纯:
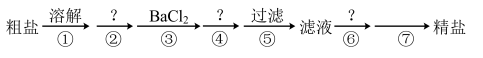
④步所加试剂是________ 。
(2)第⑥步发生反应的离子方程式为________________________ 、________________________ 。
(3)第⑦步的操作名称________ ,需要的玻璃仪器有________ 、________ 。
(4)通过步骤⑤中过滤后的滤液,检验 已除尽的操作方法是
已除尽的操作方法是________________________ 。
Ⅱ.(5)设阿伏加 德罗常数为NA,标准状况下,某O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积是________ L。
(6)用双线桥法标出下列反应的电子转移方向和数目________ 。2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
 以及泥沙等杂质,为了除去可溶性杂质,有以下实验步骤进行提纯:
以及泥沙等杂质,为了除去可溶性杂质,有以下实验步骤进行提纯: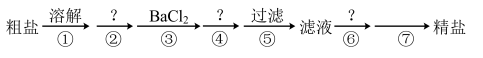
④步所加试剂是
(2)第⑥步发生反应的离子方程式为
(3)第⑦步的操作名称
(4)通过步骤⑤中过滤后的滤液,检验
 已除尽的操作方法是
已除尽的操作方法是Ⅱ.(5)设阿伏加 德罗常数为NA,标准状况下,某O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积是
(6)用双线桥法标出下列反应的电子转移方向和数目
您最近一年使用:0次
2020-07-23更新
|
61次组卷
|
2卷引用:内蒙古包头市回民中学2020-2021学年高一上学期期中考试化学试题
9 . 海水是宝贵的自然资源,从海水中可以提取多种化工原料,如图是某工厂对海水综合利用的示意图:
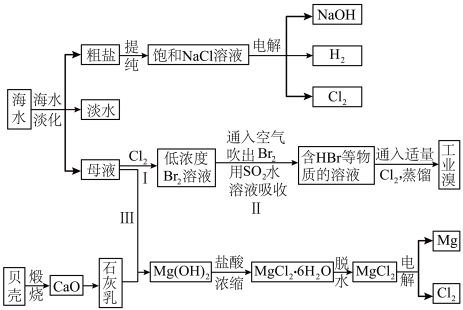
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。则加入试剂的先后顺序是________ (填编号)。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_____________ 。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式:_______________________ 。
(3)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入MgCl2溶液,充分搅拌后经________ (填操作方法)可得纯净的Mg(OH)2。
(4)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是________ (填字母)。
A.H2 B.CO2 C.N2 D.O2 E.水蒸气

(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。则加入试剂的先后顺序是
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
(3)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入MgCl2溶液,充分搅拌后经
(4)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是
A.H2 B.CO2 C.N2 D.O2 E.水蒸气
您最近一年使用:0次
2020-06-05更新
|
110次组卷
|
2卷引用:内蒙古集宁一中西校区2019-2020学年高一下学期期中考试化学试题
名校
10 . 要除去NaCl溶液中含有的MgCl2,应选用的试剂和操作方法是( )
| A.加入适量Na2SO4后蒸发 | B.加入适量NaOH溶液后过滤 |
| C.加入过量NaOH溶液后蒸发 | D.加入过量Na2CO3后过滤 |
您最近一年使用:0次
2019-12-05更新
|
108次组卷
|
3卷引用:内蒙古包头市第四中学2019-2020学年高一上学期期中考试化学试题



