名校
1 . 闽盐集团晾晒海水获得的粗盐中含有可溶性杂质 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是
 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是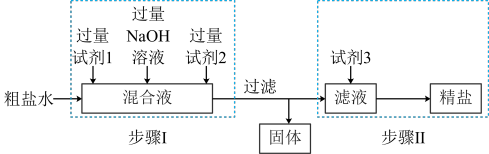
A.“步骤Ⅰ”中试剂1为 溶液,试剂2为 溶液,试剂2为 溶液 溶液 |
| B.“步骤Ⅰ”生成的沉淀也可在加完试剂3之后一次性过滤 |
| C.“步骤Ⅱ”试剂3可以用稀硫酸代替稀盐酸 |
| D.“步骤Ⅱ”从滤液中获得精盐的方法是蒸发结晶 |
您最近一年使用:0次
名校
2 . 海水资源非常丰富。某化学实验小组同学为了从海带中提取碘和海水提溴,进行以下实验:
Ⅰ.从海带中提取碘单质,实验流程图如下:
(1)在进行步骤①之前,称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入___________ 中灼烧至海带完全成灰烬。
(2)步骤④中使用稀硫酸和 溶液能更有利于提取碘,写出离子方程式
溶液能更有利于提取碘,写出离子方程式___________ 。
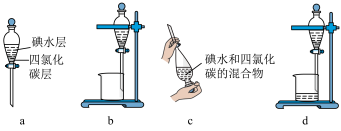
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是___________ (填字母)。___________ 。
Ⅱ.海水中主要离子的含量如下:
(5)利用海水可以提取溴和镁,提取过程如下: 溶液中得到
溶液中得到 晶体的主要实验操作是
晶体的主要实验操作是___________ 、洗涤、烘干。从 晶体中得到无水
晶体中得到无水 的主要方法是
的主要方法是___________ 。
②用 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为___________ 。
③依据上述流程,若将5 海水中的溴元素转化为工业溴,至少需要标准状况下
海水中的溴元素转化为工业溴,至少需要标准状况下 的体积为
的体积为___________ L(忽略 溶解)。
溶解)。
Ⅰ.从海带中提取碘单质,实验流程图如下:
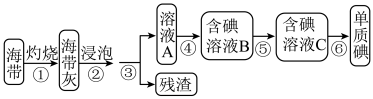
(1)在进行步骤①之前,称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入
(2)步骤④中使用稀硫酸和
 溶液能更有利于提取碘,写出离子方程式
溶液能更有利于提取碘,写出离子方程式(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是
Ⅱ.海水中主要离子的含量如下:
| 成分 |  |  |  |  |  |  |  |
含量/( ) ) | 18980 | 10560 | 2560 | 1272 | 400 | 142 | 64 |
(5)利用海水可以提取溴和镁,提取过程如下:
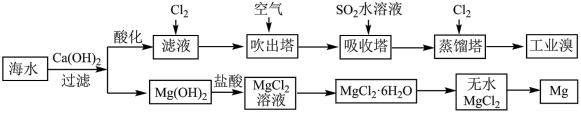
 溶液中得到
溶液中得到 晶体的主要实验操作是
晶体的主要实验操作是 晶体中得到无水
晶体中得到无水 的主要方法是
的主要方法是②用
 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为③依据上述流程,若将5
 海水中的溴元素转化为工业溴,至少需要标准状况下
海水中的溴元素转化为工业溴,至少需要标准状况下 的体积为
的体积为 溶解)。
溶解)。
您最近一年使用:0次
名校
3 . 高锰酸钾生产过程中产生的废锰渣(主要成分为 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
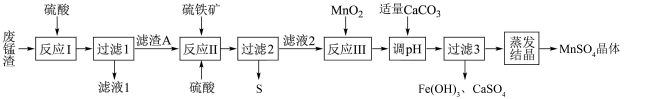
已知:硫铁矿的主要成分为二硫化亚铁( ,杂质不参与反应)。
,杂质不参与反应)。
回答下列问题:
(1)二硫化亚铁中S元素的化合价为_______ 。
(2)①滤渣A的主要成分是_______ (填化学式);
②“反应II”生成 、
、 等物质的离子方程式为
等物质的离子方程式为_______ 。
③“反应III”中还原剂和氧化剂物质的量之比为_______ ;
④“调 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为_______ 。
 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
已知:硫铁矿的主要成分为二硫化亚铁(
 ,杂质不参与反应)。
,杂质不参与反应)。回答下列问题:
(1)二硫化亚铁中S元素的化合价为
(2)①滤渣A的主要成分是
②“反应II”生成
 、
、 等物质的离子方程式为
等物质的离子方程式为③“反应III”中还原剂和氧化剂物质的量之比为
④“调
 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为
您最近一年使用:0次
名校
4 . 化工产品中,含氯物质众多,其用途广泛。回答下列问题:
(1)如图为氯及其化合物的“价-类”二维图。缺失的物质B为_______ (填化学式)。

(2)次氯酸钠是一种含氯物质,取含次氯酸钠14.9g/L的“84”消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为_______ mol/L。
(3)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知:Ca(ClO3)2易溶于水。
①“一系列操作”为_______ 、_______ 。
②“转化”发生反应的离子方程式为_______ 。
(1)如图为氯及其化合物的“价-类”二维图。缺失的物质B为

(2)次氯酸钠是一种含氯物质,取含次氯酸钠14.9g/L的“84”消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
(3)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知:Ca(ClO3)2易溶于水。
①“一系列操作”为
②“转化”发生反应的离子方程式为
您最近一年使用:0次
名校
5 . 氯化亚铜(CuCl)难溶于醇和水,在潮湿空气中易水解氧化,广泛应用于冶金工业,以铜为原料生产 的流程如下:
的流程如下:错误 的是
 的流程如下:
的流程如下: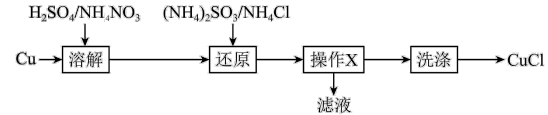
A.“溶解”时可能发生的反应: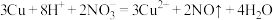 |
B.“还原”反应的氧化产物是 或 或 |
| C.“操作X”是过滤 |
| D.“洗涤”时先用硝酸洗,再用乙醇洗 |
您最近一年使用:0次
2024-03-14更新
|
513次组卷
|
4卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一下学期第一次月考化学试题
6 . 某工厂的工业废水中含有大量的 、较多量的
、较多量的 和
和 ,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀
,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀 、NaOH溶液)
、NaOH溶液)

(1)若废水是由 、
、 和
和 组成的混合溶液,其中
组成的混合溶液,其中 ,
, ,
, ,(溶液中
,(溶液中 和
和 浓度忽略不计),则
浓度忽略不计),则 为
为________  。
。
(2)试剂①是________ 。
(3)固体E的成分是________ (填化学式),操作c名称为________ 。
(4)若取2mL溶液D加入试管中,然后向其中滴加氢氧化钠溶液,可观察到的现象是________ ,此过程中涉及氧化还原反应的化学方程式是________ 。
(5)回收的 经一系列变化后可制得一种新型绿色净水剂高铁酸钠
经一系列变化后可制得一种新型绿色净水剂高铁酸钠 ,主要用于饮用水处理。其中一种制备原理如下,请配平该反应的离子方程式:
,主要用于饮用水处理。其中一种制备原理如下,请配平该反应的离子方程式:_____
________ ________
________ ________
________ ________
________ ________
________ ________
________ ,
,
当有 生成时,转移电子的数目约为
生成时,转移电子的数目约为________ 个。
 、较多量的
、较多量的 和
和 ,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀
,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀 、NaOH溶液)
、NaOH溶液)
(1)若废水是由
 、
、 和
和 组成的混合溶液,其中
组成的混合溶液,其中 ,
, ,
, ,(溶液中
,(溶液中 和
和 浓度忽略不计),则
浓度忽略不计),则 为
为 。
。(2)试剂①是
(3)固体E的成分是
(4)若取2mL溶液D加入试管中,然后向其中滴加氢氧化钠溶液,可观察到的现象是
(5)回收的
 经一系列变化后可制得一种新型绿色净水剂高铁酸钠
经一系列变化后可制得一种新型绿色净水剂高铁酸钠 ,主要用于饮用水处理。其中一种制备原理如下,请配平该反应的离子方程式:
,主要用于饮用水处理。其中一种制备原理如下,请配平该反应的离子方程式:________
 ________
________ ________
________ ________
________ ________
________ ________
________ ,
,当有
 生成时,转移电子的数目约为
生成时,转移电子的数目约为
您最近一年使用:0次
2024-02-03更新
|
119次组卷
|
2卷引用:内蒙古呼和浩特市2023-2024学年高一上学期期末教学质量检测化学试卷
名校
解题方法
7 . 现有含有少NaCl、 、
、 等杂质的
等杂质的 溶液,选择适当的试剂除去杂质,得到纯净的
溶液,选择适当的试剂除去杂质,得到纯净的 固体,实验流程如下图所示。
固体,实验流程如下图所示。

(1)沉淀A的主要成分是___________ (填化学式)。
(2)③加入过量的Y的目的是___________ 。
(3)溶液3中肯定含有的杂质是___________ ,为除去杂质可向溶液3中加入过量的___________ 。
 、
、 等杂质的
等杂质的 溶液,选择适当的试剂除去杂质,得到纯净的
溶液,选择适当的试剂除去杂质,得到纯净的 固体,实验流程如下图所示。
固体,实验流程如下图所示。 
(1)沉淀A的主要成分是
(2)③加入过量的Y的目的是
(3)溶液3中肯定含有的杂质是
您最近一年使用:0次
8 . 某废旧金属材料中主要含Fe、Cu、Al、 、
、 、
、 (其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
(1)“焙烧”的目的主要是将金属单质转化为氧化物,并除去_______ 。
(2)“碱浸”时发生反应的化学方程式为_______ 。
(3)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是_______ 。
(4)第一次酸浸完全后“加入过量试剂a”后发生的化学反应中有一个属于化合反应,其离子方程式为_______ 。
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量杂质离子,该反应的离子方程式为_______ 。
①设计实验检验滤液Ⅱ中是否含有上述离子:_______ 。
②若要定量测定所得绿矾纯度,可通过如下方法:称取 样品用稀硫酸溶解,滴加
样品用稀硫酸溶解,滴加 的酸性
的酸性 溶液,恰好完全反应时,消耗酸性
溶液,恰好完全反应时,消耗酸性 溶液的体积为
溶液的体积为 ,则
,则 的纯度为
的纯度为_______ 。(写出计算过程,结果保留三位有效数字)已知: (未配平)
(未配平)
 、
、 、
、 (其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。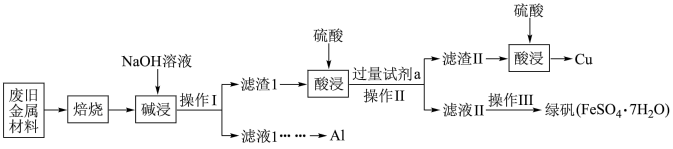
(1)“焙烧”的目的主要是将金属单质转化为氧化物,并除去
(2)“碱浸”时发生反应的化学方程式为
(3)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是
(4)第一次酸浸完全后“加入过量试剂a”后发生的化学反应中有一个属于化合反应,其离子方程式为
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量杂质离子,该反应的离子方程式为
①设计实验检验滤液Ⅱ中是否含有上述离子:
②若要定量测定所得绿矾纯度,可通过如下方法:称取
 样品用稀硫酸溶解,滴加
样品用稀硫酸溶解,滴加 的酸性
的酸性 溶液,恰好完全反应时,消耗酸性
溶液,恰好完全反应时,消耗酸性 溶液的体积为
溶液的体积为 ,则
,则 的纯度为
的纯度为 (未配平)
(未配平)
您最近一年使用:0次
2023-07-28更新
|
433次组卷
|
2卷引用:内蒙古自治区乌海市第一中学2023-2024学年高一下学期4月第一次月考化学试题
解题方法
9 . 海洋约占地球表面积的71%,其中的水资源和其他化学资源具有十分巨大的开发潜力。例如可从海水中提取镁、从海带中提取碘。海带中含有碘元素,从海带中提取碘的实验过程如下图所示:

(1)实验步骤①会用到下列仪器中的___________ (填字母)。
a.陶土网 b.坩埚 c.泥三角 d.蒸发皿
(2)步骤⑥的操作名称是___________ 。
(3)步骤④中反应的离子方程式为___________ 。
(4)请设计一种检验水溶液中是否含有碘单质的方法:___________ 。
(5)海带灰中含有的硫酸盐、碳酸盐等,在实验步骤___________ (填序号)中实现与碘分离。

(1)实验步骤①会用到下列仪器中的
a.陶土网 b.坩埚 c.泥三角 d.蒸发皿
(2)步骤⑥的操作名称是
(3)步骤④中反应的离子方程式为
(4)请设计一种检验水溶液中是否含有碘单质的方法:
(5)海带灰中含有的硫酸盐、碳酸盐等,在实验步骤
您最近一年使用:0次
名校
10 . 一种带有多孔结构的镍铝合金对 有较强的吸附性,其高催化活性和热稳定性使该镍铝合金被广泛用于工业生产和有机合成反应中。以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程如图所示。
有较强的吸附性,其高催化活性和热稳定性使该镍铝合金被广泛用于工业生产和有机合成反应中。以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程如图所示。

回答下列有关问题:
(1)在空气中“煅烧”镍黄铁矿生成 、
、 和一种有刺激性气味的气体,该气体为
和一种有刺激性气味的气体,该气体为_______ (填化学式)。
(2)已知 中C的化合价为+2,则Ni的化合价为
中C的化合价为+2,则Ni的化合价为_______ ,“ ”中发生的反应类型为
”中发生的反应类型为_______ 。
(3)Ni、Al高温熔融时,通入Ar的主要作用是_______ 。高温熔融物冷却后,需要进行粉碎处理,粉碎的目的是_______ 。
(4)为增强镍铝合金对 的吸附性,“碱浸”需溶解部分铝的主要目的是铝溶解的过程中会产生大量气体,可以使镍产生多孔结构,从而增强对
的吸附性,“碱浸”需溶解部分铝的主要目的是铝溶解的过程中会产生大量气体,可以使镍产生多孔结构,从而增强对 的吸附性,主要反应的离子方程式为
的吸附性,主要反应的离子方程式为_______ 。
(5)“浸出液”中的铝元素可循环利用,回收铝元素并制备铝的流程为:

加入足量的X后,获得固体 的操作是
的操作是_______ ,洗涤沉淀的操作是_______ 。
 有较强的吸附性,其高催化活性和热稳定性使该镍铝合金被广泛用于工业生产和有机合成反应中。以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程如图所示。
有较强的吸附性,其高催化活性和热稳定性使该镍铝合金被广泛用于工业生产和有机合成反应中。以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程如图所示。
回答下列有关问题:
(1)在空气中“煅烧”镍黄铁矿生成
 、
、 和一种有刺激性气味的气体,该气体为
和一种有刺激性气味的气体,该气体为(2)已知
 中C的化合价为+2,则Ni的化合价为
中C的化合价为+2,则Ni的化合价为 ”中发生的反应类型为
”中发生的反应类型为(3)Ni、Al高温熔融时,通入Ar的主要作用是
(4)为增强镍铝合金对
 的吸附性,“碱浸”需溶解部分铝的主要目的是铝溶解的过程中会产生大量气体,可以使镍产生多孔结构,从而增强对
的吸附性,“碱浸”需溶解部分铝的主要目的是铝溶解的过程中会产生大量气体,可以使镍产生多孔结构,从而增强对 的吸附性,主要反应的离子方程式为
的吸附性,主要反应的离子方程式为(5)“浸出液”中的铝元素可循环利用,回收铝元素并制备铝的流程为:

加入足量的X后,获得固体
 的操作是
的操作是
您最近一年使用:0次



