名校
1 . 海水资源非常丰富。某化学实验小组同学为了从海带中提取碘和海水提溴,进行以下实验:
Ⅰ.从海带中提取碘单质,实验流程图如下:
(1)在进行步骤①之前,称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入___________ 中灼烧至海带完全成灰烬。
(2)步骤④中使用稀硫酸和 溶液能更有利于提取碘,写出离子方程式
溶液能更有利于提取碘,写出离子方程式___________ 。
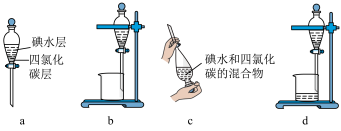
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是___________ (填字母)。___________ 。
Ⅱ.海水中主要离子的含量如下:
(5)利用海水可以提取溴和镁,提取过程如下: 溶液中得到
溶液中得到 晶体的主要实验操作是
晶体的主要实验操作是___________ 、洗涤、烘干。从 晶体中得到无水
晶体中得到无水 的主要方法是
的主要方法是___________ 。
②用 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为___________ 。
③依据上述流程,若将5 海水中的溴元素转化为工业溴,至少需要标准状况下
海水中的溴元素转化为工业溴,至少需要标准状况下 的体积为
的体积为___________ L(忽略 溶解)。
溶解)。
Ⅰ.从海带中提取碘单质,实验流程图如下:
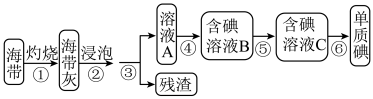
(1)在进行步骤①之前,称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入
(2)步骤④中使用稀硫酸和
 溶液能更有利于提取碘,写出离子方程式
溶液能更有利于提取碘,写出离子方程式(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是
Ⅱ.海水中主要离子的含量如下:
| 成分 |  |  |  |  |  |  |  |
含量/( ) ) | 18980 | 10560 | 2560 | 1272 | 400 | 142 | 64 |
(5)利用海水可以提取溴和镁,提取过程如下:
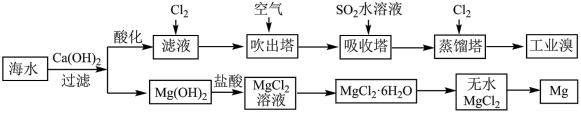
 溶液中得到
溶液中得到 晶体的主要实验操作是
晶体的主要实验操作是 晶体中得到无水
晶体中得到无水 的主要方法是
的主要方法是②用
 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为③依据上述流程,若将5
 海水中的溴元素转化为工业溴,至少需要标准状况下
海水中的溴元素转化为工业溴,至少需要标准状况下 的体积为
的体积为 溶解)。
溶解)。
您最近一年使用:0次
2 . 某废旧金属材料中主要含Fe、Cu、Al、 、
、 、
、 (其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
(1)“焙烧”的目的主要是将金属单质转化为氧化物,并除去_______ 。
(2)“碱浸”时发生反应的化学方程式为_______ 。
(3)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是_______ 。
(4)第一次酸浸完全后“加入过量试剂a”后发生的化学反应中有一个属于化合反应,其离子方程式为_______ 。
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量杂质离子,该反应的离子方程式为_______ 。
①设计实验检验滤液Ⅱ中是否含有上述离子:_______ 。
②若要定量测定所得绿矾纯度,可通过如下方法:称取 样品用稀硫酸溶解,滴加
样品用稀硫酸溶解,滴加 的酸性
的酸性 溶液,恰好完全反应时,消耗酸性
溶液,恰好完全反应时,消耗酸性 溶液的体积为
溶液的体积为 ,则
,则 的纯度为
的纯度为_______ 。(写出计算过程,结果保留三位有效数字)已知: (未配平)
(未配平)
 、
、 、
、 (其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。
(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾等。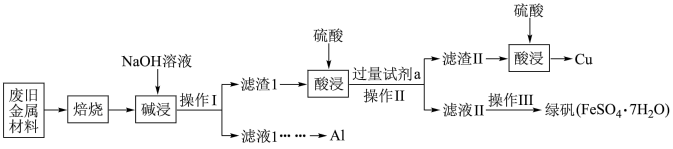
(1)“焙烧”的目的主要是将金属单质转化为氧化物,并除去
(2)“碱浸”时发生反应的化学方程式为
(3)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是
(4)第一次酸浸完全后“加入过量试剂a”后发生的化学反应中有一个属于化合反应,其离子方程式为
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量杂质离子,该反应的离子方程式为
①设计实验检验滤液Ⅱ中是否含有上述离子:
②若要定量测定所得绿矾纯度,可通过如下方法:称取
 样品用稀硫酸溶解,滴加
样品用稀硫酸溶解,滴加 的酸性
的酸性 溶液,恰好完全反应时,消耗酸性
溶液,恰好完全反应时,消耗酸性 溶液的体积为
溶液的体积为 ,则
,则 的纯度为
的纯度为 (未配平)
(未配平)
您最近一年使用:0次
2023-07-28更新
|
446次组卷
|
2卷引用:内蒙古自治区乌海市第一中学2023-2024学年高一下学期4月第一次月考化学试题



