名校
解题方法
1 . 某工厂的废金属屑中主要成分为 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如图
,为探索工业废料的再利用,某化学兴趣小组设计了如图 所示实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体
所示实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体 和胆矾晶体。
和胆矾晶体。
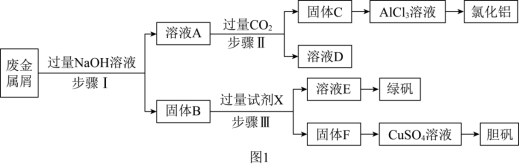
请回答下列问题:
(1)试剂X是_______ 。
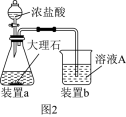
(2)在步骤Ⅱ过程,生成固体C发生的化学反应方程式为_______ ,若用如图 装置制取
装置制取 并通入溶液
并通入溶液 中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免沉淀减少,可采取的改进措施是
中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免沉淀减少,可采取的改进措施是_______ 。
(3)检验溶液 中的金属阳离子时,滴加
中的金属阳离子时,滴加_______ ,溶液无明显现象,说明溶液中不存在Fe3+,用离子方程式解释其可能的原因_______ 。
(4)由绿矾晶体(FeSO4•7H2O)固体配制240mL 0.10mol•L-1FeSO4溶液,需要用到的仪器有药匙、玻璃棒、量筒、烧杯、托盘天平、胶头滴管、_______ 。以下操作会导致所配溶液浓度偏低的是_______ 。
A.容量瓶中原有少量蒸馏水
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
C.定容时俯视刻度线
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如图
,为探索工业废料的再利用,某化学兴趣小组设计了如图 所示实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体
所示实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体 和胆矾晶体。
和胆矾晶体。
请回答下列问题:
(1)试剂X是
(2)在步骤Ⅱ过程,生成固体C发生的化学反应方程式为
 装置制取
装置制取 并通入溶液
并通入溶液 中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免沉淀减少,可采取的改进措施是
中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免沉淀减少,可采取的改进措施是
(3)检验溶液
 中的金属阳离子时,滴加
中的金属阳离子时,滴加(4)由绿矾晶体(FeSO4•7H2O)固体配制240mL 0.10mol•L-1FeSO4溶液,需要用到的仪器有药匙、玻璃棒、量筒、烧杯、托盘天平、胶头滴管、
A.容量瓶中原有少量蒸馏水
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
C.定容时俯视刻度线
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
您最近一年使用:0次
2023-03-18更新
|
238次组卷
|
2卷引用:内蒙古鄂尔多斯市西四旗2023-2024学年高一上学期期末考试化学试题
2 . 某工厂以黄铁矿(主要成分为 )为原料,通过接触氧化法生产
)为原料,通过接触氧化法生产 ,其过程如下所示:
,其过程如下所示:

(1) 中S元素的化合价为
中S元素的化合价为_______ 。
(2)高温煅烧黄铁矿粉可以产生接触氧化需要的混合气体与炉渣(主要成分为Fe2O3),则煅烧炉中发生反应的化学方程式为_______ ;此外,煅烧产物含有的粉尘和水蒸气会降低催化剂的活性,需在进入接触室前除去。
(3)接触室中发生反应的化学方程式为_______ 。
(4)吸收塔尾气的主要成分为_______ ;如将该尾气直接排放到大气中,可能导致的环境问题是_______ ,为提高原料的利用率,可以将尾气再次输入_______ (填设备名称)中参与反应,并在最终排放前用碱液吸收。
(5)经过调查,当地铁路部门设置的物资运价如下:
①可以用铁制罐车运输浓 的原因为
的原因为_______ 。
②已知现代大型 工厂技术成熟,对原料的利用率可达到90%以上,若只从运输成本角度考虑,
工厂技术成熟,对原料的利用率可达到90%以上,若只从运输成本角度考虑,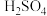 工厂应靠近
工厂应靠近_______ (选填“原料产地”或“产品市场”)。
 )为原料,通过接触氧化法生产
)为原料,通过接触氧化法生产 ,其过程如下所示:
,其过程如下所示:
(1)
 中S元素的化合价为
中S元素的化合价为(2)高温煅烧黄铁矿粉可以产生接触氧化需要的混合气体与炉渣(主要成分为Fe2O3),则煅烧炉中发生反应的化学方程式为
(3)接触室中发生反应的化学方程式为
(4)吸收塔尾气的主要成分为
(5)经过调查,当地铁路部门设置的物资运价如下:
| 车型 | 物资 | 单辆载重 | 单辆运价 |
| 敞车 | 黄铁矿石 | 80 吨 | 2.9元/公里 |
| 罐车 | 浓 | 50 吨 | 2.6元/公里 |
 的原因为
的原因为②已知现代大型
 工厂技术成熟,对原料的利用率可达到90%以上,若只从运输成本角度考虑,
工厂技术成熟,对原料的利用率可达到90%以上,若只从运输成本角度考虑,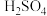 工厂应靠近
工厂应靠近
您最近一年使用:0次
名校
解题方法
3 . 铝是一种重要金属,从铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)中冶炼Al的工业生产流程如下图:
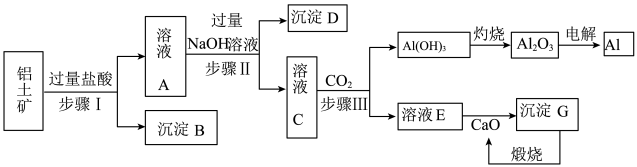
(1)溶液A中含的阳离子主要有________ .
(2)写出步骤II生成溶液C 的离子方程式________ ,步骤I、II、III都要用到的分离方法是________ .
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有________ (填化学式).
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:________ .
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)________ (用含a、b的最简式表示).

(1)溶液A中含的阳离子主要有
(2)写出步骤II生成溶液C 的离子方程式
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)
您最近一年使用:0次
2020-08-28更新
|
304次组卷
|
4卷引用:内蒙古鄂尔多斯市第一中学2022-2023 学年高一上学期期末考试化学试题
4 . 某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜.请根据流程图,填写物质名称(或主要成分的化学式)或操作方法,完成回收硫酸亚铁和铜的简单实验方案.

(1)A、B、D分别为_______ 、______ 、____________ 。
(2)操作Ⅱ、操作Ⅲ分别是_____________ 、_____________________ 。

(1)A、B、D分别为
(2)操作Ⅱ、操作Ⅲ分别是
您最近一年使用:0次
5 . 粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,为除去上述杂质离子,可供选用的试剂有:①稀盐酸 ②Na2CO3溶液 ③BaCl2溶液 ④NaOH溶液,上述四种溶液的加入顺序不合理的是
| A.②③④① | B.③②④① | C.③④②① | D.④③②① |
您最近一年使用:0次
2018-11-25更新
|
88次组卷
|
2卷引用:【市级联考】内蒙古鄂尔多斯市2018-2019学年高一上学期期中考试化学试题
名校
解题方法
6 . ZnO在医药、石化等领域有广泛的用途。研究小组用某闪锌矿(主要成分ZnS,含有FeS、SiO2、MnCO3等杂质)制备氧化锌和硫单质,设计如下流程:
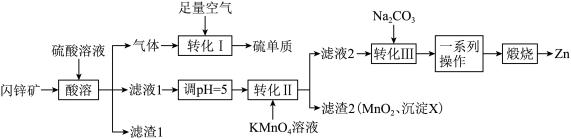
请回答下列问题:
(1)滤渣1的化学式为_______ ,
(2)沉淀X的化学式为______________ 。
(3)“转化Ⅱ”中主要反应的离子方程式为___________________________ 。
(4)“一系列操作”包括过滤、洗涤、干燥。洗涤沉淀的操作为__________________ 。

请回答下列问题:
(1)滤渣1的化学式为
(2)沉淀X的化学式为
(3)“转化Ⅱ”中主要反应的离子方程式为
(4)“一系列操作”包括过滤、洗涤、干燥。洗涤沉淀的操作为
您最近一年使用:0次



