名校
1 . 已知某工业废水中含有大量FeSO4,较多的CuSO4, 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。

(1)步骤1的主要操作是______ ,(填操作名称)需用到的玻璃仪器除烧杯外还有_______ 。
(2)步骤2中发生反应的化学方程式为___________
(3)步骤3中发生反应的化学方程式 为_______
(4)步骤4中涉及的操作是:蒸发浓缩、________ 、过滤、洗涤、烘干。

(1)步骤1的主要操作是
(2)步骤2中发生反应的化学方程式为
(3)步骤3中发生反应的
(4)步骤4中涉及的操作是:蒸发浓缩、
您最近一年使用:0次
2019-10-23更新
|
111次组卷
|
2卷引用:内蒙古锡林浩特市第六中学2019-2020学年高一上学期第一次月考化学试题
名校
2 . 某工厂的工业废水中含有大量的 FeSO4、较多的 CuSO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图完成回收硫酸亚铁和铜的简单实验方案,回答下列问题:(图中所加试剂均为过量,流程图中无需填写)

(1)操作f的名称为____________ ,物质c的成分_________________
(2)试剂a的化学式为_____ ,加入该试剂所发生的化学方程式为______________ 。
(3) 请写出c→h+k的化学方程式______________

(1)操作f的名称为
(2)试剂a的化学式为
(3) 请写出c→h+k的化学方程式
您最近一年使用:0次
2019-10-18更新
|
88次组卷
|
2卷引用:【全国百强校】内蒙古自治区乌兰察布市集宁一中(西校区)2019-2020学年高一上学期期中考试化学试题
名校
3 . 下列除去杂质方法正确的是( )
| A.除去CO2中混有的CO:用浓NaOH溶液洗气 |
| B.除去BaCO3固体中混有的BaSO4:加过量稀盐酸后,过滤、洗涤 |
| C.除去KNO3溶液中混有的NaCl:蒸发结晶 |
| D.除去Cu粉中混有的CuO:加适量稀硫酸后,过滤、洗涤 |
您最近一年使用:0次
2019-09-28更新
|
422次组卷
|
9卷引用:内蒙古自治区奈曼旗第一中学2020-2021学年高一上学期期中考试化学试题
内蒙古自治区奈曼旗第一中学2020-2021学年高一上学期期中考试化学试题河北省邢台市桥西区第一中学2019-2020学年高一9月月考化学试题广东省北大附中深圳南山分校2019-2020学年高一上学期期中考试化学试题山西省朔州市怀仁市第一中学2018-2019学年高一上学期期中考试化学试题安徽省怀宁中学2019-2020学年高一上学期第二次月考化学试题河北省张家口市宣化区2020-2021学年高一上学期9月月考化学试题四川省棠湖中学2020-2021学年高一上学期第一次月考化学试题四川省绵阳市江油一中2020-2021学年高一上学期10月月考化学试题(已下线)第1章能力提升测评卷-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
4 . 从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的工艺流程如下:

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为_________________________ 。
(2)灼烧用的仪器_________________ 填名称)。
(3)沉淀A的成分是______________ (填化学式)。
(4)冶炼铝的化学方程式__________________________________ 。

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为
(2)灼烧用的仪器
(3)沉淀A的成分是
(4)冶炼铝的化学方程式
您最近一年使用:0次
真题
名校
5 . 咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5℃,100℃以上开始升华),有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约1%~5%、单宁酸(Ka约为10−6,易溶于水及乙醇)约3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的流程如下图所示。

索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题:
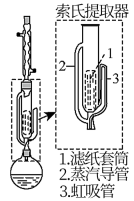
(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是______________ ,圆底烧瓶中加入95%乙醇为溶剂,加热前还要加几粒______________ 。
(2)提取过程不可选用明火直接加热,原因是______________ ,与常规的萃取相比,采用索氏提取器的优点是______________ 。
(3)提取液需经“蒸馏浓缩”除去大部分溶剂,与水相比,乙醇作为萃取剂的优点是______________ 。“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有______________ (填标号)。
A.直形冷凝管 B.球形冷凝管C.接收瓶D.烧杯
(4)浓缩液加生石灰的作用是中和______________ 和吸收______________ 。
(5)可采用如图所示的简易装置分离提纯咖啡因 。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是
。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是______________ 。

索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题:

(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是
(2)提取过程不可选用明火直接加热,原因是
(3)提取液需经“蒸馏浓缩”除去大部分溶剂,与水相比,乙醇作为萃取剂的优点是
A.直形冷凝管 B.球形冷凝管C.接收瓶D.烧杯
(4)浓缩液加生石灰的作用是中和
(5)可采用如图所示的简易装置分离提纯咖啡因
 。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是
。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是
您最近一年使用:0次
2019-06-09更新
|
15788次组卷
|
39卷引用:内蒙古赤峰二中人教版高中化学必修1同步练习:第一章第1节第一课时 化学实验安全
内蒙古赤峰二中人教版高中化学必修1同步练习:第一章第1节第一课时 化学实验安全四川省泸县第四中学2019-2020学年高一下学期第二次月考化学试题安徽省蚌埠市第二中学2022-2023学年高一上学期第一次月考化学试题2019年全国统一考试化学试题(新课标Ⅱ)(已下线)专题10.3 化学实验方案的设计与评价 (练)-《2020年高考一轮复习讲练测》2020届二轮复习 综合实验探究 专题卷(全国通用)2020届人教版高三化学二轮复习非选择题专攻练——化学实验设计与评价的综合应用1专题5.2 化学实验的设计与评价(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升重庆市云阳江口中学校2020届高三下学期第一次月考化学试题西藏自治区林芝市第二高级中学2020届高三上学期第一次月考理科综合化学试题(已下线)专题6.2 实验综合题(必考)(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)第02讲 物质的分离和提纯(精讲)——2021年高考化学一轮复习讲练测(已下线)专题讲座(九) 热点实验综合探究 (精讲)-2021年高考化学一轮复习讲练测(已下线)专题13 实验题大题不丢分-2021年高考化学必做热点专题(已下线)大题05 有机制备类实验题-【考前抓大题】备战2021年高考化学(全国通用)(已下线)专题10 化学实验基础——备战2021年高考化学纠错笔记(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)广西南宁市第十中学2020-2021学年高二下学期3月月考化学试题(已下线)押全国卷理综第26题 实验综合-备战2021年高考化学临考题号押题(课标全国卷)黑龙江省大庆市高中2020-2021学年高二下学期期末考试化学试题(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第28讲 物质的分离、提纯、检验与鉴别(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)云南省弥勒市第一中学2021-2022学年高二上学期第三次月考化学试题(已下线)专题10 化学实验综合—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押全国卷理综第26题 实验综合-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点10 实验方案的设计与评价-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点50 物质的分离、提纯和检验-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第26讲 物质的分离、提纯、检验与鉴别(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题十六实验设计与探究实验(已下线)第一部分 化学综合实验 热点2 实验室中物质的分离、提纯(已下线)专题19 实验综合题云南省宣威市第三中学2022-2023学年高二下学期第三次月考化学试题河南省南阳市2022-2023学年高二下学期期末考试化学试题(已下线)T28-实验题
6 . 工业上制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的Al2O3,然后电解Al2O3得到铝。下图是从铝土矿中提纯Al2O3的简单示意图。其中涉及到的一个反应是:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓。

(1)图示中(1)的实验操作是________ ;图示中(2)加入的试剂__________ 。
(2)试写出下列物质(或溶液中的溶质)的化学式:
B__________________ ;C__________________ ;H________________ ;F______________ 。
(3)写出化学方程式:
①_____________________________________ 。
③_____________________________________ 。
④_________________________________ 。

(1)图示中(1)的实验操作是
(2)试写出下列物质(或溶液中的溶质)的化学式:
B
(3)写出化学方程式:
①
③
④
您最近一年使用:0次
7 . 从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为_________________________ 。
(2)流程乙加入烧碱后生成SiO32-的离子方程式为________________ 。
(3)验证滤液B含Fe3+,可取少量滤液并加入________ (填试剂名称)。
(4)滤液E、K中均含有的溶质是________ (填化学式),写出该溶质的一种用途:________ 。

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为
(2)流程乙加入烧碱后生成SiO32-的离子方程式为
(3)验证滤液B含Fe3+,可取少量滤液并加入
(4)滤液E、K中均含有的溶质是
您最近一年使用:0次
解题方法
8 . 经检测某工厂的酸性废水中所含离子及其浓度如下表所示:
(1)c(H+)=________ mol/L。
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4·7H2O).
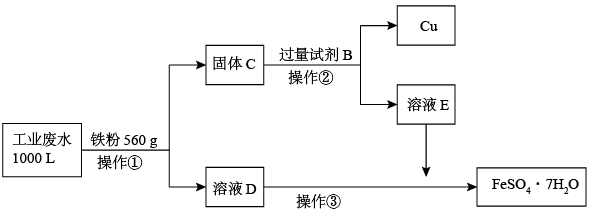
① 工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+ =Fe2++Cu、________________ 、_________________ 。
②试剂B是__________ 。
③ 操作③是_____________ 、_____________ 、过滤,最后用少量冷水洗涤晶体,在低温下干燥。
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是__________________ 。
⑤ 获得的FeSO4·7H2O需密闭保存,原因是___________________________ 。若将所得FeSO4·7H2O配成溶液,向溶液中滴加NaOH溶液的现象是_________________________________________________________________ 。
⑥上述1000 L废水经处理,可获得 FeSO4·7H2O的物质的量是_________ mol。
| 离子 | Fe3+ | Cu2+ | SO42- | Na+ | H+ |
| 浓度/(mol/L) | 2×10-3 | 1×10-3 | 1×10-2 | 2×10-3 |
(1)c(H+)=
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4·7H2O).

① 工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+ =Fe2++Cu、
②试剂B是
③ 操作③是
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是
⑤ 获得的FeSO4·7H2O需密闭保存,原因是
⑥上述1000 L废水经处理,可获得 FeSO4·7H2O的物质的量是
您最近一年使用:0次
2019高三·全国·专题练习
名校
解题方法
9 . 除去粗盐中的杂质MgCl2、CaCl2和Na2SO4,过程如下: 不正确 的是
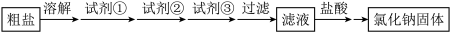
| A.试剂①、②、③分别是NaOH、Na2CO3、BaCl2 |
| B.除去Ca2+的主要反应:Ca2+ + CO32-=CaCO3↓ |
| C.检验SO42-是否除净的方法:取适量滤液,加稀盐酸酸化,再加BaCl2溶液 |
| D.加稀盐酸调节pH后,采用蒸发结晶的方法得到NaCl固体 |
您最近一年使用:0次
2019-01-24更新
|
827次组卷
|
9卷引用:内蒙古赤峰市宁城县2018-2019学年高一上学期期末考试化学试题
(已下线)内蒙古赤峰市宁城县2018-2019学年高一上学期期末考试化学试题(已下线)【南昌新东方】南昌三中2019-2020 高一(上)期末广西壮族自治区桂林市七星区桂林市第十八中学2020-2021学年高一上学期期中考试化学试题广东省广州市白云中学2022-2023学年高一下学期期中考试化学试题天津市2022-2023学年高一下学期学业水平合格考模拟化学试题北京师范大学附属中学2022-2023学年高一下学期期中考试化学试题天津市武清区黄花店中学2023-2024学年高一下学期第一次月考化学试题(文科)(已下线)考点20 化学基础实验——《备战2020年高考精选考点专项突破题集》2024届重庆市乌江新高考协作体高三下学期模拟预测化学试题
名校
10 . Ⅰ.选择不同的试剂或方法除去下列物质中的杂质(括号内为杂质),写出有关反应的方程式:
(1)Mg(Al) 离子方程式:_______________________________________________ 。
(2)Cu(Al) 离子方程式:________________________________________________ 。
(3)Na2CO3固体(NaHCO3固体) 化学方程式:________________________________ 。
(4)Na2CO3溶液(NaHCO3溶液) 离子方程式:________________________________ 。
Ⅱ.配平下列离子方程式:
(1)_____H2S +_____Cr2O72- + _____H+ = _____S↓+_____Cr3+ +_____H2O______
(2)_____C2O42- +_____MnO4- + ______ = _____CO2 + ____Mn2+ + ____H2O______
(1)Mg(Al) 离子方程式:
(2)Cu(Al) 离子方程式:
(3)Na2CO3固体(NaHCO3固体) 化学方程式:
(4)Na2CO3溶液(NaHCO3溶液) 离子方程式:
Ⅱ.配平下列离子方程式:
(1)_____H2S +_____Cr2O72- + _____H+ = _____S↓+_____Cr3+ +_____H2O
(2)_____C2O42- +_____MnO4- + ______ = _____CO2 + ____Mn2+ + ____H2O
您最近一年使用:0次



