1 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向浓度均为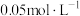 的 的 、 、 混合溶液中滴加少量 混合溶液中滴加少量 溶液,有黄色沉淀生成 溶液,有黄色沉淀生成 | 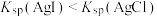 |
B | 用 试纸测得: 试纸测得: 溶液的 溶液的 约为9, 约为9, 溶液的 溶液的 约为8 约为8 |  电离出 电离出 的能力比 的能力比 的强 的强 |
C |  与浓硫酸170℃共热,制得的气体通入酸性 与浓硫酸170℃共热,制得的气体通入酸性 溶液 溶液 | 检验制得气体是否为乙烯 |
D | 向苯酚浊液中滴加 溶液,浊液变清 溶液,浊液变清 | 苯酚的酸性强于 的酸性 的酸性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 固体化合物X由3种元素组成。某学习小组进行了如下实验:
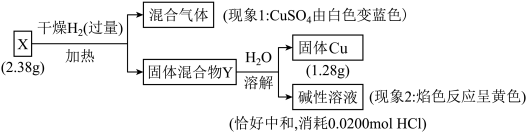
下列推断不正确 的是

下列推断
| A.由现象1得出化合物X含有O元素 |
B.X的化学式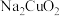 |
C.固体混合物Y的成分可能是 和 和 |
D.若X与浓盐酸反应产生氯气( )气体,则反应中X作氧化剂 )气体,则反应中X作氧化剂 |
您最近半年使用:0次
名校
解题方法
3 .  (三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(1)探究三草酸合铁酸钾的热分解产物。
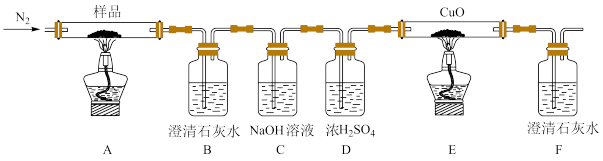
按如上图所示装置进行实验:观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色。
①装置C的作用是_______ 。
②装置E中发生反应的化学方程式为_______ 。
(2)测定三草酸合铁酸钾中铁的含量。
测定原理:

①配制溶液:实验中配制100mL1.0
 溶液,需要的仪器有烧杯、玻璃棒、量筒、
溶液,需要的仪器有烧杯、玻璃棒、量筒、_______ (从下图中选择,写出名称)。

②测定:称量10.00g晶体样品,加1.0
 溶解后配成100
溶解后配成100 溶液。
溶液。
步骤Ⅰ 取20.00 配制好的溶液于锥形瓶中,滴加0.2000
配制好的溶液于锥形瓶中,滴加0.2000
 溶液至恰好完全反应。该操作的目的是
溶液至恰好完全反应。该操作的目的是_______ 。
步骤Ⅱ 向上述溶液中加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中,加稀 酸化,用0.2000
酸化,用0.2000
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液20.00
溶液20.00 。
。
该晶体样品中铁的质量分数为_______ (写出计算过程)。
 (三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:(1)探究三草酸合铁酸钾的热分解产物。

按如上图所示装置进行实验:观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色。
①装置C的作用是
②装置E中发生反应的化学方程式为
(2)测定三草酸合铁酸钾中铁的含量。
测定原理:


①配制溶液:实验中配制100mL1.0

 溶液,需要的仪器有烧杯、玻璃棒、量筒、
溶液,需要的仪器有烧杯、玻璃棒、量筒、
②测定:称量10.00g晶体样品,加1.0

 溶解后配成100
溶解后配成100 溶液。
溶液。步骤Ⅰ 取20.00
 配制好的溶液于锥形瓶中,滴加0.2000
配制好的溶液于锥形瓶中,滴加0.2000
 溶液至恰好完全反应。该操作的目的是
溶液至恰好完全反应。该操作的目的是步骤Ⅱ 向上述溶液中加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中,加稀
 酸化,用0.2000
酸化,用0.2000
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液20.00
溶液20.00 。
。该晶体样品中铁的质量分数为
您最近半年使用:0次
4 . 下列实验方案能达到目的的是
| A.用碱石灰干燥氯气 |
| B.用燃烧的木条检验N2和CO2 |
| C.用CCl4萃取碘水中的碘单质 |
| D.用焰色反应检验碳酸氢钠溶液中是否含有碳酸钠 |
您最近半年使用:0次
5 . 要确认集气瓶中是否集满氯气,正确的操作是
| A.将AgNO3溶液滴入集气瓶中,观察是否生成白色沉淀 |
| B.用手将湿润的淀粉碘化钾试纸放在集气瓶上方,观察是否变蓝 |
| C.将湿润的淀粉碘化钾试纸粘在玻璃棒一端,伸到集气瓶口附近,观察是否变蓝 |
| D.将紫色石蕊液试滴入集气瓶中,观察是否先变红后褪色 |
您最近半年使用:0次
2021-09-10更新
|
323次组卷
|
4卷引用:江苏省盐城市东台创新高级中学2021-2022学年高一上学期12月检测化学试题
江苏省盐城市东台创新高级中学2021-2022学年高一上学期12月检测化学试题(已下线)第15讲 期末复习-2020-2021学年秋季班高一上学期化学教材知识点精讲练(沪科版)山西省临汾市2022-2023学年高一上学期9月月考化学试题课时2 氯气的制法
6 . 下列实验方案能达到目的的是
| A.用排水集气法收集NO气体 |
| B.用燃烧的木条检验N2和CO2 |
| C.用KSCN溶液检验溶液中的Fe2+ |
| D.用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液 |
您最近半年使用:0次
7 . 某混合气体可能含有H2、CO、CO2、HCl、NH3和 H2O(g)中的两种或多种,当混合气体依次通过:(1)少量澄清石灰水(无浑浊现象)(2)Ba(OH)2溶液(出现白色沉淀)(3)浓硫酸(无明显变化),(4)灼热的氧化铜(变红)(5)无水硫酸铜(变蓝).则可以判断混合气体中( )
| A.一定有H2、CO2和HCl | B.一定没有CO2,肯定有H2 |
| C.一定有CO、CO2和H2O(g) | D.可能有CO2、NH3和H2O(g) |
您最近半年使用:0次
2020-11-16更新
|
240次组卷
|
13卷引用:江苏省天一中学2021-2022学年高一上学期期中考试化学(强化班)试题
江苏省天一中学2021-2022学年高一上学期期中考试化学(强化班)试题(已下线)2010年福建省漳州三中高三上学期第二次月考试卷化学试题(已下线)2012-2013学年重庆市重庆一中高一上学期期末考试化学试卷2014-2015学年河南省方城县一中高一12月月考理综化学试卷2014-2015辽宁省实验分校高一上学期期末化学(理)试卷2016届福建省四地六校高三上学期第二次联考化学试卷2016-2017学年广西钦州市高新区高一12月月考化学试卷2016-2017学年四川省绵阳南山中学高一下学期3月月考化学试卷山东省枣庄市第八中学东校区2017-2018学年高一上学期第二次月考(12月)化学试题吉林省长春市九台区第四中学2019-2020学年高一上学期第一次月考化学试题安徽省黄山市屯溪第一中学2020-2021学年高一上学期期中考试化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2020-2021学年高一下学期期中考试化学试题宁夏银川唐徕回民中学2021-2022学年高一上学期期末考试化学试题
名校
8 . 某种混合气体,可能含有N2、HCl和CO,把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体体积都没有变化,经干燥后再通过足量的Na2O2固体,气体体积减小,最后通过灼热的铜网,经充分反应后,气体体积又减小,但还有剩余气体,以下对混合气体成分的判断,正确的是
| A.一定没有N2,CO和HCl中至少有一种 |
| B.一定没有N2,CO和HCl都有 |
| C.一定有N2,CO和HCl中至少有一种 |
| D.一定有N2和HCl,肯定没有CO |
您最近半年使用:0次
2020-10-24更新
|
726次组卷
|
2卷引用:江苏省南京市大厂高级中学2020-2021学年高一上学期期中联考化学试题
名校
9 . 某实验小组设计了如图所示装置对焦炭还原二氧化硅的气体产物进行探究。
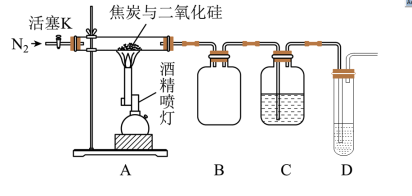
已知: 溶液可用于检验CO,反应的化学方程式为
溶液可用于检验CO,反应的化学方程式为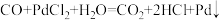 (产生黑色金属钯,使溶液变浑浊)。
(产生黑色金属钯,使溶液变浑浊)。
(1)实验时要长时间通入 ,其目的是
,其目的是__________________________________________________ 。
(2)装置B的作用是__________________________________________________ 。
(3)装置C、D中所盛试剂分别为_____________ 、_____________ ,若装置C,D中溶液均变浑浊,且经检测两气体产物的物质的量相等,则该反应的化学方程式为__________________________ 。
(4)该装置的缺点是__________________________________________________ 。

已知:
 溶液可用于检验CO,反应的化学方程式为
溶液可用于检验CO,反应的化学方程式为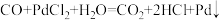 (产生黑色金属钯,使溶液变浑浊)。
(产生黑色金属钯,使溶液变浑浊)。(1)实验时要长时间通入
 ,其目的是
,其目的是(2)装置B的作用是
(3)装置C、D中所盛试剂分别为
(4)该装置的缺点是
您最近半年使用:0次
2020-10-03更新
|
854次组卷
|
7卷引用:江苏省无锡市锡山高级中学2022-2023学年高一下学期期中考试化学试卷
江苏省无锡市锡山高级中学2022-2023学年高一下学期期中考试化学试卷河北省邢台市第一中学2017-2018学年高一下学期开学考试化学试题人教版(2019)必修第二册第五章第三节 课时2必修第二册RJ第5章第三节 无机非金属材料 课时2 新型无机非金属材料云南省曲靖市罗平县第二中学2020-2021学年高一下学期6月月考化学试题(已下线)第08讲 硅酸盐材料 硅(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)安徽省合肥市肥东县综合高中2021-2022学年高一下学期期中考试化学试题
10 . 实验室在 500 °C时隔绝空气加热硫酸亚铁铵[(NH4)2Fe(SO4)2]至分解完全并确定分解产物成分的装置如图所示(已知分解的固体产物可能有 FeO、Fe2O3和 Fe3O4,气体产物可能有 NH3、N2、H2O、SO3和 SO2)。下列说法中正确的是( )
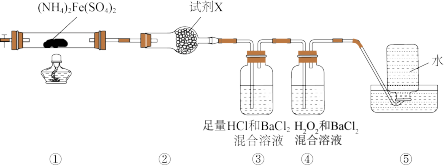

| A.装置②用于检验分解产物中是否有水蒸气生成, 试剂X 最好选用碱石灰 |
| B.装置③用于检验分解产物中是否有SO3气体生成并除去SO3和NH3 |
| C.取①中固体残留物与稀硫酸反应并滴加 KSCN溶液,溶液变红色,则残留物一定为Fe2O3 |
| D.装置④用于检验分解产物中是否有SO2气体生成,装置⑤用于收集生成的NH3和N2 |
您最近半年使用:0次
2020-09-10更新
|
231次组卷
|
16卷引用:江苏省海安高级中学2019-2020学年高二上学期入学考试化学试题
江苏省海安高级中学2019-2020学年高二上学期入学考试化学试题安徽省皖南八校2018届高三第二次联考理综化学试题广东省江门市2018年高考模拟考试理综化学试题(已下线)【中等生百日捷进提升系列-技能方法】专题15 物质的鉴别、分离、提纯类选择题解题方法和策略福建省福州市2018届高三下学期5月模拟考试理综化学试题(已下线)高考母题题源12 物质的检验、分离与提纯山东省济宁市第一中学2019届高三第一学期收心考试化学试题湖南省长沙市师大附中梅溪湖中学2020届高三上学期开学测试化学试题福建省2020届高三化学总复习专题训练——硫酸亚铁铵2020届高考化学二轮题型对题必练—— 物质组成的探究实验题(已下线)专题3.4 硫及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》(已下线)专题3.2 铁及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》(已下线)第02讲 物质的分离和提纯(精练)——2021年高考化学一轮复习讲练测四川省成都市第七中学2021届高三上学期入学考试化学试题(已下线)第28讲 物质的分离、提纯、检验与鉴别(练) — 2022年高考化学一轮复习讲练测(新教材新高考)福建省德化一中、永安一中、漳平一中三校协作2021-2022学年高一下学期5月联考化学试题



