名校
解题方法
1 . FeSO4·7H2O 广泛用于医药和工业领域。下面是以工业废铁屑为原料生产FeSO4·7H2O 的流程图。

(1)加适量碳酸钠溶液的目的是___________ ,反应Ⅰ需要加热数分钟,其原因是___________ 。
(2)判断反应Ⅱ完成的现象是___________ 。反应Ⅱ需要 100mL1mol/L 的稀硫酸,用 98.3%,ρ=1.84g/cm3 的浓硫酸配制。所用的仪器除量筒、烧杯、玻璃棒外,还需要玻璃仪器___________ 。
(3)测定 FeSO4·7H2O 产品中 Fe2+含量的方法是用 KMnO4溶液滴定法(5Fe2++MnO +8H+= 5Fe3++Mn2++4H2O),步骤为:
+8H+= 5Fe3++Mn2++4H2O),步骤为:
Ⅰ.称取 2.8500g FeSO4·7H2O 产品,配制成 250mL 溶液;
Ⅱ.量取 25.00mL 待测溶液于锥形瓶中;
Ⅲ.用硫酸酸化的 0.0100moL/L KMnO4溶液滴定至终点,消耗 KMnO4溶液体积的平均值为 20.00mL。
①判断此滴定实验达到终点的现象是___________ ;
②计算上述样品中 FeSO4·7H2O 的质量分数为___________ (用小数表示,保留三位小数);
(4)已知 FeSO4·7H2O 晶体在加热条件下发生如下反应:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。

①仪器的连接顺序为 a___________ 。
②装置 C 中的 X 为___________ ;该装置中冷水的作用是___________ 。

(1)加适量碳酸钠溶液的目的是
(2)判断反应Ⅱ完成的现象是
(3)测定 FeSO4·7H2O 产品中 Fe2+含量的方法是用 KMnO4溶液滴定法(5Fe2++MnO
 +8H+= 5Fe3++Mn2++4H2O),步骤为:
+8H+= 5Fe3++Mn2++4H2O),步骤为:Ⅰ.称取 2.8500g FeSO4·7H2O 产品,配制成 250mL 溶液;
Ⅱ.量取 25.00mL 待测溶液于锥形瓶中;
Ⅲ.用硫酸酸化的 0.0100moL/L KMnO4溶液滴定至终点,消耗 KMnO4溶液体积的平均值为 20.00mL。
①判断此滴定实验达到终点的现象是
②计算上述样品中 FeSO4·7H2O 的质量分数为
(4)已知 FeSO4·7H2O 晶体在加热条件下发生如下反应:2FeSO4·7H2O
 Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
①仪器的连接顺序为 a
②装置 C 中的 X 为
您最近半年使用:0次
名校
解题方法
2 . 下图是某同学设计的木炭和浓硫酸反应并检验所得产物的实验装置。
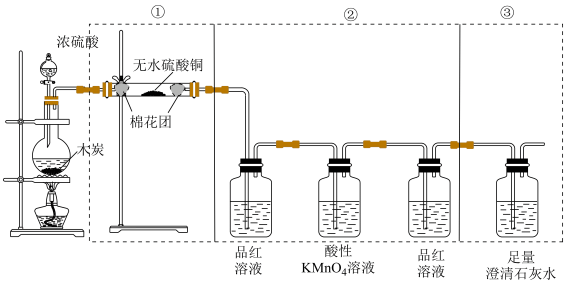
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:___________ 。
(2)②中酸性 溶液的作用是
溶液的作用是___________ ,第二瓶品红溶液的作用是___________ 。
(3)如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,则可以检出的物质是______ ;不能检出的物质是________ 。
(4)如果将仪器的连接顺序变为①、③、②,则可以检出的物质是___________ ;不能检出的物质是___________ 。
(5)有同学希望通过测量③中装置质量的增加来计算反应的木炭的质量,则在②③之间插入一个洗气瓶,其中装___________ (填写试剂名称)。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
(2)②中酸性
 溶液的作用是
溶液的作用是(3)如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,则可以检出的物质是
(4)如果将仪器的连接顺序变为①、③、②,则可以检出的物质是
(5)有同学希望通过测量③中装置质量的增加来计算反应的木炭的质量,则在②③之间插入一个洗气瓶,其中装
您最近半年使用:0次
名校
解题方法
3 . 氧化还原反应是一类重要的化学反应,广泛存在于工农业生产、科学技术和日常生活中。
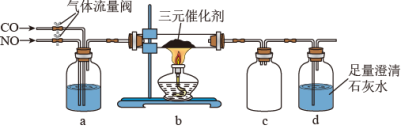
(1)汽车尾气系统中,有毒气体CO和NO在三元催化剂作用下生成无毒气体,某课外化学兴趣小组用如下装置模拟该转化过程。下列说法错误的是_______。
(2)某化工厂基于“绿色化学”理念设计了如下治污工艺流程,下列说法错误的是_______。

(3)某混合气体中可能含有 、
、 、
、 、NO、
、NO、 中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是_______。
中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是_______。
(4)氢化钠(NaH)在野外被用作生氢剂,其原理是 ,该反应中氧化剂是
,该反应中氧化剂是_______ ;被氧化与被还原元素的物质的量之比为:_______ ;
(5)汽车剧烈碰撞时,安全气囊中发生反应: 。该反应中氧化产物与还原产物的质量比为
。该反应中氧化产物与还原产物的质量比为_______ ;若氧化产物比还原产物多19.6 g,则反应生成的 在标准状况下的体积为
在标准状况下的体积为_______ L。
(6)高铁酸钠( ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。写出制备高铁酸钠的离子方程式
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。写出制备高铁酸钠的离子方程式_______ 。
(1)汽车尾气系统中,有毒气体CO和NO在三元催化剂作用下生成无毒气体,某课外化学兴趣小组用如下装置模拟该转化过程。下列说法错误的是_______。

| A.a装置中试剂为浓硫酸,起干燥、观察流速及混合气体的作用 |
B.b装置的硬质玻璃管中发生反应 |
| C.c装置为安全瓶,能防止d装置中的澄清石灰水倒吸 |
D.d装置既可检验气体 ,又可吸收实验中的有害尾气 ,又可吸收实验中的有害尾气 |

A.该流程可用于吸收 |
B.由 转化为 转化为 的过程中,氧化剂和还原剂的物质的量之比为2∶1 的过程中,氧化剂和还原剂的物质的量之比为2∶1 |
C.该过程的总反应为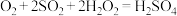 |
D. 可用做该反应过程的催化剂 可用做该反应过程的催化剂 |
 、
、 、
、 、NO、
、NO、 中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是_______。
中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是_______。A.肯定有 和 和 | B.肯定有NO |
C.肯定没有 和 和 | D.可能有 和 和 |
 ,该反应中氧化剂是
,该反应中氧化剂是(5)汽车剧烈碰撞时,安全气囊中发生反应:
 。该反应中氧化产物与还原产物的质量比为
。该反应中氧化产物与还原产物的质量比为 在标准状况下的体积为
在标准状况下的体积为(6)高铁酸钠(
 ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。写出制备高铁酸钠的离子方程式
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。写出制备高铁酸钠的离子方程式
您最近半年使用:0次
解题方法
4 . 氯元素能与许多元素形成种类繁多的化合物,这些含氯化合物在生活及工农业生产中发挥着重要的作用。
(1)从海水中获取粗盐的方法是_______ 。
(2)利用电解饱和食盐水可以制备氢气、氯气、氢氧化钠。电解时阳极产物为_______ ,该产物的检验方法为_______ 。
(3)工业上用氯气和消石灰反应制备漂白粉,其有效成分是_______ (填化学式);写出漂白粉露置在空气中失效过程中所涉及的化学方程式:_______ 、_______ 。
(4)H2与Cl2在点燃条件下可以制取HCl。某同学对HCl性质进行如下预测:
①从物质类别上看,HCl属于酸,其水溶液能与碳酸钙反应,相应的离子方程式为_______ 。
②从化合价角度看,HCl中的Cl元素显-1价,处于氯元素的最低价,因此-1价的Cl元素在反应中可以被_______ (选填“氧化”或“还原”),在一定条件下能与_______ 发生氧化还原反应(填编号)。
a.KI b.NaOH c.KMnO4
(5)已知HClO4是强酸,HClO4在水中的电离方程式为_______ 。
(1)从海水中获取粗盐的方法是
(2)利用电解饱和食盐水可以制备氢气、氯气、氢氧化钠。电解时阳极产物为
(3)工业上用氯气和消石灰反应制备漂白粉,其有效成分是
(4)H2与Cl2在点燃条件下可以制取HCl。某同学对HCl性质进行如下预测:
①从物质类别上看,HCl属于酸,其水溶液能与碳酸钙反应,相应的离子方程式为
②从化合价角度看,HCl中的Cl元素显-1价,处于氯元素的最低价,因此-1价的Cl元素在反应中可以被
a.KI b.NaOH c.KMnO4
(5)已知HClO4是强酸,HClO4在水中的电离方程式为
您最近半年使用:0次
5 . 不能鉴别 和溴蒸汽的是
和溴蒸汽的是
 和溴蒸汽的是
和溴蒸汽的是| A.湿润的淀粉碘化钾试纸 | B.水 |
C. 溶液 溶液 | D. |
您最近半年使用:0次
2022高一·上海·专题练习
解题方法
6 . 某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行):①通过炽热的炭层后,恢复到原状态,气体体积不变;②通过灼热的氧化铜时,粉末变成红色;③通过白色硫酸铜粉末时,粉末变成了蓝色晶体;④通过澄清石灰水,石灰水变浑浊。下列判断正确的是
| A.原混合气体中一定含有CO2、CO和H2 |
| B.原混合气体中一定含有H2、CO,一定没有CO2 |
| C.原混合气体中一定含有H2、CO,可能含有CO2 |
| D.原混合气体中一定含有H2、CO2,可能含有CO |
您最近半年使用:0次
7 . 根据下面实验内容和实验现象推出的结论中,错误的是
| 实验内容 | 实验现象 | 实验结论 | |
| A | 滴加酚酞试液 | 溶液变红色 | 溶液为NaOH或Ca(OH)2 |
| B | 滴加石蕊试液 | 溶液变红色 | 溶液为酸性溶液,pH<7 |
| C | 通入澄清石灰水 | 出现白色浑浊 | 该气体可能是CO2 |
| D | 滴加氯化钡试剂 | 有白色沉淀 | 溶液中可能含有 或 或 等离子 等离子 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 下列鉴别空气、氧气和二氧化碳气体的方法中,正确的是
| A.闻气味 | B.观察颜色 | C.加入澄清石灰水 | D.插入燃着的木条 |
您最近半年使用:0次
9 . 某无色气体可能含有H2O、CO2、CO、H2中的一种或几种,若将该气体依次通过以下实验装置(假设每步操作中,参加反应的气体均完全反应或吸收),下列实验设计能达到预期要求的是
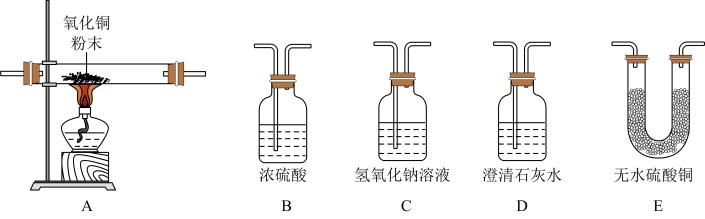

| A.气体依次通过E-D来验证是否含有H2O和CO2 |
| B.气体依次通过A-E来验证是否含有H2 |
| C.气体依次通过A-D来验证是否含有CO |
| D.气体依次通过E-D-C-B-A-D-E来验证是否含有H2O、CO2、CO、H2 |
您最近半年使用:0次
10 . 某混合气体可能含有一氧化碳、二氧化碳、氢气、氯化氢中的一种或几种。进行如图实验,下列推断正确的是
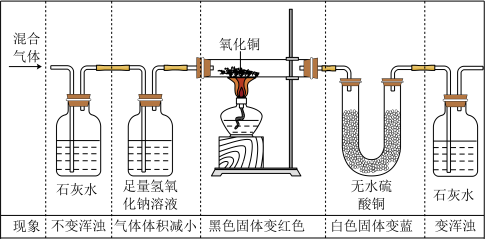

| A.一定无二氧化碳 |
| B.可能含有氯化氢 |
| C.一定有氢气 |
| D.一定有一氧化碳 |
您最近半年使用:0次



