1 . 下列实验方案能达到实验目的的是(部分夹持装置已略去)
 | 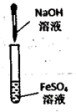 |  | 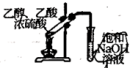 |
A.验证木炭和浓硫酸反应生成 | B.实验室制备 并能较长时间观察到白色固体 并能较长时间观察到白色固体 | C.实验室制备和收集氨气并验满 | D.制备乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-07-07更新
|
153次组卷
|
2卷引用:四川省广安市2020-2021学年高二下学期期末考试化学联考试题
名校
解题方法
2 . 摩尔盐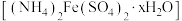 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是___________ 。
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有___________ 。取样品 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为___________ (用含a、b的代数式表示)。
(3)利用摩尔盐分解产生的 ,可制取氯化亚砜
,可制取氯化亚砜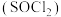 :
: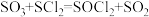 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
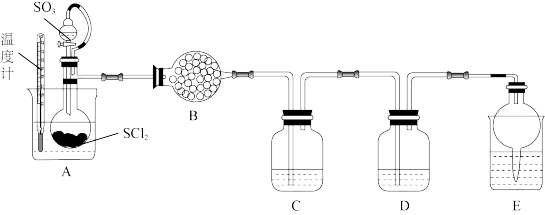
①装置B为无水 ,其作用是
,其作用是___________ 。
②装置C和装置D中的试剂分别是___________ 、___________ (填小写字母)。
a. 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液
(4)利用摩尔盐分解产生的 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
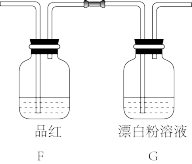
①将少量 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是___________ (用化学反应方程式表示)。
②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是___________ ,其作用是___________ ,通过___________ (填现象)即可证明亚硫酸的酸性强于次氯酸。
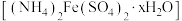 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有
 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为(3)利用摩尔盐分解产生的
 ,可制取氯化亚砜
,可制取氯化亚砜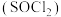 :
: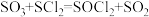 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
①装置B为无水
 ,其作用是
,其作用是②装置C和装置D中的试剂分别是
a.
 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液(4)利用摩尔盐分解产生的
 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
①将少量
 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是
您最近一年使用:0次
2022-07-15更新
|
303次组卷
|
2卷引用:河南省开封市五县2021-2022学年高二下学期期末考试化学试题
解题方法
3 . 某化学小组制备 并验证
并验证 的部分性质,装置如图所示(部分夹持装置省略):
的部分性质,装置如图所示(部分夹持装置省略):

(1)仪器a的名称是___________ 。
(2)装置A制取 的反应中,利用了浓硫酸的
的反应中,利用了浓硫酸的___________ 性,___________ (填“能”或“不能”)用浓硝酸代替。
(3)在滴加浓硫酸之前,需先通入一段时间的 ,此操作的目的是
,此操作的目的是___________ 。
(4)装置B中的反应生成乳白色浑浊的同时生成了一种强碱,则该反应的化学方程式为___________ 。
(5)装置D验证了 的漂白性,为了进一步探究
的漂白性,为了进一步探究 与品红作用的可逆性,请写出有关实验操作及现象:
与品红作用的可逆性,请写出有关实验操作及现象:___________ 。
(6)为测定装置E中收集到的混合气体中二氧化硫的含量,进行如下操作:

当注入标准状况下10mL混合气体时,酸性 ,溶液恰好褪色,假设混合气体中
,溶液恰好褪色,假设混合气体中 能被
能被 溶液充分吸收。已知:
溶液充分吸收。已知: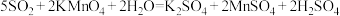 。该混合气体中二氧化硫的体积分数为
。该混合气体中二氧化硫的体积分数为___________ 。
 并验证
并验证 的部分性质,装置如图所示(部分夹持装置省略):
的部分性质,装置如图所示(部分夹持装置省略):
(1)仪器a的名称是
(2)装置A制取
 的反应中,利用了浓硫酸的
的反应中,利用了浓硫酸的(3)在滴加浓硫酸之前,需先通入一段时间的
 ,此操作的目的是
,此操作的目的是(4)装置B中的反应生成乳白色浑浊的同时生成了一种强碱,则该反应的化学方程式为
(5)装置D验证了
 的漂白性,为了进一步探究
的漂白性,为了进一步探究 与品红作用的可逆性,请写出有关实验操作及现象:
与品红作用的可逆性,请写出有关实验操作及现象:(6)为测定装置E中收集到的混合气体中二氧化硫的含量,进行如下操作:

当注入标准状况下10mL混合气体时,酸性
 ,溶液恰好褪色,假设混合气体中
,溶液恰好褪色,假设混合气体中 能被
能被 溶液充分吸收。已知:
溶液充分吸收。已知: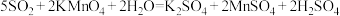 。该混合气体中二氧化硫的体积分数为
。该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
2022-07-04更新
|
280次组卷
|
2卷引用:陕西省安康市2023-2024学年高二上学期开学考化学试题
名校
4 . 下面是某校化学研究性学习小组探究的过量的Fe与浓硫酸反应的实验:
I.甲同学设计如下实验验证反应得到的混合气体中含有SO2、H2、H2O

已知:CaSO3受热易分解
(1)写出过量Fe粉与浓硫酸反应产生等体积的SO2与H2的总化学方程式:________ 。
(2)若按气体从左到右的流向,为达到实验目的,各装置连接顺序是A→______ (不可重复使用)。
(3)A中导管的作用为_____ ,装置E中的干燥管中盛放的物质为碱石灰,其作用是_______ 。
(4)证明有H2存在的实验现象是_________ 。
II.为测定混合气体中SO2的体积分数,,乙同学设计了如下实验方案:

(5) W溶液可以是下列溶液中的______ (填字母代号);
A.H2O2溶液 B.NaOH溶液 C.KMnO4溶液(硫酸酸化) D.氯水
该混合气体中二氧化硫的体积分数为_____________ (用含V、m的代数式表示)。
I.甲同学设计如下实验验证反应得到的混合气体中含有SO2、H2、H2O

已知:CaSO3受热易分解
(1)写出过量Fe粉与浓硫酸反应产生等体积的SO2与H2的总化学方程式:
(2)若按气体从左到右的流向,为达到实验目的,各装置连接顺序是A→
(3)A中导管的作用为
(4)证明有H2存在的实验现象是
II.为测定混合气体中SO2的体积分数,,乙同学设计了如下实验方案:

(5) W溶液可以是下列溶液中的
A.H2O2溶液 B.NaOH溶液 C.KMnO4溶液(硫酸酸化) D.氯水
该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
5 . 下图所示为某同学设计的检验浓硫酸和碳反应所得气体产物的实验装置图。下列说法正确的是


| A.若按①→③→②顺序连接,可检验所有气体产物 |
| B.若装置②只保留a、b,同样可以达到实验目的 |
| C.若圆底绕瓶内碳粉过量,充分反应后恢复到25℃,溶液的pH≥5.6 |
| D.实验结束后,应按从下往上、从左往右的顺序拆卸装置 |
您最近一年使用:0次
2018-05-26更新
|
522次组卷
|
6卷引用:山东省烟台市2021-2022学年高二下学期期末考试化学试题
山东省烟台市2021-2022学年高二下学期期末考试化学试题【全国市级联考】山东省济南市2018届高三5月针对性练习(二模)理综化学试题(已下线)2018年高考题及模拟题汇编 专题11 化学实验基础重庆市2019-2020学年高三下学期网络考试化学试题江西省南昌市四校联盟2020届高三第二次联考理综化学试题(已下线)第13讲 硫及其化合物(精讲)-2022年一轮复习讲练测
6 . 下列对实验的分析不合理的是
| 实验1 | 实验2 | 实验3 | |
| 装置 | 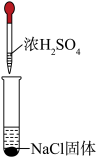 | 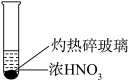 | 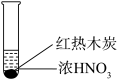 |
| 现象 | 溶液颜色无明显变化;把蘸浓氨水的玻璃棒靠近试管口,产生白烟 | 产生红棕色气体 | 产生红棕色气体 |
| A.实验1中的白烟是NH4Cl的固体小颗粒 |
| B.由实验2中的红棕色气体可以推断产生的气体一定是混合气体 |
| C.实验3中的红棕色气体不一定能说明木炭与浓硝酸发生了反应 |
| D.上述实验体现了浓H2SO4的难挥发性和浓硝酸的强氧化性 |
您最近一年使用:0次
名校
7 . (一)某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了以下实验流程图:

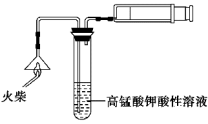
请回答以下问题:
(1)为验证气体A,按上图所示组装好装置,下一步操______________ ,观察到 ________ 的现象,即可证明火柴头上含有S元素。
(2)要证明火柴头中含有Cl元素的后续实验步骤___________________________________ 。
(3)有学生提出以下方案测定火柴头中KClO3的含量,主要实验步骤如下:刮取火柴头研碎,称其质量为2.45g→用蒸馏水浸泡后过滤、洗涤残渣→往装有滤液和洗涤液的烧杯中加过量的NaNO2溶液、AgNO3溶液和稀硝酸,搅拌充分反应→过滤、洗涤干燥→称得沉淀质量为1.435g。
①洗涤残渣的目的__________________________________________ ;
②实验测得火柴头中KClO3的质量分数为__________ 。
(二)某研究性学习小组为了研究影响化学速率的因素,设计了如下方案:
已知:反应的方程式:2KMnO4+5H2C2O4+3H2SO4 = K2SO4+2MnSO4+10CO2↑+8H2O
(1)实验①和②研究H2C2O4溶液浓度对反应速率的影响,则V1=___ mL,V2=___ mL。
(2)下列有关该实验的叙述正确的是___ 。
A.实验室必须用移液管或滴定管来量取液体的体积
B.实验计时方法是从溶液混合开始记时,到紫红色刚好褪去计时结束时结束
C.在同一温度下,最好采用平行多次实验,以确保实验数据的可靠性
D.实验①和③可研究温度对反应速率的影响
(3)某小组在进行每组实验时,均发现该反应是开始很慢,突然会加快,其可能的原因是__________________________________________________ 。


请回答以下问题:
(1)为验证气体A,按上图所示组装好装置,下一步操
(2)要证明火柴头中含有Cl元素的后续实验步骤
(3)有学生提出以下方案测定火柴头中KClO3的含量,主要实验步骤如下:刮取火柴头研碎,称其质量为2.45g→用蒸馏水浸泡后过滤、洗涤残渣→往装有滤液和洗涤液的烧杯中加过量的NaNO2溶液、AgNO3溶液和稀硝酸,搅拌充分反应→过滤、洗涤干燥→称得沉淀质量为1.435g。
①洗涤残渣的目的
②实验测得火柴头中KClO3的质量分数为
(二)某研究性学习小组为了研究影响化学速率的因素,设计了如下方案:
| 实验 编号 | 0.01mol•L-1酸性KMnO4溶液 | 0.1mol•L-1 H2C2O4溶液 | 水 | 反应温度/℃ | 反应时间/s |
| ① | 5.0mL | 5.0mL | 0 | 20 | 125 |
| ② | V1 | V2 | 2.0mL | 20 | 320 |
| ③ | 5.0mL | 5.0mL | 0 | 50 | 30 |
(1)实验①和②研究H2C2O4溶液浓度对反应速率的影响,则V1=
(2)下列有关该实验的叙述正确的是
A.实验室必须用移液管或滴定管来量取液体的体积
B.实验计时方法是从溶液混合开始记时,到紫红色刚好褪去计时结束时结束
C.在同一温度下,最好采用平行多次实验,以确保实验数据的可靠性
D.实验①和③可研究温度对反应速率的影响
(3)某小组在进行每组实验时,均发现该反应是开始很慢,突然会加快,其可能的原因是
您最近一年使用:0次
名校
8 . 实验室用草酸与浓硫酸反应制备 ,其原理如下:
,其原理如下: 。某课题组同学设计实验探究
。某课题组同学设计实验探究 还原磷石膏(
还原磷石膏( )并检验气体产物[
)并检验气体产物[ 能被
能被 悬浊液吸收生成
悬浊液吸收生成 ],装置如图所示。
],装置如图所示。
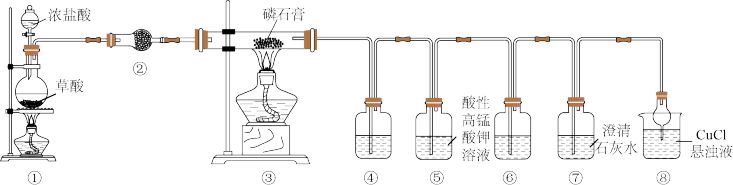
(1)在实验室中利用装置①还可制取的气体有__________ (填一种即可)。
(2)装置②中盛放的试剂为_________ ,装置④⑥中盛放的试剂均为品红溶液,其作用分别为________________ 、________________ 。
(3)若装置④中溶液褪色,装置⑥中溶液不褪色,装置⑦中溶液变浑浊,则装置③中发生反应的化学方程式为_________________________ 。
(4)装置⑤中发生反应的离子方程式为_________________________ 。
(5)实验结束时,先熄灭____________ (填“①”或“③”)处的酒精灯,其目的为_________________ 。
 ,其原理如下:
,其原理如下: 。某课题组同学设计实验探究
。某课题组同学设计实验探究 还原磷石膏(
还原磷石膏( )并检验气体产物[
)并检验气体产物[ 能被
能被 悬浊液吸收生成
悬浊液吸收生成 ],装置如图所示。
],装置如图所示。
(1)在实验室中利用装置①还可制取的气体有
(2)装置②中盛放的试剂为
(3)若装置④中溶液褪色,装置⑥中溶液不褪色,装置⑦中溶液变浑浊,则装置③中发生反应的化学方程式为
(4)装置⑤中发生反应的离子方程式为
(5)实验结束时,先熄灭
您最近一年使用:0次
2020-12-11更新
|
164次组卷
|
3卷引用:河南省焦作市2019-2020学年高二上学期期末学业水平测试化学试题
20-21高二上·浙江·期中
解题方法
9 . 如图所示分别是某课外活动小组设计的制取氨气并用氨气进行喷泉实验的三组装置,回答下列问题:

(1)用A图所示的装置可制备干燥的NH3:
①反应的化学方程式为___________ 。
②干燥管中干燥剂能否改用无水CaCl2?___________ (填“能”或“不能”)。
(2)用B图所示的装置可快速制取较大量NH3,检验NH3是否收集满的实验方法是___________ 。
(3)用C图所示的装置进行喷泉实验,若测得C装置烧瓶中NH3的质量是相同状况下相同体积H2质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧瓶容积的___________ 。

(1)用A图所示的装置可制备干燥的NH3:
①反应的化学方程式为
②干燥管中干燥剂能否改用无水CaCl2?
(2)用B图所示的装置可快速制取较大量NH3,检验NH3是否收集满的实验方法是
(3)用C图所示的装置进行喷泉实验,若测得C装置烧瓶中NH3的质量是相同状况下相同体积H2质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧瓶容积的
您最近一年使用:0次
名校
10 . 已知饱和氯化铵溶液与亚硝酸钠晶体混合加热可制备氮气。利用如下装置制取氮气,并用氮气制备Ca3N2,Ca3N2遇水发生水解反应。下列说法错误的是


A.①中发生的化学反应为NaNO2+NH4Cl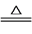 NaCl+N2↑+2H2O NaCl+N2↑+2H2O |
| B.④、⑥中依次盛装的试剂可以是浓H2SO4、碱石灰 |
| C.③中盛放的试剂是NaOH 溶液 |
| D.实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊试纸变蓝 |
您最近一年使用:0次
2018-03-01更新
|
612次组卷
|
9卷引用:河北省承德市隆化县存瑞中学2020-2021学年高二下学期期末联考化学试题
河北省承德市隆化县存瑞中学2020-2021学年高二下学期期末联考化学试题山西省孝义市2018届高三下学期高考模拟卷(一)理综化学试题(已下线)2019年8月25日 《每日一题》2020年高考一轮复习—— 每周一测山西大学附中2020届高三上学期第二次模块诊断化学试题河北省隆化县存瑞中学2020届高三上学期期中考试化学试题(已下线)第6单元 常见的非金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)第7周 晚练题-备战2022年高考化学周测与晚练(新高考专用)(已下线)第29讲 常见气体的制备与性质实验(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第27讲 物质的制备与性质实验(练)-2023年高考化学一轮复习讲练测(新教材新高考)



