24. (一)常温下,向100 mL 0.01 mol·L
-1 HA溶液中逐滴加入0.02 mol·L
-1 MOH溶液,图中所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。
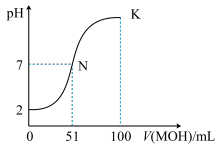
(1)由图中信息可知HA为
____________酸(填“强”或“弱”)。
(2)常温下一定浓度的MA稀溶液的pH=a,则a
________7,用离子方程式表示其原因
_________________,此时,溶液中水电离出的c(OH
-)=
__________mol·L
-1。
(3)请写出
K点所对应的溶液中离子浓度的大小关系:
_____________________ (4)K点所对应的溶液中,c(M
+)+c(MOH)
__________2c(A
-)
(二)Ⅰ.氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001 moL·L
-1酸性KMnO
4溶液和未知浓度的无色NaHSO
3溶液。反应的离子方程式是2MnO
4-+5HS0
3-+H
+= 2Mn
2++5SO
42-+3H
2O。
请完成下列问题:
(1)该滴定实验所需仪器有下列中的
________。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL) C.量筒(10 mL) D.锥形瓶 E.铁架台 F.滴定管夹 G.烧杯 H.白纸 I.胶头滴管 J.漏斗
(2)本实验
________(填“需要”或“不需要”)使用指示剂,理由是
___________________ Ⅱ.一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。某研究性学习小组在实验室中配制1 mol·L
-1稀硫酸标准溶液。然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是
________(填序号)。
A.实验中所用到的滴定管、容量瓶在使用前均需要查漏
B.若选用100 mL容量瓶配制标准酸溶液,需用密度为1.84 g·mL
-1、98%的浓硫酸5.43 mL
C.容量瓶中有少量的蒸馏水,会导致所配标准溶液的浓度偏小
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大
E.若配制标准酸溶液在定容时俯视读数,则导致所测的NaOH溶液浓度偏大
F.中和滴定实验,若滴定前平视读数、滴定结束俯视读数,则导致实验结果偏大