1 .  具有氧化性、还原性和漂白性,某同学在实验室利用
具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问题:
做相关验证和探究实验。回答下列问题:
(1)用如图1装置(夹持仪器已省略)验证 具有氧化性。
具有氧化性。 的名称为
的名称为___________ 。
②装置甲试管中反应的离子方程式为___________ 。
③说明 具有氧化性的现象为
具有氧化性的现象为___________ 。
(2)该同学设计如图2所示装置(夹持仪器已省略)制备 (难溶解于水中)。
(难溶解于水中)。 的作用是
的作用是___________ 。
②三颈烧瓶中反应的化学方程式为___________ 。
(3)该实验体现了 的性质是
的性质是___________ 。
(4)实验表明,将纯净的 缓缓地通入到
缓缓地通入到 溶液中,得到
溶液中,得到 沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
假设Ⅰ:溶液中的 ;
;
假设Ⅱ:溶解在水中的氧气。
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
实验i现象为___________ ,实验ii的现象为___________ 。
②验证假设Ⅱ。请完成下列表格:
实验iv的步骤为___________ ,实验目的是___________ 。
 具有氧化性、还原性和漂白性,某同学在实验室利用
具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问题:
做相关验证和探究实验。回答下列问题:(1)用如图1装置(夹持仪器已省略)验证
 具有氧化性。
具有氧化性。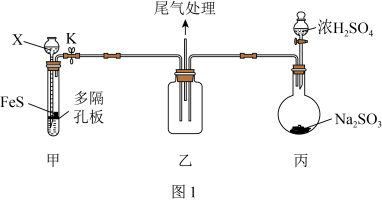
 的名称为
的名称为②装置甲试管中反应的离子方程式为
③说明
 具有氧化性的现象为
具有氧化性的现象为(2)该同学设计如图2所示装置(夹持仪器已省略)制备
 (难溶解于水中)。
(难溶解于水中)。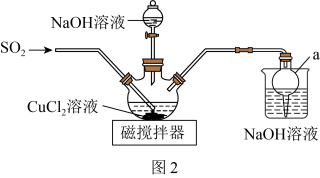
 的作用是
的作用是②三颈烧瓶中反应的化学方程式为
(3)该实验体现了
 的性质是
的性质是(4)实验表明,将纯净的
 缓缓地通入到
缓缓地通入到 溶液中,得到
溶液中,得到 沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:假设Ⅰ:溶液中的
 ;
;假设Ⅱ:溶解在水中的氧气。
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
实验 | 向 溶液中缓慢通入纯净的 溶液中缓慢通入纯净的 气体 气体 | 假设I成立 | |
实验 | 向 溶液的烧杯中缓慢通入纯净的 溶液的烧杯中缓慢通入纯净的 气体 气体 |
②验证假设Ⅱ。请完成下列表格:
| 实验步骤 | 实验现象 | 实验目的 | |
| 实验iii | 同实验 步骤 步骤 | 同实验 的相关现象 的相关现象 | 作对照实验 |
| 实验iv | 产生白色沉淀 | ||
您最近一年使用:0次
2024-02-23更新
|
668次组卷
|
8卷引用:专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
(已下线)专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)四川省广元市川师大万达中学2023-2024学年高一下学期3月月考化学试题黑龙江省牡丹江市第一高级中学2023-2024学年高一下学期5月期中考试化学试题四川省绵阳中学2023-2024学年高三下学期2月开学考理科综合-高中化学(已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)2024届内蒙古自治区乌海市第六中学高三下学期第三次模拟考试理综试题-高中化学河南省郑州市第五高级中学2023-2024学年高三2月开学考理综试题-高中化学江西省部分学校2023-2024学年高三上学期2月月考化学试题
解题方法
2 . 某化学小组拟设计实验探究SO2与钙盐溶液的反应情况。
【文献资料】
①CaSO3是难溶于水、易溶于盐酸的白色固体;
②实验室用Na2SO3粉末和70%硫酸反应制备SO2;
③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
【设计实验】
实验Ⅰ:探究二氧化硫与氯化钙溶液的反应。
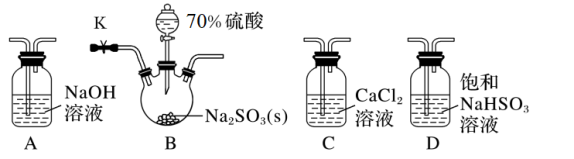
(1)若气体从左至右流动,选择装置并排序为___________ (填字母)。
(2)D装置的作用是___________ (用离子方程式表示)。
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色沉淀是CaSO3;
假设2:白色沉淀是CaSO4;
假设3:白色沉淀是CaSO4和CaSO3。
②乙同学设计实验证明白色沉淀是CaSO4,他的实验方法和现象是___________ 。
③丙同学认为C中生成硫酸钙的原因是装置内O2氧化了SO2。
排除装置内O2干扰采取的措施是:在启动B中反应之前,___________ (填实验步骤),重新实验,C中无明显现象,所以SO2和CaCl2溶液不反应。
实验Ⅱ:探究SO2和Ca(ClO)2溶液的反应。
丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若SO2过量,则发生的反应为Ca(ClO)2+2SO2+2H2O=CaSO4↓+2HCl+H2SO4;
②若SO2少量,则发生的反应为___________ 。
(5)为了探究C中SO2是否过量,戊同学取少量C中上层清液于试管中,加入下列物质可以达到实验目的的是___________ (填字母)。
a.NaHCO3溶液
b.品红溶液
c.AgNO3溶液
d.紫色石蕊溶液
【文献资料】
①CaSO3是难溶于水、易溶于盐酸的白色固体;
②实验室用Na2SO3粉末和70%硫酸反应制备SO2;
③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
【设计实验】
实验Ⅰ:探究二氧化硫与氯化钙溶液的反应。

(1)若气体从左至右流动,选择装置并排序为
(2)D装置的作用是
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色沉淀是CaSO3;
假设2:白色沉淀是CaSO4;
假设3:白色沉淀是CaSO4和CaSO3。
②乙同学设计实验证明白色沉淀是CaSO4,他的实验方法和现象是
③丙同学认为C中生成硫酸钙的原因是装置内O2氧化了SO2。
排除装置内O2干扰采取的措施是:在启动B中反应之前,
实验Ⅱ:探究SO2和Ca(ClO)2溶液的反应。
丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若SO2过量,则发生的反应为Ca(ClO)2+2SO2+2H2O=CaSO4↓+2HCl+H2SO4;
②若SO2少量,则发生的反应为
(5)为了探究C中SO2是否过量,戊同学取少量C中上层清液于试管中,加入下列物质可以达到实验目的的是
a.NaHCO3溶液
b.品红溶液
c.AgNO3溶液
d.紫色石蕊溶液
您最近一年使用:0次
名校
解题方法
3 . 如图所示,某同学利用Na2SO3和浓H2SO4制取SO2并探究其性质。
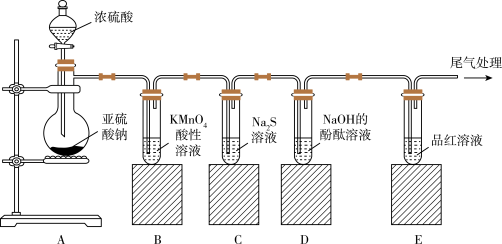
(1)装置C中的实验现象是___ ,该实验现象说明SO2具有___ 性。
(2)能验证SO2具有酸性氧化物的通性的实验现象是___ 。
(3)探究H2SO3的酸性强于HClO,该同学用如图所示装置达成实验目的。
A.小苏打溶液
B.品红溶液
C.酸性KMnO4溶液
D.漂白粉溶液
①装置的连接顺序为纯净SO2→___ (选填字母)
②可证明H2SO3的酸性强于HClO的实验现象是__

(1)装置C中的实验现象是
(2)能验证SO2具有酸性氧化物的通性的实验现象是
(3)探究H2SO3的酸性强于HClO,该同学用如图所示装置达成实验目的。
A.小苏打溶液

B.品红溶液

C.酸性KMnO4溶液

D.漂白粉溶液

①装置的连接顺序为纯净SO2→
②可证明H2SO3的酸性强于HClO的实验现象是
您最近一年使用:0次
2021-04-30更新
|
257次组卷
|
3卷引用:湖南省娄底市第一中学2020-2021学年高一下学期期中考试化学(高考班)试题
湖南省娄底市第一中学2020-2021学年高一下学期期中考试化学(高考班)试题(已下线)专题01 硫及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)湖南省常德市一中2020-2021学年高一下学期期中考试化学试题
4 . 在实验过程中,若一种气体极易溶于一种液体,则容易发生倒吸现象,给实验造成危险。现有4位同学分别设计了一个实验,希望通过观察到的明显现象来说明二氧化碳极易溶于氢氧化钠溶液,设计的装置如下:

其中一位同学向充满二氧化碳的塑料瓶D中加入氢氧化钠溶液,盖紧瓶塞后振荡,如果看到瓶子变瘪了,说明二氧化碳与氢氧化钠溶液发生了反应。对装置A~C,将能达到实验目的的装置、操作方法和实验现象填入下表(可不填满):
_______________________________

其中一位同学向充满二氧化碳的塑料瓶D中加入氢氧化钠溶液,盖紧瓶塞后振荡,如果看到瓶子变瘪了,说明二氧化碳与氢氧化钠溶液发生了反应。对装置A~C,将能达到实验目的的装置、操作方法和实验现象填入下表(可不填满):
| 所选装置 | 操作方法 | 实验现象 |
您最近一年使用:0次
2020-01-29更新
|
94次组卷
|
2卷引用:2020年春季人教版高中化学必修1第三章《金属及其化合物》测试卷
5 . 某课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,采用了不同的实验方法(装置如图所示)。
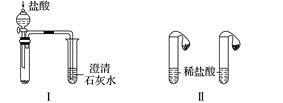
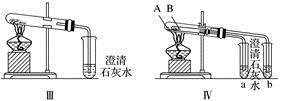
(1)根据上图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)____ 。
(2)图Ⅲ所示实验能够鉴别这两种物质,其反应的化学方程式为_______ 。
(3)图Ⅳ不仅能鉴别碳酸钠和碳酸氢钠,同时又能验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的物质为__________ ,实验过程中的现象为________ 。


(1)根据上图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)
(2)图Ⅲ所示实验能够鉴别这两种物质,其反应的化学方程式为
(3)图Ⅳ不仅能鉴别碳酸钠和碳酸氢钠,同时又能验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的物质为
您最近一年使用:0次
2018-12-22更新
|
165次组卷
|
3卷引用:贵州省息烽县一中2018-2019学年高一上学期期中考试化学试题
6 . 已知 ,某同学认为钠和
,某同学认为钠和 也可以发生类似的反应,他在实验室中选择如图所示的装置对钠与
也可以发生类似的反应,他在实验室中选择如图所示的装置对钠与 的反应进行了实验探究。依据要求回答问题:
的反应进行了实验探究。依据要求回答问题:
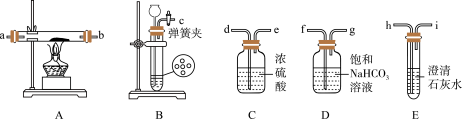
(1)实验室制备 的化学反应方程式为
的化学反应方程式为________
(2)为达到实验目的,题图装置的连接顺序为c→_______
(3)装置气密性良好,装好药品后打开弹簧夹,待装置中的空气排尽后点燃酒精灯。能说明装置中空气已经排尽的现象是____________
(4)该同学用稀盐酸与 反应制备
反应制备 ,向装置B中加入稀盐酸后,发现
,向装置B中加入稀盐酸后,发现 与稀盐酸没有接触。由于稀盐酸已经用完,为使反应顺利进行可再加入的试剂是
与稀盐酸没有接触。由于稀盐酸已经用完,为使反应顺利进行可再加入的试剂是______
A 稀硝酸 B 溶液 C 苯 D
溶液 C 苯 D 
(5)若反应过程中 足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:
足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:
①生成的固体物质为
②生成的固体物质为 和C的混合物
和C的混合物
③生成的固体物质为 和
和 的混合物
的混合物
④生成的固体物质为 和C的混合物
和C的混合物
该同学报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是________
(6)该同学经过反思,认为上述实验设计中存在缺陷。该缺陷是___________
 ,某同学认为钠和
,某同学认为钠和 也可以发生类似的反应,他在实验室中选择如图所示的装置对钠与
也可以发生类似的反应,他在实验室中选择如图所示的装置对钠与 的反应进行了实验探究。依据要求回答问题:
的反应进行了实验探究。依据要求回答问题:
(1)实验室制备
 的化学反应方程式为
的化学反应方程式为(2)为达到实验目的,题图装置的连接顺序为c→
(3)装置气密性良好,装好药品后打开弹簧夹,待装置中的空气排尽后点燃酒精灯。能说明装置中空气已经排尽的现象是
(4)该同学用稀盐酸与
 反应制备
反应制备 ,向装置B中加入稀盐酸后,发现
,向装置B中加入稀盐酸后,发现 与稀盐酸没有接触。由于稀盐酸已经用完,为使反应顺利进行可再加入的试剂是
与稀盐酸没有接触。由于稀盐酸已经用完,为使反应顺利进行可再加入的试剂是A 稀硝酸 B
 溶液 C 苯 D
溶液 C 苯 D 
(5)若反应过程中
 足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:
足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为

②生成的固体物质为
 和C的混合物
和C的混合物③生成的固体物质为
 和
和 的混合物
的混合物④生成的固体物质为
 和C的混合物
和C的混合物该同学报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是
(6)该同学经过反思,认为上述实验设计中存在缺陷。该缺陷是
您最近一年使用:0次
7 . 甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮、一氧化氮生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。
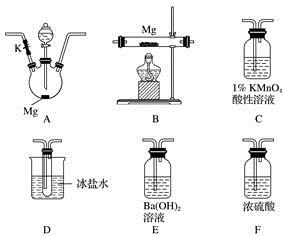
(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是________________________________ 。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→____________ →E,确定还原产物中有二氧化氮的现象是______________________________________ ,实验中要多次使用装置F,第二次使用F的目的是______________________________________________ 。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:________________________________ 。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是______________________________________ 。
(5)设计一种实验方案,验证镁与硝酸反应时确实有氮气生成:__________________________ 。
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。

(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是
(5)设计一种实验方案,验证镁与硝酸反应时确实有氮气生成:
您最近一年使用:0次
2016-12-09更新
|
1389次组卷
|
10卷引用:2015-2016学年江苏省扬州中学高一下期中化学试卷
2015-2016学年江苏省扬州中学高一下期中化学试卷(已下线)同步君 必修1 第4章 第4节 硝酸高中化学人教版 必修1 第四章 非金属及其化合物 4.氨 硫酸 硝酸 硝酸辽宁省沈阳市第一二〇中学2021-2022学年高一下学期线上教学质量检测期中考试化学试题云南省元江县一中2018-2019学年高一上学期12月考试化学试题贵州省剑河县二中2018-2019学年高一上学期期末考试化学试题内蒙古集宁一中2019-2020学年高二下学期第二次月考化学试题山西省忻州市静乐县第一中学2019-2020学年高二下学期第一次月考化学试题云南省玉溪市通海二中2020-2021学年高一下学期期中考试化学试题2016届湖北省沙市中学高三下第一次半月考理综化学试卷
18-19高一·全国·假期作业
8 . 下列装置能达到实验目的的是 ( )
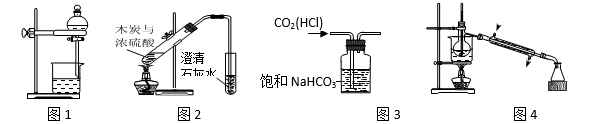

| A.图1用于分离酒精和水 |
B.图2用于验证木炭与浓硫酸的反应产物中含有CO2 (已知:C+2H2SO4(浓) 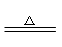 CO2↑+2SO2↑+2H2O,SO2能使澄清石灰水变浑浊) CO2↑+2SO2↑+2H2O,SO2能使澄清石灰水变浑浊) |
| C.图3用于除去CO2中的少量HCl |
| D.图4用于制备蒸馏水 |
您最近一年使用:0次
9 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO。已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。
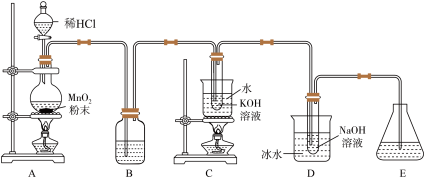
回答下列问题:
(1)试验中盛放MnO2粉末的装置名称是___________ 。
(2)装置A中产生氯气的化学方程式是___________ 。
(3)装置D中发生反应的离子反应式是___________ 。
(4)装置D中冰水的作用是___________ 。
(5)在下列试剂中可选用加入装置E的最佳试剂是___________(填标号)。
(6)探究KClO3、NaClO的氧化能力
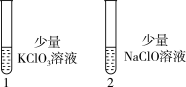
操作:向1号和2号试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3___________ NaClO。(填“大于”或“小于”)

回答下列问题:
(1)试验中盛放MnO2粉末的装置名称是
(2)装置A中产生氯气的化学方程式是
(3)装置D中发生反应的离子反应式是
(4)装置D中冰水的作用是
(5)在下列试剂中可选用加入装置E的最佳试剂是___________(填标号)。
| A.KI溶液 | B.饱和食盐水 | C. 溶液 溶液 | D.浓 |

操作:向1号和2号试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3
您最近一年使用:0次
2023-05-21更新
|
405次组卷
|
3卷引用:【精品卷】2.2.2 氯气的制法课堂例题-人教版2023-2024学年必修第一册
(已下线)【精品卷】2.2.2 氯气的制法课堂例题-人教版2023-2024学年必修第一册浙江省金华十校2022-2023学年高一上学期期末调研模拟考试化学试题浙江省金华市十校2022-2023学年高一下学期期末调研考试化学试题
10 . 已知 易溶于水和乙醇。某实验小组用如下装置制备
易溶于水和乙醇。某实验小组用如下装置制备 并探究其性质。装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入
并探究其性质。装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入 浓硫酸,充分反应直至装置A中反应停止。回答下列问题:
浓硫酸,充分反应直至装置A中反应停止。回答下列问题:
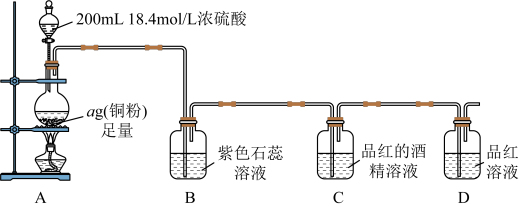
(1)盛装浓硫酸仪器的名称是___________ 。
(2)写出装置A中发生反应的化学方程式为___________ 。
(3)根据装置C、D的现象,可以得出的结论是___________ 。
(4)使品红褪色的主要微粒可能有___________ ;根据提出假设,设计对照验证实验。实验过程中除温度外,还需要控制的变量有___________ (写出两点即可)
 易溶于水和乙醇。某实验小组用如下装置制备
易溶于水和乙醇。某实验小组用如下装置制备 并探究其性质。装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入
并探究其性质。装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入 浓硫酸,充分反应直至装置A中反应停止。回答下列问题:
浓硫酸,充分反应直至装置A中反应停止。回答下列问题:
(1)盛装浓硫酸仪器的名称是
(2)写出装置A中发生反应的化学方程式为
(3)根据装置C、D的现象,可以得出的结论是
(4)使品红褪色的主要微粒可能有
您最近一年使用:0次



