名校
1 . 化学在生活中有着广泛的应用,下列对应关系正确的是
| 选项 | 化学性质 | 实际应用 |
| A | FeCl3溶液显酸性 | 脱除燃气中H2S |
| B | Na2S溶液显碱性 | 去除废水中Cu2+,Hg2+ 等 |
| C | 活性炭具有还原性 | 用作自来水的净化剂 |
| D | NaClO2具有氧化性 | 脱除烟气中的SO2及NOx |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-06-26更新
|
351次组卷
|
5卷引用:辽宁省名校2022届高三第二次联合考试化学试题
辽宁省名校2022届高三第二次联合考试化学试题【全国百强校】山西省忻州市第一中学2018-2019学年高二下学期第三次月考化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题01-2020年北京新高考化学模拟试题广东省广州市天河中学2021届高三上学期1月月考化学试题黑龙江省绥化市高中联盟校联合考试2021-2022学年高三上学期12月月考化学试题
2 . 化学在生活中有着广泛的应用。下列对应关系错误的是
| 选项 | 化学性质 | 实际应用 |
| A | ClO2具有强氧化性 | 自来水消毒杀菌 |
| B | SO2具有还原性 | 用作漂白剂 |
| C | NaHCO3受热分解并且生成气体 | 焙制糕点 |
| D | Al(OH)3分解吸收大量热量并有H2O生成 | 阻燃胶合板 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-03-26更新
|
136次组卷
|
6卷引用:辽宁师范大学附属中学2019-2020学年高二下学期期末考试化学试题
3 . 二氧化硫和亚硫酸在工农业生产中具有重要的用途。某化学兴趣小组对SO2和H2SO3的一些性质进行了探究。回答下列问题:
I.探究SO2性质
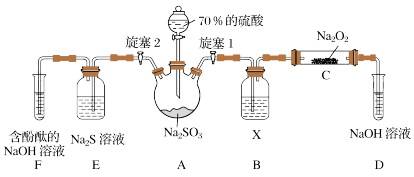
(1)装置B中试剂X是______ 。
(2)关闭旋塞1后,打开旋塞2,装置E中的Na2S溶液用于验证SO2的______ 性,F中的现象______ 。
(3)推测C中固体产物的成分,并写出固体产物中含有的阴离子的检验方法:______ 。
II.探究H2SO3的酸性强于HClO(可能所需要的装置和试剂如图所示)。
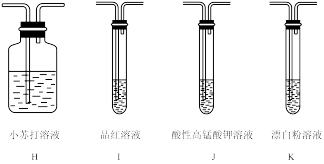
(4)所需装置的连接顺序为:纯净的SO2→______→_______→______→______,______ (填装置标号),装置K中反应的离子方程式为______ 。
(5)能证明H2SO3的酸性强于HClO的现象______ 。
I.探究SO2性质

(1)装置B中试剂X是
(2)关闭旋塞1后,打开旋塞2,装置E中的Na2S溶液用于验证SO2的
(3)推测C中固体产物的成分,并写出固体产物中含有的阴离子的检验方法:
II.探究H2SO3的酸性强于HClO(可能所需要的装置和试剂如图所示)。

(4)所需装置的连接顺序为:纯净的SO2→______→_______→______→______,
(5)能证明H2SO3的酸性强于HClO的现象
您最近一年使用:0次
名校
解题方法
4 . 二氧化硫和亚硫酸在工农业生产中具有重要的用途。某化学兴趣小组对 和
和 的一些性质进行了探究。回答下列问题:
的一些性质进行了探究。回答下列问题:
Ⅰ.某同学设计了如图装置用于制取 和验证
和验证 的性质。
的性质。 具有一定氧化性。
具有一定氧化性。
(1)装置A中发生反应的化学方程式为___________ 。
(2)在框图内选择合适装置依次验证 的漂白性、酸性、还原性,上图各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上图各装置按气流从左到右方向连接顺序为A→___________ (填装置字母,还原性设计两个装置)。
(3)实验前必须鼓入 ,目的是
,目的是___________ 。
(4)装置F中产生了白色沉淀,其成分是___________ (化学式)。
(5)实验中发现装置A中 可能部分被氧化,现需测定
可能部分被氧化,现需测定 的纯度:称取
的纯度:称取 样品,配成
样品,配成 溶液;取其中的
溶液;取其中的 溶液,与
溶液,与 酸性
酸性 溶液发生以下反应:
溶液发生以下反应: ,实验消耗
,实验消耗 溶液
溶液 ,以上样品中
,以上样品中 的质量分数为
的质量分数为___________ (保留三位有效数字)。
Ⅱ.探究 的酸性强于
的酸性强于 (可能所需要的装置和试剂如图所示)。
(可能所需要的装置和试剂如图所示)。___________ (填装置标号)。
(7)能证明 的酸性强于
的酸性强于 的现象
的现象___________ 。
 和
和 的一些性质进行了探究。回答下列问题:
的一些性质进行了探究。回答下列问题:Ⅰ.某同学设计了如图装置用于制取
 和验证
和验证 的性质。
的性质。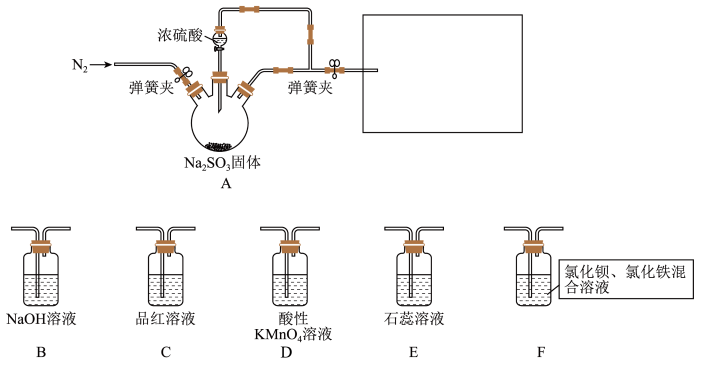
 具有一定氧化性。
具有一定氧化性。(1)装置A中发生反应的化学方程式为
(2)在框图内选择合适装置依次验证
 的漂白性、酸性、还原性,上图各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上图各装置按气流从左到右方向连接顺序为A→(3)实验前必须鼓入
 ,目的是
,目的是(4)装置F中产生了白色沉淀,其成分是
(5)实验中发现装置A中
 可能部分被氧化,现需测定
可能部分被氧化,现需测定 的纯度:称取
的纯度:称取 样品,配成
样品,配成 溶液;取其中的
溶液;取其中的 溶液,与
溶液,与 酸性
酸性 溶液发生以下反应:
溶液发生以下反应: ,实验消耗
,实验消耗 溶液
溶液 ,以上样品中
,以上样品中 的质量分数为
的质量分数为Ⅱ.探究
 的酸性强于
的酸性强于 (可能所需要的装置和试剂如图所示)。
(可能所需要的装置和试剂如图所示)。
(7)能证明
 的酸性强于
的酸性强于 的现象
的现象
您最近一年使用:0次
5 . 氯化铁溶液在科学研究和生产生活中有较多用途。
Ⅰ.向氯化铁溶液中滴加几滴KSCN溶液后,滴加H2O2溶液,红色褪去。已知红色褪去的同时有气体生成,经检验为O2,小组同学对红色褪去的原因提出了三种假设:
(1)假设I:H2O2还原Fe3+,使其转变为Fe2+;
假设II:H2O2分解生成O2,O2氧化KSCN;
假设Ⅲ:___________ 。
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加KSCN溶液,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
实验②:另取同浓度的FeCl3溶液滴加2滴KSCN溶液,溶液变红,再通入O2,无明显变化。
实验结论:实验①说明假设_____ 不正确;实验②的目的是______ ;由实验①②得出假设______ 是正确的。
Ⅱ.用覆铜板制作印刷电路板时,常用FeCl3溶液作腐蚀液。某化学兴趣小组在实验室进行了模拟实验。
【实验I】向盛有10mL2mol/LFeCl3溶液的试管中,加入一块铜片(Cu过量),反应一段时间后,溶液黄色褪去。
(2)用离子方程式解释溶液黄色褪去的原因_________ 。
【实验Ⅱ】为验证上述实验中Fe3+是否完全反应,该小组同学取上层清液于另一支试管中,滴入3滴0.1mol/LKSCN溶液。结果发现,上层清液中立即产生白色沉淀,同时滴入处局部出现红色,振荡后红色立即消失。
【查阅资料】为解释该现象产生的原因,同学们查阅资料得知:
①(SCN)2与卤素单质(Cl2、Br2、I2)的化学性质相似,氧化性介于溴单质和碘单质之间,且浓度越大氧化性越强;
② ;
;
③CuSCN为白色固体,几乎不溶于水。
【实验Ⅲ】为探究白色沉淀产生的原因,同学们设计了如下实验。填写实验方案:
(3)步骤2中取CuCl2溶液的浓度为_____ mol/L。
【分析解释】
(4)实验Ⅱ中白色沉淀的成分是___________ (填化学式)。
(5)根据资料,结合产生白色沉淀的离子方程式,解释实验Ⅱ中“滴入KSCN溶液处局部出现红色”的原因。①产生白色沉淀的离子方程式:___________ ;②局部出现红色的原因:___________ 。
Ⅰ.向氯化铁溶液中滴加几滴KSCN溶液后,滴加H2O2溶液,红色褪去。已知红色褪去的同时有气体生成,经检验为O2,小组同学对红色褪去的原因提出了三种假设:
(1)假设I:H2O2还原Fe3+,使其转变为Fe2+;
假设II:H2O2分解生成O2,O2氧化KSCN;
假设Ⅲ:
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加KSCN溶液,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
实验②:另取同浓度的FeCl3溶液滴加2滴KSCN溶液,溶液变红,再通入O2,无明显变化。
实验结论:实验①说明假设
Ⅱ.用覆铜板制作印刷电路板时,常用FeCl3溶液作腐蚀液。某化学兴趣小组在实验室进行了模拟实验。
【实验I】向盛有10mL2mol/LFeCl3溶液的试管中,加入一块铜片(Cu过量),反应一段时间后,溶液黄色褪去。
(2)用离子方程式解释溶液黄色褪去的原因
【实验Ⅱ】为验证上述实验中Fe3+是否完全反应,该小组同学取上层清液于另一支试管中,滴入3滴0.1mol/LKSCN溶液。结果发现,上层清液中立即产生白色沉淀,同时滴入处局部出现红色,振荡后红色立即消失。
【查阅资料】为解释该现象产生的原因,同学们查阅资料得知:
①(SCN)2与卤素单质(Cl2、Br2、I2)的化学性质相似,氧化性介于溴单质和碘单质之间,且浓度越大氧化性越强;
②
 ;
;③CuSCN为白色固体,几乎不溶于水。
【实验Ⅲ】为探究白色沉淀产生的原因,同学们设计了如下实验。填写实验方案:
| 实验方案 | 现象 |
| 步骤1:取10mL2mol/L的FeCl2溶液,滴加3滴0.1mol/L的KSCN溶液 | 无明显现象 |
| 步骤2:取10mL_____mol/L的CuCl2溶液,滴加3滴0.1mol/L的KSCN溶液 | 产生白色沉淀 |
【分析解释】
(4)实验Ⅱ中白色沉淀的成分是
(5)根据资料,结合产生白色沉淀的离子方程式,解释实验Ⅱ中“滴入KSCN溶液处局部出现红色”的原因。①产生白色沉淀的离子方程式:
您最近一年使用:0次
6 . 某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。[制取氨气的反应原理:2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+2H2O ]
CaCl2 + 2NH3↑+2H2O ]
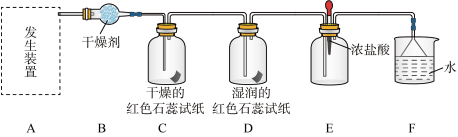
【实验探究】
(1)利用上述原理,实验室制取氨气应选用下图中________ 发生装置进行实验。
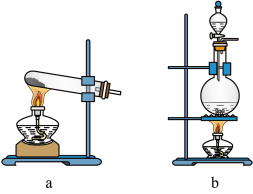
(2)B装置中的干燥剂可选用________ 。
(3)用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为________ L。(NH4Cl的摩尔质量为53.5g·mol—1)
(4)气体通过C、D装置时,试纸颜色会发生变化的是____ (填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_______ 。
(6)F装置中倒置漏斗的作用_______ 。
【拓展应用】
(7)某同学用如图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有________ 性质(填序号)。
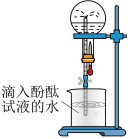
a 还原性 b 极易溶于水 c 与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮:8NH3 + 6NO2 =7N2 + 12H2O
该反应中氨气体现________ (填“氧化性”或“还原性”)。请你列举出氨气的另一种用途________ 。
 CaCl2 + 2NH3↑+2H2O ]
CaCl2 + 2NH3↑+2H2O ]
【实验探究】
(1)利用上述原理,实验室制取氨气应选用下图中

(2)B装置中的干燥剂可选用
(3)用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为
(4)气体通过C、D装置时,试纸颜色会发生变化的是
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(6)F装置中倒置漏斗的作用
【拓展应用】
(7)某同学用如图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有

a 还原性 b 极易溶于水 c 与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮:8NH3 + 6NO2 =7N2 + 12H2O
该反应中氨气体现
您最近一年使用:0次
2020-06-09更新
|
180次组卷
|
6卷引用:辽宁省铁岭市开原市第二高级中学2021届高三第二次模拟考试化学试题
7 . 绿矾(FeSO4·xH2O)是生血片的主要成分,某研究性学习小组拟对绿矾热分解产物进行探究,
【实验猜想】绿帆分解可能生成Fe、FeO、Fe2O3、SO3、SO2或H2O等。
【实验探究】该小组用如图所示装贸进行实验(夹持仪器略)

回答下列问题:
(1)为保证实验结果的准确性,点燃灯之前的关键操作:________________________ 。(注:气密性已检验完)
(2)【实验现象】
A中固体变红色,B中无水CuS04_________ ,C中蓝色石蕊试纸_________ 。D中产生白色沉淀。
(3)反应结束后,取A中固体继续进行实验,实验的操作及现象如下:
①向固体样品中加入过量稀硫酸,固体完全溶解,且无气体放出;
②取①中溶液滴入少量铁氰化钾溶液,无明显现象;
③另取①中溶液,并向其中滴入KSCN溶液,溶液变红。
由此得出结论:红色固体为______________________ (写化学式),该物质的常见用途:_________ 。
(4)D中白色沉淀的成分:_______________________ (写化学式),有同学认为还应该增加一个实验:取D中沉淀,加入一定量的盐酸以确定其组成,事实上不需要再进行实验也可以确定沉淀成分,请说明理由:____________________ 。
【实验拓展】
(5)测定绿矾中结晶水的含量:该小组同学设计如下实验步骤:
Ⅰ.准确称量27.8g绿矾样品,配成250 mL溶液后量取25.00mL所配制的溶液于锥形瓶中;
Ⅱ.用硫酸酸化的0.100 0mol·L-1KMn04溶液滴定至终点;
Ⅲ.重复操作3次,消耗KMn04溶液的体积分别为20.02mL、24.98mL、19.98 mL。
①根据以上数据,计算绿矾化学式中结晶水数目x=______________________________ 。
②下列情况会使测得的x偏小的是______________________________ 。
a.开始读数时滴定管尖嘴有气泡而终点时无气泡
b.样品失去部分结晶水
C.量取待测液前未用待测液润洗滴定管
d.滴定开始时平视
【实验结论】
(6)FeS04·xH20的分解的化学方程式为:_____________________________________________ 。
【实验猜想】绿帆分解可能生成Fe、FeO、Fe2O3、SO3、SO2或H2O等。
【实验探究】该小组用如图所示装贸进行实验(夹持仪器略)

回答下列问题:
(1)为保证实验结果的准确性,点燃灯之前的关键操作:
(2)【实验现象】
A中固体变红色,B中无水CuS04
(3)反应结束后,取A中固体继续进行实验,实验的操作及现象如下:
①向固体样品中加入过量稀硫酸,固体完全溶解,且无气体放出;
②取①中溶液滴入少量铁氰化钾溶液,无明显现象;
③另取①中溶液,并向其中滴入KSCN溶液,溶液变红。
由此得出结论:红色固体为
(4)D中白色沉淀的成分:
【实验拓展】
(5)测定绿矾中结晶水的含量:该小组同学设计如下实验步骤:
Ⅰ.准确称量27.8g绿矾样品,配成250 mL溶液后量取25.00mL所配制的溶液于锥形瓶中;
Ⅱ.用硫酸酸化的0.100 0mol·L-1KMn04溶液滴定至终点;
Ⅲ.重复操作3次,消耗KMn04溶液的体积分别为20.02mL、24.98mL、19.98 mL。
①根据以上数据,计算绿矾化学式中结晶水数目x=
②下列情况会使测得的x偏小的是
a.开始读数时滴定管尖嘴有气泡而终点时无气泡
b.样品失去部分结晶水
C.量取待测液前未用待测液润洗滴定管
d.滴定开始时平视
【实验结论】
(6)FeS04·xH20的分解的化学方程式为:
您最近一年使用:0次
名校
8 . 绿矾是含有一定量结晶水的硫酸亚铁(FeSO4·XH2O),在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________ 、_______________ 。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。
①仪器B的名称是____________________ 。
②将下列实验操作步骤正确排序___________________ (填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________ (列式表示)。若实验时按a、d次序操作,则使x__________ (填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。C、D中的溶液依次为BaCl2溶液、浓H2SO4。C、D中有气泡冒出,并可观察到的现象分别为产生白色沉淀、品红溶液褪色。写出硫酸亚铁高温分解反应的化学方程式_____________________ 。
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。
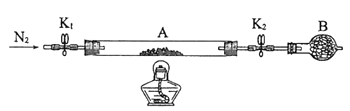
①仪器B的名称是
②将下列实验操作步骤正确排序
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。C、D中的溶液依次为BaCl2溶液、浓H2SO4。C、D中有气泡冒出,并可观察到的现象分别为产生白色沉淀、品红溶液褪色。写出硫酸亚铁高温分解反应的化学方程式
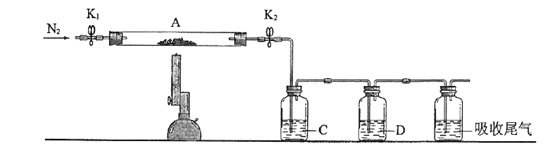
您最近一年使用:0次
2018-08-21更新
|
245次组卷
|
3卷引用:辽宁省葫芦岛市第六中学2019届高三上学期9月化学练习题
名校
解题方法
9 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)如何检验绿矾晶体中Fe2+是否被氧化?_______________________________
(2)已知本实验所用绿矾晶体没有被氧化。为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2) (设为装置A) 称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。
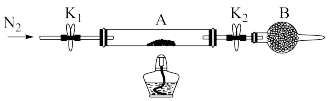
①将下列实验操作步骤正确排序__________ (填标号);重复上述操作步骤,直至装置A恒重,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量装置A的质量 f.冷却到室温
②根据实验记录,计算绿矾化学式中结晶水数目x=_____________ (列式表示) 。若实验时按a、d次序操作,则使x_____________ (填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2) 中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为__________ (填标号)。C、D中有气泡冒出,并可观察到的现象分别为_____________ 。
A.品红 B.NaOH C.BaCl2 D.Ba(NO3)2 E.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_______________ 。
(4)绿矾溶液在空气中久置出现红褐色沉淀,写出相关的离子方程式____________________ 。
(1)如何检验绿矾晶体中Fe2+是否被氧化?
(2)已知本实验所用绿矾晶体没有被氧化。为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2) (设为装置A) 称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。
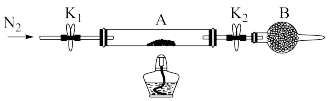
①将下列实验操作步骤正确排序
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量装置A的质量 f.冷却到室温
②根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁的分解产物,将(2) 中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为
A.品红 B.NaOH C.BaCl2 D.Ba(NO3)2 E.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式
(4)绿矾溶液在空气中久置出现红褐色沉淀,写出相关的离子方程式
您最近一年使用:0次
名校
10 . I.高锰酸钾在实验室和工农业生产中有广泛的用途,实验室以二氧化锰为主要原料制备高锰酸钾,其部分流程如下:
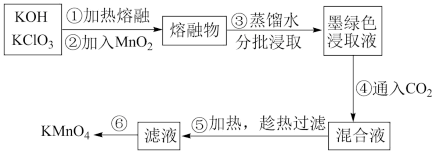
(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是_______ (用化学方程式表示)。
(2)第④步通入适量CO2,发生反应生成 、MnO2和碳酸盐,则发生反应的离子方程式为
、MnO2和碳酸盐,则发生反应的离子方程式为____ 。
(3)第⑥步加热浓缩至液面有细小晶体析出时,停止加热,冷却结晶、过滤、洗涤、干燥,干燥过程中,温度不宜过高,其原因是_______ (用化学方程式表)。
(4)H2O2和KMnO4都是常用的强氧化剂,若向H2O2溶液中滴加酸性高锰酸钾溶液,则酸性高锰酸钾溶液会褪色,写出该反应的离子方程式:_____ 。
II.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和C12的性质。
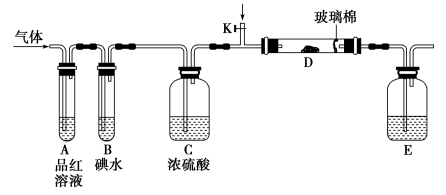
(5)若从左端分别通入SO2和C12,装置A中观察到的现象是否相同_______ (填“相同”或“不相同”)。
(6)若装置B中装有5.0mL1.0mol•L-1的碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2mol电子,则该反应的化学方程式为_____ 。
(7)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含有X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含有X的溶液反应的离子方程式:_______ 。

(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是
(2)第④步通入适量CO2,发生反应生成
 、MnO2和碳酸盐,则发生反应的离子方程式为
、MnO2和碳酸盐,则发生反应的离子方程式为(3)第⑥步加热浓缩至液面有细小晶体析出时,停止加热,冷却结晶、过滤、洗涤、干燥,干燥过程中,温度不宜过高,其原因是
(4)H2O2和KMnO4都是常用的强氧化剂,若向H2O2溶液中滴加酸性高锰酸钾溶液,则酸性高锰酸钾溶液会褪色,写出该反应的离子方程式:
II.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和C12的性质。

(5)若从左端分别通入SO2和C12,装置A中观察到的现象是否相同
(6)若装置B中装有5.0mL1.0mol•L-1的碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2mol电子,则该反应的化学方程式为
(7)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含有X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含有X的溶液反应的离子方程式:
您最近一年使用:0次
2016-12-09更新
|
1025次组卷
|
5卷引用:辽宁省铁岭市六校协作体2020届高三第二次联考化学试题



