20. 已知硫酸亚铁铵[(NH
4)
2SO
4·FeSO
4·6H
2O](俗称莫尔盐)可溶于水,在100℃~110℃时分解。为探究其化学性质,甲、乙两同学设计了如下实验。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验,装置C中可观察到的现象是
____________________,由此可知分解产物中有
_________。
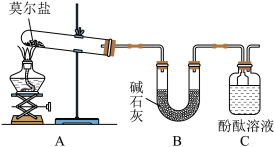
乙同学认为莫尔盐晶体分解的产物中还可能含有SO
3(g)、SO
2(g)及N
2(g)。为验证产物的存在,用下列装置进行实验。
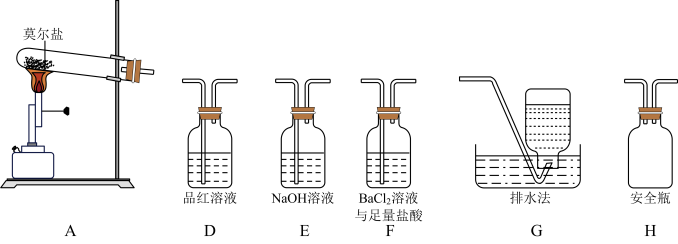
(2)乙同学的实验中,装置依次连接的合理顺序为:A→H→
( )→
( )→
( )→G。
(3)证明含有SO
3的实验现象是
______________;安全瓶H的作用是
_________。
Ⅱ.为测定硫酸亚铁铵纯度,称取m g莫尔盐样品,配成500 mL溶液。甲、乙两位同学设计了如下两个实验方案。
甲方案:取25.00 mL样品溶液用0.1000 mol·L
-1的酸性K
2Cr
2O
7 溶液分三次进行滴定。
乙方案:(通过NH

测定)实验设计装置如下图所示。取25.00 mL样品溶液进行该实验。
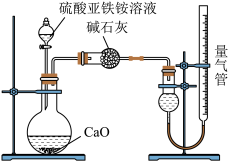
请回答:
(4)甲方案中的离子方程式为:
________________。
(5)乙方案中量气管中最佳试剂是
________a 水
b 饱和NaHCO
3溶液 c CCl
4(6)若测得NH
3为V L(已折算为标准状况下),则硫酸亚铁铵纯度为
_____(列出计算式)。