名校
1 . 某课外活动小组设计实验验证二氧化碳跟过氧化钠反应时需要与水接触。下列说法中正确的是
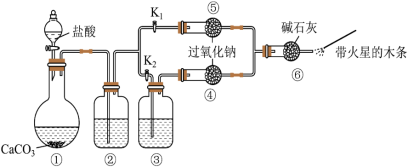

| A.装置①中盐酸不能换成硫酸 |
B.装置②中的试剂是饱和 溶液 溶液 |
C.打开弹簧夹 ,关闭 ,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 |
| D.上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应 |
您最近一年使用:0次
2022-12-07更新
|
193次组卷
|
2卷引用:吉林省延边州2022-2023学年高一上学期期末学业质量检测化学试题
名校
2 . 用如图所示实验装置进行相关实验探究,下列说法不合理的是

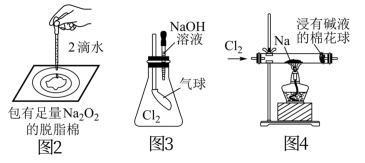


| A.图1若二氧化锰过量,则浓盐酸可全部反应完 |
| B.图2证明Na2O2与水反应放热 |
| C.图3证明Cl2能与烧碱溶液反应 |
| D.图4探究钠与Cl2反应 |
您最近一年使用:0次
2022-01-05更新
|
289次组卷
|
2卷引用:吉林省吉林松花江中学2022-2023学年高一上学期1月期末考试化学试题
3 . 有关如图实验的说法正确的是( )
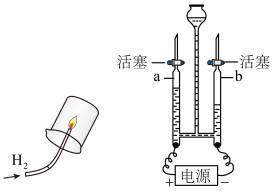

| A.点燃氢气前不用检验纯度 |
| B.干冷烧杯内壁无明显变化 |
| C.b管气体能使带火星木条复燃 |
| D.两个实验均可证明水的组成 |
您最近一年使用:0次
2020-08-06更新
|
34次组卷
|
2卷引用:吉林省农安县哈拉海中学2019-2020学年高一上学期开学考试化学试题
4 . 为研究铜与浓硫酸的反应,实验小组同学进行如图实验,下列说法错误的是

| A.F中可以盛放酸性KMnO4溶液 |
| B.为确认有硫酸铜生成,可向反应后的A中加水 |
| C.此实验设计不能排除浓硫酸中的水是否影响B装置现象的判断 |
| D.可通过D中固体不变色而E中溶液褪色的现象证明浓硫酸中硫元素的氧化性强于氢元素 |
您最近一年使用:0次
2020-05-17更新
|
186次组卷
|
5卷引用:吉林省汪清县第四中学2020-2021学年高一下学期第一次阶段考试化学试题
5 . 关于下列实验装置或操作的说法中,正确的是


| A.①实验室用MnO2固体与浓盐酸共热,制取并收集干燥、纯净的Cl2 |
| B.②实验中若左边棉花变橙色,右边棉花变蓝色,则能证明氧化性:Cl2>Br2>I2 |
| C.③实验试管中会生成血红色沉淀 |
| D.用图④操作可提取碘酒中的碘 |
您最近一年使用:0次
2016-12-09更新
|
1761次组卷
|
2卷引用:2014-2015吉林省松原市扶余县一中高一上学期期末化学试卷
6 . 为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中不正确的是
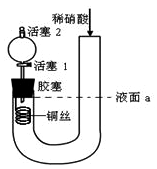

| A.关闭活塞1,加入稀硝酸至液面a处 |
| B.在装置左侧稍加热可以加快稀硝酸与铜的反应速率 |
| C.通过关闭或开启活塞1可以控制反应的进行 |
| D.反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO |
您最近一年使用:0次
2016-12-09更新
|
1695次组卷
|
19卷引用:吉林省延边第二中学2020届高三上学期第一次调研化学试题
吉林省延边第二中学2020届高三上学期第一次调研化学试题(已下线)2011届北京市丰台区高三下学期统一练习(一)(理综)化学部分2014-2015福建省福州市八县高一下学期联考化学试卷2015-2016学年黑龙江省实验中学高二下期末化学试卷上海市格致中学2016-2017学年高一下学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【押题专练】内蒙古赤峰二中2017-2018学年高一上学期期末考试化学试题(已下线)2018年12月12日 《每日一题》人教必修1-硝酸的强氧化性上海市嘉定区2016届高三第一次质量调研化学试题四川省成都龙泉第二中学2021届高三上学期九月月考化学试题浙江省浙北G2(嘉兴一中、湖州中学)2020-2021学年高二上学期期中联考化学试题辽宁省六校2021届高三上学期期中联考化学试题广东省佛山市顺德李兆基中学2020-2021学年高一3月月考化学试卷江苏省苏州市相城区黄埭中学2020-2021学年高一下学期3月月考化学试题黑龙江省哈尔滨市第六中学2020-2021学年高一4月月考化学试题湖北省部分重点高中2020-2021学年高一下学期4月联考化学试题课中-5.2.3 硝酸 酸雨及防治-人教2019必修第二册江苏省盐城市东台创新高级中学2021-2022学年高一5月份月检测化学试题(已下线)3.2.2 铵盐和硝酸-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
名校
7 . 为达到相应实验目的,下列实验操作、 现象正确,并且可行的是
| 编号 | 实验目的 | 实验操作 |
| A | 证明碳酸酸性强于硼酸 | 向饱和碳酸氢钠溶液中滴加少量的硼酸溶液,无气泡产生 |
| B | 检验食品脱氧剂中还原铁粉是否已变质 | 取脱氧剂包装内固体粉末于试管中,加足量稀盐酸溶解,充分反应后滴加KSCN溶液,振荡,观察溶液颜色变化 |
| C | 证明:H2SO3的酸性大于H2S | 向 Na2S溶液中缓缓通入过量SO2,观察到大量臭鸡蛋气味气体逸出 |
| D | 证明Ksp(Mg(OH)2)> Ksp(Fe(OH)3 | 向10ml 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,出现红褐色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 学习小组在实验室中利用下图所示装置制备SO2并进行相关性质的探究。回答下列问题:
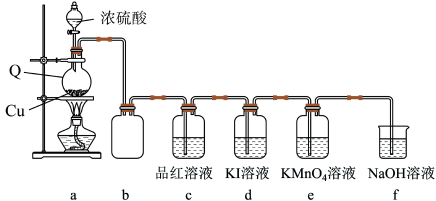
(1)仪器Q的名称为_______ ;装置c中品红溶液褪色,可证明SO2具有_______ 性,装置b的作用是_______ 。
(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是_______ 。
(3)装置a中反应的化学方程式为_______ 。
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O= +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
Ⅰ.取适量装置d中浊液,向其中滴加几滴_______ 溶液(填试剂名称),振荡,无明显变化,浊液中无I2。
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,_______ ,出现白色沉淀,产物溶液中存在 。
。
综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为_______ 。

(1)仪器Q的名称为
(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是
(3)装置a中反应的化学方程式为
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=
 +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。Ⅰ.取适量装置d中浊液,向其中滴加几滴
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,
 。
。综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为
您最近一年使用:0次
2023-01-19更新
|
888次组卷
|
4卷引用:吉林省长春市新解放学校2022-2023学年高一下学期4月月考化学试题
9 . 某研究性学习小组利用如图装置制备 ,并对
,并对 的性质进行探究(装置的气密性已检查)。
的性质进行探究(装置的气密性已检查)。
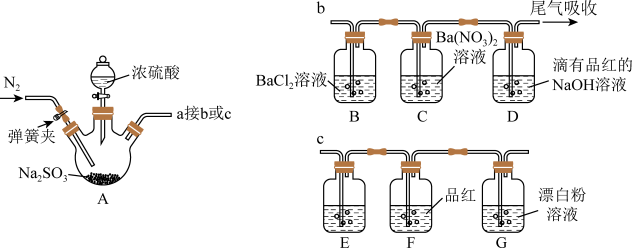
Ⅰ.探究 与可溶性钡的强酸盐是否反应(接口a接b)
与可溶性钡的强酸盐是否反应(接口a接b)
(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间 ,再关闭弹簧夹,此操作的目的是
,再关闭弹簧夹,此操作的目的是_______ 。
(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是_______ ,装置C中反应的离子方程式是_______ 。
(3)装置D中 全部转化为
全部转化为 的离子方程式为:
的离子方程式为:_______ 。
Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是_______
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是_______ ,其作用是_______ ,通过_______ 现象即可证明亚硫酸的酸性强于次氯酸。
 ,并对
,并对 的性质进行探究(装置的气密性已检查)。
的性质进行探究(装置的气密性已检查)。
Ⅰ.探究
 与可溶性钡的强酸盐是否反应(接口a接b)
与可溶性钡的强酸盐是否反应(接口a接b)(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间
 ,再关闭弹簧夹,此操作的目的是
,再关闭弹簧夹,此操作的目的是(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是
(3)装置D中
 全部转化为
全部转化为 的离子方程式为:
的离子方程式为:Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是
您最近一年使用:0次
2022-06-17更新
|
142次组卷
|
2卷引用:吉林省长春外国语学校2023-2024学年高二上学期开学考试化学试题
名校
解题方法
10 . 请用下列装置设计一个实验,证明Cl2的氧化性比I2的氧化性强。
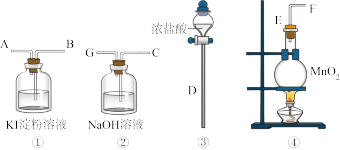
请回答下列问题:
(1)若气流从左到右,则上述仪器的连接顺序为D接E,F接_______ ,________ 接_______ 。若要制得纯净的氯气,则还要先后通过的试剂是_________ ,__________ 。
(2)圆底烧瓶中发生反应的化学方程式为___________ 。
(3)证明Cl2比I2的氧化性强的实验现象是___________ 。
(4)氯气与NaOH溶液反应的离子方程式:________ ,检验Na+的实验名称是_______ ,叙述检验Cl-的操作方法及结论_______ 。

请回答下列问题:
(1)若气流从左到右,则上述仪器的连接顺序为D接E,F接
(2)圆底烧瓶中发生反应的化学方程式为
(3)证明Cl2比I2的氧化性强的实验现象是
(4)氯气与NaOH溶液反应的离子方程式:
您最近一年使用:0次



