1 . 如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网,其右端出气管口放有脱脂棉。
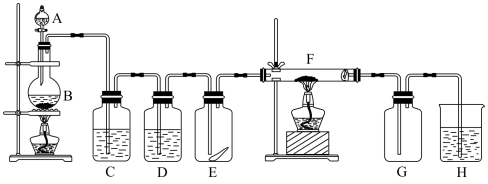
(1)装置C中盛装的溶液是____________ ,D中试剂的作用是________ 。
(2)E中的红色布条是否褪色?____ (填“是”或“否”);写出F中反应的化学反应方程式:________________ ,其反应现象为_____________ 。
(3)新制氯水呈黄绿色说明其中含有_____ ,(填化学式,下同),若将紫色石蕊溶液滴入新制氯水中,可观察到的现象是_________________ ,说明其中含有__________ 。
(4)H中的试剂为___________ ,用来吸收多余氯气。工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白精,该反应的化学方程式为_________________________ 。

(1)装置C中盛装的溶液是
(2)E中的红色布条是否褪色?
(3)新制氯水呈黄绿色说明其中含有
(4)H中的试剂为
您最近一年使用:0次
2020-04-13更新
|
163次组卷
|
5卷引用:吉林省白山市长白县实验中学2019-2020学年高一11月月考化学试题
吉林省白山市长白县实验中学2019-2020学年高一11月月考化学试题河南省南阳市第一中学2019-2020学年高一上学期第一次月考化学试题安徽省滁州市明光中学2019-2020学年高一下学期开学考试化学试题(已下线)专题06 氯及其化合物(核心素养卷)——【新教材精创】2019-2020学年高中化学新教材知识讲学陕西省蓝田县城关中学大学区联考2022-2023学年高一下学期6月期末考试化学试题
2 . 某兴趣小组的同学设计实验制备并探究SO2的性质。回答下列问题:
(1)实验室用废铜屑制备SO2的化学方程式为______ 。
(2)将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有______ 性。
(3)将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为______ 。
(4)将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为______ 。(Cr2O72-被还原为Cr3+)
(5)常温下,改变0.1mol•L-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)=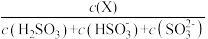 ]随pH的变化如图所示:
]随pH的变化如图所示:
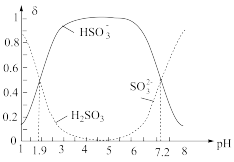
H2SO3的lgKa1=______ ;反应HSO3-+OH- SO32-+H2O的lgK=
SO32-+H2O的lgK=______ ;用0.100mol•L-1NaOH溶液滴入0.100mol•L-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为______ 。
(1)实验室用废铜屑制备SO2的化学方程式为
(2)将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有
(3)将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为
(4)将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为
(5)常温下,改变0.1mol•L-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)=
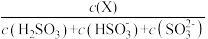 ]随pH的变化如图所示:
]随pH的变化如图所示:
H2SO3的lgKa1=
 SO32-+H2O的lgK=
SO32-+H2O的lgK=
您最近一年使用:0次



