1 . 某校化学兴趣小组为验证 的性质,设计如图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
的性质,设计如图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
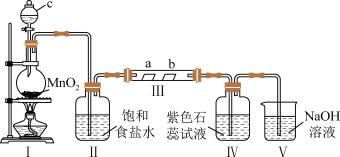
(1)装置I中仪器c的名称是_______ ,实验室用 和浓盐酸制备
和浓盐酸制备 的化学方程式为
的化学方程式为_______ 。
(2)装置II的作用是_______ 。
(3)若实验中产生的 足量,装置IV中的实验现象
足量,装置IV中的实验现象_______ 。
(4)写出装置V中反应的离子方程式_______ 。
(5)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象,为了达到这一实验目的,你认为还需在图中装置II与III之间添加图中的_______ 装置(填序号)。
① ②
② ③
③ ④
④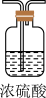
(6)可用 和
和 制备的漂粉精
制备的漂粉精
①漂白精的有效成分是_______ 。
②漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的途径主要是: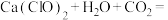 ______+______(把反应补充完整)。
______+______(把反应补充完整)。_______
③池水的酸碱性对漂粉精的消毒效果影响明显。
a.若池水碱性过强,杀毒作用会_______ (填“增强”或“减弱”)。
b.若池水酸性过强,会刺激眼睛和皮肤。有时加入 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是_______ (填离子符号)。
④某届奥运会期间,发生了室外游泳池水变绿的事件,成为当时的一大新闻。有关负责人说,池水变绿是藻类生长造成的。该游泳池每隔一段时间就要投放含氯消毒剂,当再次投放时,误投了过氧化氢( )消毒剂。消毒剂为什么不起作用了?请分析原因:
)消毒剂。消毒剂为什么不起作用了?请分析原因:_______ 。
 的性质,设计如图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
的性质,设计如图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
(1)装置I中仪器c的名称是
 和浓盐酸制备
和浓盐酸制备 的化学方程式为
的化学方程式为(2)装置II的作用是
(3)若实验中产生的
 足量,装置IV中的实验现象
足量,装置IV中的实验现象(4)写出装置V中反应的离子方程式
(5)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象,为了达到这一实验目的,你认为还需在图中装置II与III之间添加图中的
①
 ②
② ③
③ ④
④
(6)可用
 和
和 制备的漂粉精
制备的漂粉精①漂白精的有效成分是
②漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的途径主要是:
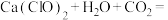 ______+______(把反应补充完整)。
______+______(把反应补充完整)。③池水的酸碱性对漂粉精的消毒效果影响明显。
a.若池水碱性过强,杀毒作用会
b.若池水酸性过强,会刺激眼睛和皮肤。有时加入
 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是④某届奥运会期间,发生了室外游泳池水变绿的事件,成为当时的一大新闻。有关负责人说,池水变绿是藻类生长造成的。该游泳池每隔一段时间就要投放含氯消毒剂,当再次投放时,误投了过氧化氢(
 )消毒剂。消毒剂为什么不起作用了?请分析原因:
)消毒剂。消毒剂为什么不起作用了?请分析原因:
您最近一年使用:0次
名校
解题方法
2 . 甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用如图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)
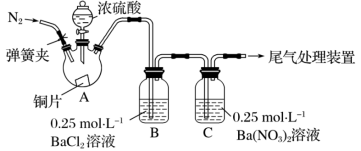
实验操作和现象:
(1)盛放浓硫酸的装置名称为____ 。
(2)A中反应的化学方程式是____ 。
(3)C中白色沉淀是____ (填化学式,下同),C中液面上方生成的浅棕色气体是_____ 。
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是____ ;乙在A、B间增加洗气瓶D,D中盛放的试剂是____ 。
②进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸,请写出乙中产生少量白色沉淀的离子方程式:____ 。
(5)合并(4)中两同学的方案进行试验。B中无沉淀生成,而C中产生白色沉淀,根据甲、乙同学的实验目的可得出的结论是____ 。

实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 尚未发现白色沉淀溶解 |
(2)A中反应的化学方程式是
(3)C中白色沉淀是
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是
②进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
(5)合并(4)中两同学的方案进行试验。B中无沉淀生成,而C中产生白色沉淀,根据甲、乙同学的实验目的可得出的结论是
您最近一年使用:0次
2022-09-21更新
|
206次组卷
|
2卷引用:北京市第五中学2022-2023学年高一上学期第二次阶段检测化学试题
名校
解题方法
3 . 下列实验方案能达到实验目的的是(部分夹持装置已略去)
A.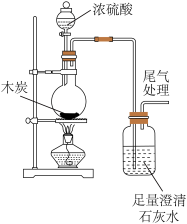 验证木炭和浓硫酸反应生成CO2 验证木炭和浓硫酸反应生成CO2 |
B. 实验室制备Fe(OH)2并能较长时间观察到白色固体 实验室制备Fe(OH)2并能较长时间观察到白色固体 |
C. 实验室制备和收集氨气并验满 实验室制备和收集氨气并验满 |
D.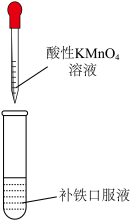 证明补铁口服液中存在+2价的铁 证明补铁口服液中存在+2价的铁 |
您最近一年使用:0次
解题方法
4 .  是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。
【 的制备】
的制备】
(1)用下图装置制备 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是___________ 。 ;
;___________ 。
【 的性质探究】
的性质探究】
资料:i. 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。
ii.单质硫可溶于 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。
某小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是___________ 。
②同学讨论后,设计了如下实验,证实该条件下 的确可以将
的确可以将 氧化成
氧化成 。
。___________ 。
b.连通后电流计指针偏转,一段时间后,___________ (填操作和现象)。
(4)实验I的现象与资料i不相符,其原因是新生成的产物( )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是___________ 。
(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是___________ ,请设计验证此猜想的实验方案___________ 。
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与___________ 等因素有关。
 是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。【
 的制备】
的制备】(1)用下图装置制备
 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是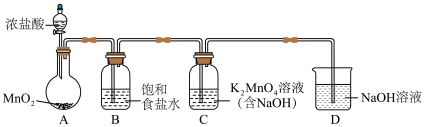
 ;
;【
 的性质探究】
的性质探究】资料:i.
 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。ii.单质硫可溶于
 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。某小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | 实验过程 | 实验现象 |
| Ⅰ |
| 紫色变浅( ),生成棕褐色沉淀( ),生成棕褐色沉淀( ) ) |
| Ⅱ |
| 溶液呈淡黄色( ),生成浅粉色沉淀(MnS) ),生成浅粉色沉淀(MnS) |
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有
 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是②同学讨论后,设计了如下实验,证实该条件下
 的确可以将
的确可以将 氧化成
氧化成 。
。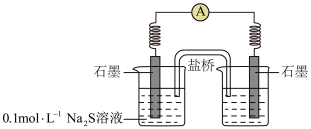
b.连通后电流计指针偏转,一段时间后,
(4)实验I的现象与资料i不相符,其原因是新生成的产物(
 )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与
您最近一年使用:0次
5 . 实验小组利用如下图所示的装置制备氯气及探究氯气的性质。
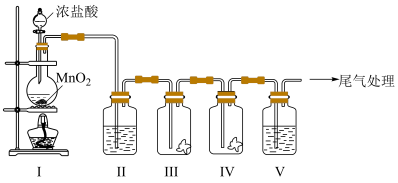
(1)I中制备氯气所发生反应的化学方程式是___________ 。
(2)Ⅱ的目的是除去氯气中的水蒸气,则瓶中盛放的试剂是___________ 。
(3)利用Ⅲ、IV装置探究氯气与水反应的产物。
①实验前,向Ⅲ、Ⅳ中均放入干燥的蓝色石蕊纸花,并向___________ (填Ⅲ或Ⅳ)中滴少量水将纸花润湿。
②实验时,根据Ⅲ中的纸花不变色及Ⅳ中___________ 现象,甲同学得出初步结论:氯气与水反应生成具有酸性 及漂白性 的物质。
③同学们分析后,认为用该实验装置得出“氯气与水反应有酸性物质生成”的结论不严谨,理由是___________ 。
(4)为推断氯气溶于水的产物并验证其光照分解的产物 ,利用数字传感器监测光照过程中某氯水的 、氯水中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示:
、氯水中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示:

支持“氯气与水反应有酸性物质生成”的实验证据是___________ ;
②结合此实验,氯气溶于水发生反应的化学方程式是___________ ;
③分析上述三条曲线的变化趋势,得出的结论是___________ 。

(1)I中制备氯气所发生反应的化学方程式是
(2)Ⅱ的目的是除去氯气中的水蒸气,则瓶中盛放的试剂是
(3)利用Ⅲ、IV装置探究氯气与水反应的产物。
①实验前,向Ⅲ、Ⅳ中均放入干燥的蓝色石蕊纸花,并向
②实验时,根据Ⅲ中的纸花不变色及Ⅳ中
③同学们分析后,认为用该实验装置得出“氯气与水反应有酸性物质生成”的结论不严谨,理由是
(4)
 、氯水中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示:
、氯水中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示:
支持“氯气与水反应有酸性物质生成”的实验证据是
②结合此实验,氯气溶于水发生反应的化学方程式是
③分析上述三条曲线的变化趋势,得出的结论是
您最近一年使用:0次
名校
6 . 某小组同学在实验室制备高铁酸钾(K2FeO4),并探究制备的适宜条件。制备K2FeO4的实验装置如下(夹持装置略)。

资料:K2FeO4为紫色固体,微溶于KOH溶液。
(1)装置A中产生Cl2的化学方程式是_______ (锰被还原为Mn2+)。
(2)研究试剂a对K2FeO4产率的影响,对比实验如下。
上述实验中,溶液总体积、FeCl3和Fe(NO3)3的物质的量、Cl2的通入量均相同。
①实验Ⅱ、Ⅲ产生K2FeO4,将方程式补充完整。
还原反应:_______ 。
氧化反应:_______ 。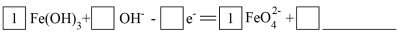
②对实验Ⅰ未产生K2FeO4而实验Ⅱ能产生的原因提出假设:实验Ⅱ溶液碱性较强,增强+3价铁的还原性。以下实验证实了该假设。
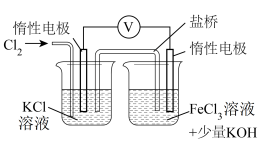
步骤1:通入Cl2,电压表示数为V1;
步骤2:向右侧烧杯中加入_______ (填试剂),电压表示数为V2(V2>V1)。
③反思装置B的作用:用饱和NaCl溶液除去HCl,用平衡移动原理解释_______ 。
④实验Ⅱ中K2FeO4的产率比实验Ⅲ低,试解释原因:_______ 。
(3)向实验Ⅱ所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅。可能原因是通入Cl2后发生_______ (填离子方程式)而使溶液碱性减弱,进而导致K2FeO4分解。

资料:K2FeO4为紫色固体,微溶于KOH溶液。
(1)装置A中产生Cl2的化学方程式是
(2)研究试剂a对K2FeO4产率的影响,对比实验如下。
| 实验编号 | 试剂a | 实验现象 |
| Ⅰ | FeCl3和少量KOH | 无明显现象 |
| Ⅱ | FeCl3和过量KOH | 得到紫色溶液,无紫色固体 |
| Ⅲ | Fe(NO3)3和过量KOH | 得到紫色溶液(颜色比Ⅱ深),有紫色固体 |
①实验Ⅱ、Ⅲ产生K2FeO4,将方程式补充完整。
还原反应:
氧化反应:
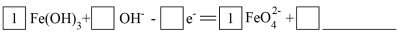
②对实验Ⅰ未产生K2FeO4而实验Ⅱ能产生的原因提出假设:实验Ⅱ溶液碱性较强,增强+3价铁的还原性。以下实验证实了该假设。

步骤1:通入Cl2,电压表示数为V1;
步骤2:向右侧烧杯中加入
③反思装置B的作用:用饱和NaCl溶液除去HCl,用平衡移动原理解释
④实验Ⅱ中K2FeO4的产率比实验Ⅲ低,试解释原因:
(3)向实验Ⅱ所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅。可能原因是通入Cl2后发生
您最近一年使用:0次
名校
解题方法
7 . Ⅰ.某课处小组模拟工业流程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。

(1)写出实验室用Cu与浓硝酸制取 的化学方程式
的化学方程式_____ 。
(2)盛有 溶液的烧杯为尾气处理装置,补全该装置中反应的化学方程式:
溶液的烧杯为尾气处理装置,补全该装置中反应的化学方程式:_____ 。
_____ _____
_____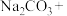 _____
_____ _____
_____ _____;
_____;
(3)用 代替
代替 与水和a气体反应可生成硝酸,该反应原子利用率为100%。此反应的化学方程式是
与水和a气体反应可生成硝酸,该反应原子利用率为100%。此反应的化学方程式是_____ 。
Ⅱ.资料显示:
ⅰ.“ 的氧化性随溶液pH的增大逐渐减弱”。
的氧化性随溶液pH的增大逐渐减弱”。
ⅱ.pH>9.28时,发生歧化反应生成 。
。
某兴趣小组探究不同条件下KI与 反应,实验如下。
反应,实验如下。
(4)实验②中生成 的离子方程式是
的离子方程式是_____ 。
(5)实验④比②溶液颜色浅的原因是_____ 。
(6)为进一步探究KI与 的反应,用上表中的装置继续进行实验:
的反应,用上表中的装置继续进行实验:
对于实验⑥的现象,甲同学提出猜想“pH=10时 不能氧化
不能氧化 ”,设计了下列装置进行实验,验证猜想。
”,设计了下列装置进行实验,验证猜想。

ⅰ、烧杯a中的溶液为_____ 。
ⅱ、实验结果表明,此猜想不成立。支持该结论的实验现象是:通入 后,
后,_____ 。故实验⑥中溶液不变蓝的原因可能是_____ (用离子方程式表示)。

(1)写出实验室用Cu与浓硝酸制取
 的化学方程式
的化学方程式(2)盛有
 溶液的烧杯为尾气处理装置,补全该装置中反应的化学方程式:
溶液的烧杯为尾气处理装置,补全该装置中反应的化学方程式:_____
 _____
_____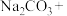 _____
_____ _____
_____ _____;
_____;(3)用
 代替
代替 与水和a气体反应可生成硝酸,该反应原子利用率为100%。此反应的化学方程式是
与水和a气体反应可生成硝酸,该反应原子利用率为100%。此反应的化学方程式是Ⅱ.资料显示:
ⅰ.“
 的氧化性随溶液pH的增大逐渐减弱”。
的氧化性随溶液pH的增大逐渐减弱”。ⅱ.pH>9.28时,发生歧化反应生成
 。
。某兴趣小组探究不同条件下KI与
 反应,实验如下。
反应,实验如下。| 装置 | 烧杯中的液体 | 现象(5分钟后) |
 | ①2mL1mol/LKI溶液+5滴淀粉 | 无明显变化 |
| ②2mL1mol/LKI溶液+5滴淀粉+2mL0.2mol/LHCl溶液 | 溶液变蓝 | |
| ③2mL1mol/LKI溶液+5滴淀粉+2mL0.2mol/LKCl溶液 | 无明显变化 | |
④2mL1mol/LKI溶液+5滴淀粉+2mL0.2mol/L 溶液 溶液 | 溶液变蓝、颜色较②浅 |
 的离子方程式是
的离子方程式是(5)实验④比②溶液颜色浅的原因是
(6)为进一步探究KI与
 的反应,用上表中的装置继续进行实验:
的反应,用上表中的装置继续进行实验:| 小烧杯中的液体 | 现象(5分钟后) |
| ⑤2mLpH=8.5混有KOH的1molKI溶液+5滴淀粉 | 溶液才略变蓝 |
| ⑥2mLpH=10混有KOH的1molKI溶液+5滴淀粉 | 无明显变化 |
 不能氧化
不能氧化 ”,设计了下列装置进行实验,验证猜想。
”,设计了下列装置进行实验,验证猜想。
ⅰ、烧杯a中的溶液为
ⅱ、实验结果表明,此猜想不成立。支持该结论的实验现象是:通入
 后,
后,
您最近一年使用:0次
名校
8 . 某小组同学在实验室制备、收集氯气,并进行氯水中相关物质的性质探究,回答下列问题。

(1)制备Cl2。装置Ⅰ中反应的离子 方程式是___________ 。
(2)除去Cl2中混有的HCl。装置Ⅱ中溶液a为饱和___________ 溶液。
(3)收集Cl2。装置Ⅲ中气体应该从集气瓶的___________ (选“m”或“n”)口进入。
(4)蘸有NaOH溶液的棉花上发生反应的离子 方程式是___________ 。
(5)氯水中相关物质的性质探究。
①若装置Ⅳ中试剂b为H2O,制得氯水。氯水呈黄绿色是由于其中含有___________ ;Cl2与H2O反应的化学方程式为___________ 。
②若装置Ⅳ中试剂b为CCl4,可制得Cl2的CCl4溶液(Cl2可溶于CCl4,且不与CCl4反应)。取稀盐酸、新制氯水、Cl2的CCl4溶液,分别滴在三张红色纸条上,可观察到___________ 现象,证明氯水中HClO具有漂白性作用。
③验证氯水中HClO光照分解的产物。将装置Ⅳ广口瓶中的氯水转移至三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。


若能够证明氯水中HClO在光照下发生了分解反应,则图中纵坐标可以表示的物理量是___________ (填字母)。(注:酸性溶液中,c(H+)越大,pH越小,溶液酸性越强。)
a.氯水的pH b.氢离子的浓度 c.氯离子的浓度 d.氧气的体积分数

(1)制备Cl2。装置Ⅰ中反应的
(2)除去Cl2中混有的HCl。装置Ⅱ中溶液a为饱和
(3)收集Cl2。装置Ⅲ中气体应该从集气瓶的
(4)蘸有NaOH溶液的棉花上发生反应的
(5)氯水中相关物质的性质探究。
①若装置Ⅳ中试剂b为H2O,制得氯水。氯水呈黄绿色是由于其中含有
②若装置Ⅳ中试剂b为CCl4,可制得Cl2的CCl4溶液(Cl2可溶于CCl4,且不与CCl4反应)。取稀盐酸、新制氯水、Cl2的CCl4溶液,分别滴在三张红色纸条上,可观察到
③验证氯水中HClO光照分解的产物。将装置Ⅳ广口瓶中的氯水转移至三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。


若能够证明氯水中HClO在光照下发生了分解反应,则图中纵坐标可以表示的物理量是
a.氯水的pH b.氢离子的浓度 c.氯离子的浓度 d.氧气的体积分数
您最近一年使用:0次
解题方法
9 . 实验小组利用如下图所示的装置制备氯气及探究氯气的性质。
资料: 遇淀粉溶液变蓝,利用此现象可检验溶液中的
遇淀粉溶液变蓝,利用此现象可检验溶液中的 。
。

(1)Ⅰ中制备氯气时,发生反应的化学方程式是___________ 。
(2)Ⅱ的目的是除去氯气中的水蒸气,则瓶中盛放的试剂是___________ 。
(3)利用Ⅲ、Ⅳ装置探究氯气与水反应的产物。
①实验前,向Ⅲ、Ⅳ中均放入干燥的蓝色石蕊纸花,并向___________ 中滴少量水将纸花润湿。
②实验时,根据Ⅲ中的纸花不变色及___________ 现象,甲同学得出初步结论:氯气与水反应生成具有酸性及漂白性的物质。
③同学们分析后,认为用该实验装置不能得出“氯气与水反应有酸性物质生成”的结论,理由是___________ 。
(4)利用装置V探究 的氧化性。V中盛有
的氧化性。V中盛有 溶液,随
溶液,随 通入,溶液由浅绿色逐渐变为棕黄色。为进一步验证
通入,溶液由浅绿色逐渐变为棕黄色。为进一步验证 被
被 氧化后所得的产物,实验方案如下:分别取少量V中反应后的溶液于两支试管中,
氧化后所得的产物,实验方案如下:分别取少量V中反应后的溶液于两支试管中,___________ 。
资料:
 遇淀粉溶液变蓝,利用此现象可检验溶液中的
遇淀粉溶液变蓝,利用此现象可检验溶液中的 。
。
(1)Ⅰ中制备氯气时,发生反应的化学方程式是
(2)Ⅱ的目的是除去氯气中的水蒸气,则瓶中盛放的试剂是
(3)利用Ⅲ、Ⅳ装置探究氯气与水反应的产物。
①实验前,向Ⅲ、Ⅳ中均放入干燥的蓝色石蕊纸花,并向
②实验时,根据Ⅲ中的纸花不变色及
③同学们分析后,认为用该实验装置不能得出“氯气与水反应有酸性物质生成”的结论,理由是
(4)利用装置V探究
 的氧化性。V中盛有
的氧化性。V中盛有 溶液,随
溶液,随 通入,溶液由浅绿色逐渐变为棕黄色。为进一步验证
通入,溶液由浅绿色逐渐变为棕黄色。为进一步验证 被
被 氧化后所得的产物,实验方案如下:分别取少量V中反应后的溶液于两支试管中,
氧化后所得的产物,实验方案如下:分别取少量V中反应后的溶液于两支试管中,
您最近一年使用:0次
10 . Ⅰ.实验室用下图所示的装置制备并收集纯净、干燥的 。
。

(1)实验室制取 的化学方程式是
的化学方程式是_______ 。
(2)除杂装置①中的试剂是_______ 。
(3)除杂装置②中盛放浓硫酸,其作用是_______ 。
(4)请将收集装置的导气管补充完整。
(5)尾气处理装置中的试剂是_______ 。
Ⅱ.某实验小组用收集到到的氯气制得氯水并对氯水成分和性质进行研究,实验如下:
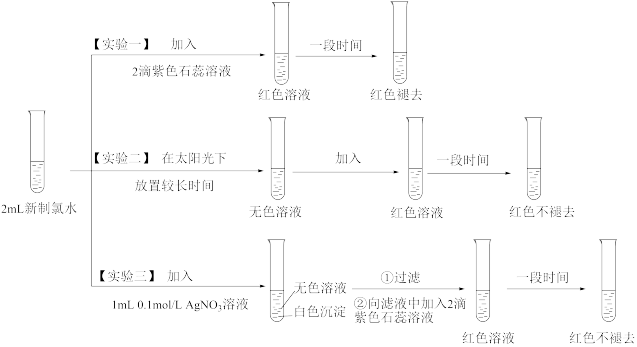
(6)实验一的现象表明,氯水具有酸性和_______ 性。
(7)氯气与水反应的化学方程式为_______ 。
(8)用化学用语说明实验二中“红色不褪去”的原因_______ 。
【实验四】
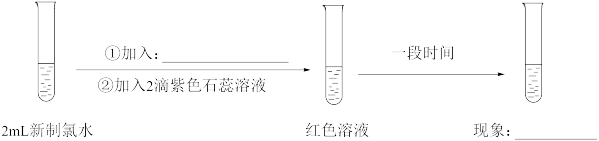
(9)实验四证明了实验三中“红色不褪去”不是因为氯水被稀释,补充所加试剂和现象_______ 。
进一步探究实验三中“红色不褪去”的原因。
【实验五】取实验三的白色沉淀,洗涤,用饱和氯化钠溶液浸泡,取上层清液,滴加2滴紫色石蕊溶液,一段时间后,颜色褪去。
(10)写出氯水和硝酸银溶液反应的化学方程式_______ 。
 。
。
(1)实验室制取
 的化学方程式是
的化学方程式是(2)除杂装置①中的试剂是
(3)除杂装置②中盛放浓硫酸,其作用是
(4)请将收集装置的导气管补充完整。
(5)尾气处理装置中的试剂是
Ⅱ.某实验小组用收集到到的氯气制得氯水并对氯水成分和性质进行研究,实验如下:

(6)实验一的现象表明,氯水具有酸性和
(7)氯气与水反应的化学方程式为
(8)用化学用语说明实验二中“红色不褪去”的原因
【实验四】

(9)实验四证明了实验三中“红色不褪去”不是因为氯水被稀释,补充所加试剂和现象
进一步探究实验三中“红色不褪去”的原因。
【实验五】取实验三的白色沉淀,洗涤,用饱和氯化钠溶液浸泡,取上层清液,滴加2滴紫色石蕊溶液,一段时间后,颜色褪去。
(10)写出氯水和硝酸银溶液反应的化学方程式
您最近一年使用:0次





