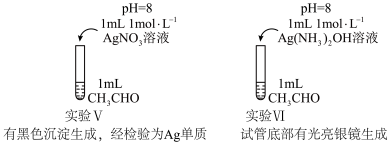
1 . 某实验小组进行如下关于银镜反应的实验探究。
Ⅰ.探究银镜反应中 的作用
的作用
已知:①银镜沉淀速率过快可影响其结构和形貌,从而影响其光泽;
② 开始沉淀时
开始沉淀时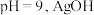 不稳定,易不可逆分解为黑色
不稳定,易不可逆分解为黑色 ;
;
③在实验Ⅰ、Ⅱ、Ⅲ中的 溶液可视作中性溶液。
溶液可视作中性溶液。 的氧化性会随浓度增加而上升,对比实验Ⅰ和Ⅱ,实验小组提出两个猜想:
的氧化性会随浓度增加而上升,对比实验Ⅰ和Ⅱ,实验小组提出两个猜想:
<猜想1> 的氧化性随溶液
的氧化性随溶液 的增大而增大
的增大而增大
<猜想2>_______ 。
(2)该实验小组为进一步探究而设计实验Ⅲ,实验装置如图所示,最终得到结论:“猜想1不合理,猜想2合理”。简述实验Ⅲ的实验过程:_______ 。 相同,对比实验Ⅱ和实验Ⅳ,实验现象出现差异的原因是
相同,对比实验Ⅱ和实验Ⅳ,实验现象出现差异的原因是_______ 。
Ⅱ.该小组在一次制银镜时误将无标签的 溶液当成稀氨水,使得
溶液当成稀氨水,使得 转化为淡黄色
转化为淡黄色 沉淀。查阅资料知只有极浓的氨水可以将
沉淀。查阅资料知只有极浓的氨水可以将 溶解,而实验室并无浓氨水,故不能利用
溶解,而实验室并无浓氨水,故不能利用 制备银氨溶液。实验小组决定采用肼还原
制备银氨溶液。实验小组决定采用肼还原 制银镜,实验报告如下。
制银镜,实验报告如下。
请将实验报告的空缺部分填充完整。
Ⅰ.探究银镜反应中
 的作用
的作用已知:①银镜沉淀速率过快可影响其结构和形貌,从而影响其光泽;
②
 开始沉淀时
开始沉淀时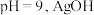 不稳定,易不可逆分解为黑色
不稳定,易不可逆分解为黑色 ;
;③在实验Ⅰ、Ⅱ、Ⅲ中的
 溶液可视作中性溶液。
溶液可视作中性溶液。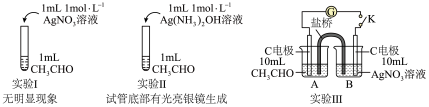
 的氧化性会随浓度增加而上升,对比实验Ⅰ和Ⅱ,实验小组提出两个猜想:
的氧化性会随浓度增加而上升,对比实验Ⅰ和Ⅱ,实验小组提出两个猜想:<猜想1>
 的氧化性随溶液
的氧化性随溶液 的增大而增大
的增大而增大<猜想2>
(2)该实验小组为进一步探究而设计实验Ⅲ,实验装置如图所示,最终得到结论:“猜想1不合理,猜想2合理”。简述实验Ⅲ的实验过程:
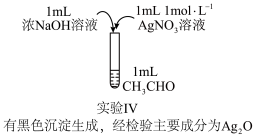
 相同,对比实验Ⅱ和实验Ⅳ,实验现象出现差异的原因是
相同,对比实验Ⅱ和实验Ⅳ,实验现象出现差异的原因是Ⅱ.该小组在一次制银镜时误将无标签的
 溶液当成稀氨水,使得
溶液当成稀氨水,使得 转化为淡黄色
转化为淡黄色 沉淀。查阅资料知只有极浓的氨水可以将
沉淀。查阅资料知只有极浓的氨水可以将 溶解,而实验室并无浓氨水,故不能利用
溶解,而实验室并无浓氨水,故不能利用 制备银氨溶液。实验小组决定采用肼还原
制备银氨溶液。实验小组决定采用肼还原 制银镜,实验报告如下。
制银镜,实验报告如下。请将实验报告的空缺部分填充完整。
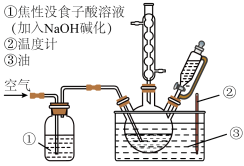
| 实验目的 | 采用肼还原 制得银镜并以此深入探究银镜反应中 制得银镜并以此深入探究银镜反应中 的作用 的作用 | |
| 实验原理 | ①肼 具有强还原性,易吸潮、易被氧化、易与 具有强还原性,易吸潮、易被氧化、易与 等酸性气体反应,常压下可与水形成共沸物(其中肼含量约69%); 等酸性气体反应,常压下可与水形成共沸物(其中肼含量约69%);② 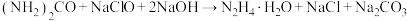 ; ;③  。 。 | |
| 实验药品 |  悬浊液、 悬浊液、 溶液(加 溶液(加 碱化, 碱化,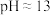 )、催化剂、焦性没食子酸(别名连苯三酚)溶液(加 )、催化剂、焦性没食子酸(别名连苯三酚)溶液(加 碱化, 碱化,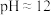 )、尿素、油、 )、尿素、油、 盐酸。 盐酸。 | |
| 实验仪器 | 制备肼的全套装置[具体仪器见装置图,需注意的几点:a.实验最好使用洗气瓶,但因实验室没有洗气瓶,故用 | |
| 实验操作 | ①依图组装仪器并检查气密性,装入药品; ②用 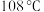 油浴加热,向三预烧瓶缓缓鼓入空气,同时缓缓将恒压滴液漏斗内药品滴入三颈烧瓶,加热约 油浴加热,向三预烧瓶缓缓鼓入空气,同时缓缓将恒压滴液漏斗内药品滴入三颈烧瓶,加热约 后停止加热; 后停止加热;③将三预烧瓶内的液体进行减压蒸馏,得到氨肼混合溶液,将其滴加入  悬浊液中。 悬浊液中。 |
|
| 实验结果 | 实验制得了银单质,但其并未附着在试管壁上形成银镜,而是松散的银粉。 | |
| 实验反思 | ①焦性没食子酸溶液(加 碱化)的作用是 碱化)的作用是②为深入研究为何该反应没有生成银镜,我们又做了如下实验:
| |
您最近一年使用:0次
2 . 下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象结论 | |
| A | 比较碳酸和盐酸的酸性强弱 | 适量二氧化碳通入氯化钡溶液中 | 产生沉淀,碳酸的酸性比盐酸弱 |
| B | 检验某钠盐的成分 | 向钠盐中滴加稀盐酸并将产生的气体通入澄清石灰水 | 石灰水变浑浊,该钠盐为Na2CO3 |
| C | 检验MnO2和浓盐酸反应后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入稀HNO3、AgNO3溶液 | 产生大量白色沉淀,则盐酸有剩余 |
| D | 制备Fe(OH)3胶体 | 向沸水中滴入几滴FeCl3饱和溶液,继续煮沸,并用激光笔照射溶液变红褐色,出现 | 丁达尔效应,产生了胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 如图所示实验方案无法 达到预期实验目的的是
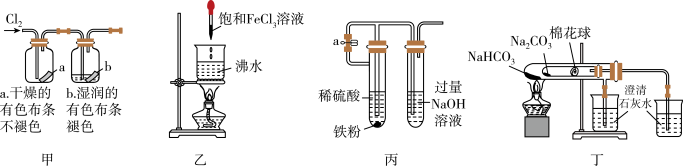

| A.用甲装置证明Cl2与水反应的产物有漂白性 |
| B.用乙装置制备氢氧化铁胶体 |
| C.用丙装置制备Fe(OH)2 |
| D.用丁装置比较Na2CO3和NaHCO3的稳定性 |
您最近一年使用:0次
解题方法
4 . 某实验活动小组设计了如下反应装置制备无水氯化铝,已知无水氯化铝易潮解,遇水蒸气产生大量白雾,在标压下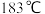 升华,经冷却后可凝华为固体。
升华,经冷却后可凝华为固体。
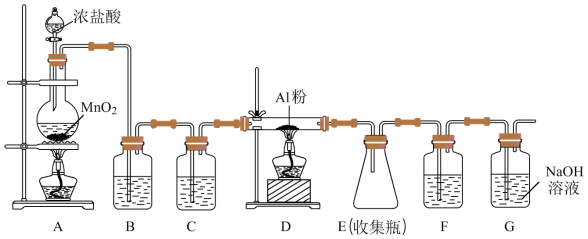
请回答:
(1)盛装浓盐酸的仪器的名称是:___________ ,向其中加入如图所示的浓盐酸,其物质的量浓度是___________  。
。
(2)装置B的作用是___________ ,装置F中盛放___________ 。
(3)请写出装置A中发生的化学方程式___________ ,D中反应的化学方程式___________ G中反应的离子方程式___________ 。
(4)某学习小组用下图装置研究气体X的性质,气体X的主要成分是氯气,其中含有少量水蒸气。请回答下列问题:
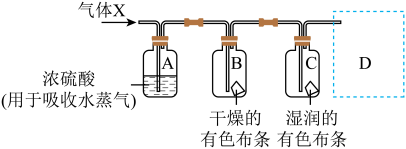
分别描述B、C装置中的现象:B___________ ,C___________ ,从物质性质说明B、C装置中现象不同的原因:___________ 。
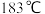 升华,经冷却后可凝华为固体。
升华,经冷却后可凝华为固体。
请回答:
(1)盛装浓盐酸的仪器的名称是:
 。
。| 盐酸 化学式:  相对分子质量:36.5 外观:合格 密度:   的质量分数:36.5% 的质量分数:36.5%符合 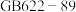 |
(2)装置B的作用是
(3)请写出装置A中发生的化学方程式
(4)某学习小组用下图装置研究气体X的性质,气体X的主要成分是氯气,其中含有少量水蒸气。请回答下列问题:

分别描述B、C装置中的现象:B
您最近一年使用:0次
5 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO。已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。
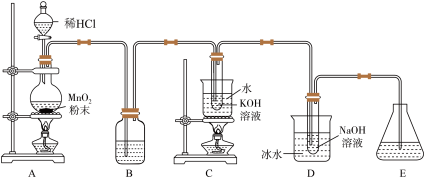
回答下列问题:
(1)试验中盛放MnO2粉末的装置名称是___________ 。
(2)装置A中产生氯气的化学方程式是___________ 。
(3)装置D中发生反应的离子反应式是___________ 。
(4)装置D中冰水的作用是___________ 。
(5)在下列试剂中可选用加入装置E的最佳试剂是___________(填标号)。
(6)探究KClO3、NaClO的氧化能力
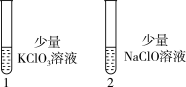
操作:向1号和2号试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3___________ NaClO。(填“大于”或“小于”)

回答下列问题:
(1)试验中盛放MnO2粉末的装置名称是
(2)装置A中产生氯气的化学方程式是
(3)装置D中发生反应的离子反应式是
(4)装置D中冰水的作用是
(5)在下列试剂中可选用加入装置E的最佳试剂是___________(填标号)。
| A.KI溶液 | B.饱和食盐水 | C. 溶液 溶液 | D.浓 |

操作:向1号和2号试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3
您最近一年使用:0次
2023-05-21更新
|
372次组卷
|
3卷引用:浙江省金华十校2022-2023学年高一上学期期末调研模拟考试化学试题
名校
6 . 下图是实验室制备氯气并进行一系列相关实验的装置(加热和夹持仪器已省略)。
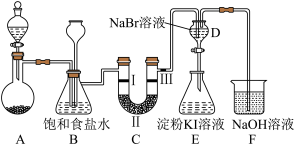
(1)用来盛放浓盐酸的仪器的名称是_______ ,装置A选用二氧化锰固体和浓盐酸在加热条件下制备氯气,反应的化学方程式为_______ 。
(2)装置C可验证干燥的氯气没有漂白性,则装置C中II的作用是_______ ,I与III是干燥的有色布条,描述I、III处的现象:_______ 。
(3)E 中实验现象为_______ 。

(1)用来盛放浓盐酸的仪器的名称是
(2)装置C可验证干燥的氯气没有漂白性,则装置C中II的作用是
(3)E 中实验现象为
您最近一年使用:0次
2022-11-19更新
|
123次组卷
|
2卷引用:浙江省杭州市S9联盟2022-2023学年高一上学期期中联考化学试题
7 . 氯及其化合物既是重要化工原料,又是高效、广谱消毒剂。
(1)实验室处理氯气尾气的化学方程式:_______ 。
(2)实验室利用如图装置制备NaClO和NaClO3,已知;6OH-+3Cl2 5Cl-+
5Cl-+ +3H2O
+3H2O
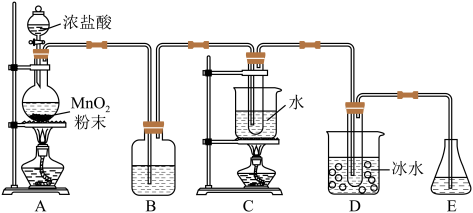
①盛放浓盐酸的仪器名称是_______ ,A中发生反应的离子方程式为_______ 。
②B的作用是_______ ;C中试管内盛放的试剂为_______ 。
③用8.7gMnO2与足量浓盐酸充分反应,生成Cl2的质量为_______ 。
(3)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。
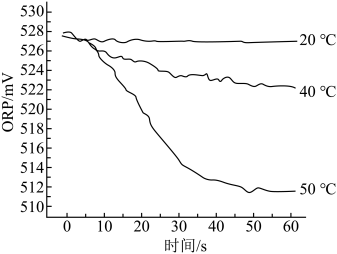
已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是为_______ 。
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是_______ 。
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,则需加水的质量为_______ g。
(1)实验室处理氯气尾气的化学方程式:
(2)实验室利用如图装置制备NaClO和NaClO3,已知;6OH-+3Cl2
 5Cl-+
5Cl-+ +3H2O
+3H2O
①盛放浓盐酸的仪器名称是
②B的作用是
③用8.7gMnO2与足量浓盐酸充分反应,生成Cl2的质量为
(3)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是为
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,则需加水的质量为
您最近一年使用:0次
8 . 如图是实验室制备氯气并进行一系列相关实验的装置(加热和夹持仪器已省略)。
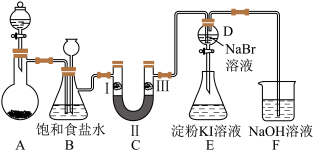
(1)装置A选用二氧化锰固体和浓盐酸在加热条件下制备氯气,反应的化学方程式为_______ 。
(2)装置B中饱和食盐水的作用是_______ ;装置B中长颈漏斗的作用是_______ 。
(3)装置C可验证氯气不具有漂白性,则I、II、III依次放入_______ (填字母)。
(4)已知:Cl2的氧化性强于I2,则E中实验现象为_______ 。
(5)装置F中的离子方程式是_______ 。

(1)装置A选用二氧化锰固体和浓盐酸在加热条件下制备氯气,反应的化学方程式为
(2)装置B中饱和食盐水的作用是
(3)装置C可验证氯气不具有漂白性,则I、II、III依次放入
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)装置F中的离子方程式是
您最近一年使用:0次
9 . 已知 易溶于水和乙醇。某实验小组用如下装置制备
易溶于水和乙醇。某实验小组用如下装置制备 并探究其性质。装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入
并探究其性质。装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入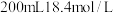 浓硫酸,充分反应直至装置A中反应停止。回答下列问题:
浓硫酸,充分反应直至装置A中反应停止。回答下列问题:
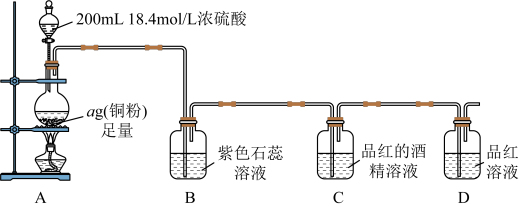
(1)盛装浓硫酸仪器的名称是___________ 。
(2)写出装置A中发生反应的化学方程式为___________ 。
(3)根据装置C、D的现象,可以得出的结论是___________ 。
(4)使品红褪色的主要微粒可能有___________ ;根据提出假设,设计对照验证实验。实验过程中除温度外,还需要控制的变量有___________ (写出两点即可)
 易溶于水和乙醇。某实验小组用如下装置制备
易溶于水和乙醇。某实验小组用如下装置制备 并探究其性质。装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入
并探究其性质。装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入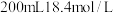 浓硫酸,充分反应直至装置A中反应停止。回答下列问题:
浓硫酸,充分反应直至装置A中反应停止。回答下列问题:
(1)盛装浓硫酸仪器的名称是
(2)写出装置A中发生反应的化学方程式为
(3)根据装置C、D的现象,可以得出的结论是
(4)使品红褪色的主要微粒可能有
您最近一年使用:0次
21-22高一上·浙江·阶段练习
解题方法
10 . 在常温下,Fe 与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,完成高温下“Fe与水蒸气的反应实验”然后对产物进行检验。请回答该实验中的问题。
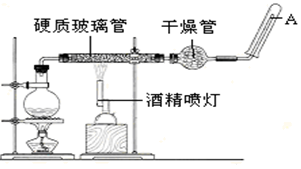
(1)写出该反应的化学方程式______
(2)实验开始时应先点燃_______ ,实验结束时应先熄灭_______ 。
(3)该同学探究反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按如图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出有关变色反应的化学方程式_______ 。
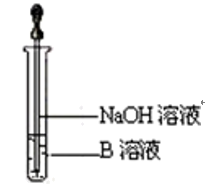
氢氧化亚铁具有强还原性极容易被氧化变色:写出一种实验制备氢氧化亚铁防止氧化的措施:______ 。
(4)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有还原性。由此可知,实验室中含Fe2+盐溶液现用现配制的原因_______ ,并且配制含Fe2+的盐溶液时应加入少量 _______ ,检验硫酸铁盐溶液中是否含有硫酸亚铁盐的方法是 _______ 。

(1)写出该反应的化学方程式
(2)实验开始时应先点燃
(3)该同学探究反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按如图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出有关变色反应的化学方程式

氢氧化亚铁具有强还原性极容易被氧化变色:写出一种实验制备氢氧化亚铁防止氧化的措施:
(4)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有还原性。由此可知,实验室中含Fe2+盐溶液现用现配制的原因
您最近一年使用:0次