解题方法
1 .  溶液与KI溶液混合时,按照复分解反应原理分析,可得到AgI黄色沉淀。查阅资料可知:①
溶液与KI溶液混合时,按照复分解反应原理分析,可得到AgI黄色沉淀。查阅资料可知:① 溶液呈酸性;②
溶液呈酸性;② 具有较强的氧化性;③单质碘遇淀粉溶液会变蓝。根据所得信息,甲学生对
具有较强的氧化性;③单质碘遇淀粉溶液会变蓝。根据所得信息,甲学生对 溶液与KI溶液混合时发生的反应做出了如下猜测:
溶液与KI溶液混合时发生的反应做出了如下猜测:
猜测1:发生复分解反应。
猜测2: 与
与 发生氧化还原反应。
发生氧化还原反应。
(1)①如果猜测2成立,则发生反应的化学方程式为_______ ;为了验证该猜测,甲同学往反应后的溶液中加入淀粉,观察到溶液变蓝,证明猜测2成立。
②乙同学认为甲同学的实验方案不能证明猜测2成立,原因是 溶液中的
溶液中的 在酸性条件下具有较强的氧化性,也可能氧化
在酸性条件下具有较强的氧化性,也可能氧化 ,反应的离子方程式为
,反应的离子方程式为_______ ;该反应中的氧化剂和还原剂的物质的量之比为_______ 。
(2)乙同学利用原电池原理来验证以上猜测,设计了如图所示实验装置(盐桥中的离子可以自由移动,两烧杯中电解质溶液足量),一段时间后,电流计指针发生偏转, 溶液无气泡产生,石墨2表面有银白色金属析出。
溶液无气泡产生,石墨2表面有银白色金属析出。
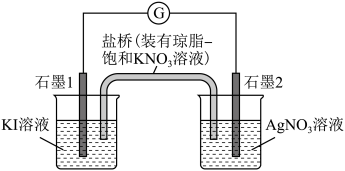
①该装置的负极为石墨_______ (填“1”或“2”)。
②若石墨2增重5.4g(不考虑其他反应),则电路中转移电子数为_______  。
。
③根据实验现象,证明猜测2成立。若将盐桥中的 溶液换成
溶液换成 溶液,一段时间后,电流计指针不发生偏转,可能原因是
溶液,一段时间后,电流计指针不发生偏转,可能原因是_______ 。
(3)原电池在生产生活和学习中有着广泛的应用,下列关于原电池的说法正确的是_______(填标号)。
 溶液与KI溶液混合时,按照复分解反应原理分析,可得到AgI黄色沉淀。查阅资料可知:①
溶液与KI溶液混合时,按照复分解反应原理分析,可得到AgI黄色沉淀。查阅资料可知:① 溶液呈酸性;②
溶液呈酸性;② 具有较强的氧化性;③单质碘遇淀粉溶液会变蓝。根据所得信息,甲学生对
具有较强的氧化性;③单质碘遇淀粉溶液会变蓝。根据所得信息,甲学生对 溶液与KI溶液混合时发生的反应做出了如下猜测:
溶液与KI溶液混合时发生的反应做出了如下猜测:猜测1:发生复分解反应。
猜测2:
 与
与 发生氧化还原反应。
发生氧化还原反应。(1)①如果猜测2成立,则发生反应的化学方程式为
②乙同学认为甲同学的实验方案不能证明猜测2成立,原因是
 溶液中的
溶液中的 在酸性条件下具有较强的氧化性,也可能氧化
在酸性条件下具有较强的氧化性,也可能氧化 ,反应的离子方程式为
,反应的离子方程式为(2)乙同学利用原电池原理来验证以上猜测,设计了如图所示实验装置(盐桥中的离子可以自由移动,两烧杯中电解质溶液足量),一段时间后,电流计指针发生偏转,
 溶液无气泡产生,石墨2表面有银白色金属析出。
溶液无气泡产生,石墨2表面有银白色金属析出。
①该装置的负极为石墨
②若石墨2增重5.4g(不考虑其他反应),则电路中转移电子数为
 。
。③根据实验现象,证明猜测2成立。若将盐桥中的
 溶液换成
溶液换成 溶液,一段时间后,电流计指针不发生偏转,可能原因是
溶液,一段时间后,电流计指针不发生偏转,可能原因是(3)原电池在生产生活和学习中有着广泛的应用,下列关于原电池的说法正确的是_______(填标号)。
| A.原电池是化学能转化为电能的装置 | B.原电池内发生的反应为氧化还原反应 |
| C.所有的化学反应均可设计成原电池 | D.电子从负极流出,经电解质溶液流入正极 |
您最近一年使用:0次
2023-05-20更新
|
210次组卷
|
2卷引用:江西省吉安市吉州区部分学校联考2022-2023学年高一下学期7月期末考试化学试题
2011·江西吉安·一模
2 . 下面是某学习小组对乙二酸的某些性质进行研究性学习的过程:
【研究课题】探究乙二酸的某些性质
【查阅资料】乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
又知草酸在100℃时开始升华,157℃时大量升华,并开始分解。草酸钙不溶于水。根据上述材料提供的信息,回答下列问题:
【提出猜想】
[猜想一]根据草酸晶体的组成对其分解产物进行猜想,设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,并设计了探究实验,实验装置如下(草酸晶体分解装置略)。

A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰(已知草酸蒸气也可使澄清石灰水变浑浊,草酸蒸气在低温下可冷凝为固体)。请回答下列问题:
①装置的连接顺序为:A→__________ ;
②检验产物中CO的实验现象是__________ ;
③整套装置是否存在不合理之处,__________ (填是或否),若有该如何解决__________ ;
(猜想二)乙二酸具有弱酸性,设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是__________ (填字母)
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性,设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性,写出该反应的离子方程式:__________ ;
(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4•2H2O及其它一些杂质)中H2C2O4•2H2O的含量。方法是:称取该样品0.12g,加适量水完全溶解,然后用0.020mol•L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4•2H2O的质量分数为__________ ;(已知相对原子质量:Mr(H2C2O4•2H2O)=126)。

【研究课题】探究乙二酸的某些性质
【查阅资料】乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
| 名称 | 乙二酸 | 乙二酸晶体 |
| 分子式 | H2C2O4 | H2C2O4·2H2O |
| 颜色状态 | 无色固体 | 无色晶体 |
| 溶解度(g) | 8.6(20℃) | — |
| 熔点(℃) | 189.5 | 101.5 |
| 密度(g·cm-3) | 1.900 | 1.650 |
【提出猜想】
[猜想一]根据草酸晶体的组成对其分解产物进行猜想,设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,并设计了探究实验,实验装置如下(草酸晶体分解装置略)。

A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰(已知草酸蒸气也可使澄清石灰水变浑浊,草酸蒸气在低温下可冷凝为固体)。请回答下列问题:
①装置的连接顺序为:A→
②检验产物中CO的实验现象是
③整套装置是否存在不合理之处,
(猜想二)乙二酸具有弱酸性,设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性,设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性,写出该反应的离子方程式:
(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4•2H2O及其它一些杂质)中H2C2O4•2H2O的含量。方法是:称取该样品0.12g,加适量水完全溶解,然后用0.020mol•L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4•2H2O的质量分数为

您最近一年使用:0次
3 . 某学习小组研究溶液中Fe2+的稳定性;进行如下实验,观察,记录结果。
实验I

(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是_____________ (用化学用语表示)。溶液的稳定性:FeSO4_______ (NH4)2Fe(SO4)2(填“>”或“<”)。
(2)甲同学提出实验I中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+有还原性,进行实验Ⅱ,否定了该观点,补全该实验_______ 。

(3)乙同学提出实验I中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ;分别配制0.80mol•L-1pH为1、2、3、4的FeSO4溶液,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应 4Fe2++O2+10H2O 4Fe(OH)3+8H+由实验Ⅲ,乙同学可得出的结论是
4Fe(OH)3+8H+由实验Ⅲ,乙同学可得出的结论是_________ ,原因是_________ 。
(4)进一步研究在水溶液中Fe2+的氧化机理,测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率逐渐增大的原因可能是_________ 。

(5)综合以上实验,增强Fe2+稳定性的措施有_________ 。
实验I

(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是
(2)甲同学提出实验I中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+有还原性,进行实验Ⅱ,否定了该观点,补全该实验

(3)乙同学提出实验I中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ;分别配制0.80mol•L-1pH为1、2、3、4的FeSO4溶液,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应 4Fe2++O2+10H2O
 4Fe(OH)3+8H+由实验Ⅲ,乙同学可得出的结论是
4Fe(OH)3+8H+由实验Ⅲ,乙同学可得出的结论是(4)进一步研究在水溶液中Fe2+的氧化机理,测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率逐渐增大的原因可能是

(5)综合以上实验,增强Fe2+稳定性的措施有
您最近一年使用:0次
名校
解题方法
4 . 如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).

(1)装置A中两个玻璃仪器名称分别是__ 和__ ;
(2)实验室用MnO2制备氯气的化学方程式是__ ;
(3)实验时多余的氯气可用F装置来吸收,有关化学方程式是_ ;
(4)装置B中饱和食盐水的作用是__ ;
(5)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入湿润有色布条;__ ;(可供选择的用品有:无水氯化钙、碱石灰)和干燥的有色布条。
(6)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱,当向D中缓缓通入少量氯气时,D中可以观察到的现象是__ 。

(1)装置A中两个玻璃仪器名称分别是
(2)实验室用MnO2制备氯气的化学方程式是
(3)实验时多余的氯气可用F装置来吸收,有关化学方程式是
(4)装置B中饱和食盐水的作用是
(5)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入湿润有色布条;
(6)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱,当向D中缓缓通入少量氯气时,D中可以观察到的现象是
您最近一年使用:0次
2018-09-20更新
|
298次组卷
|
5卷引用:江西省吉安市遂川中学2022-2023学年高一上学期期末考试化学试题
江西省吉安市遂川中学2022-2023学年高一上学期期末考试化学试题【全国百强校】江苏省南菁高级中学2017-2018学年高一上学期期中考试化学试题(已下线)2018年11月21日 《每日一题》人教必修1-氯气的实验室制取河南省封丘县第一中学2018-2019学年高一下学期开学考试化学试题(已下线)4.2.2 氯气与碱反应及Cl-的检验(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)
5 . 某小组设计实验探究SO2和漂粉精反应原理,装置如图所示。、

实验操作过程如下:
步骤1:连接装置并检查装置气密性,按如图所示装好药品;
步骤2:打开止水夹,向装置中通入一段时间N2,并关闭止水夹;
步骤3:取下分液漏斗的塞子,旋转活塞,向三颈瓶中滴加饱和Na2SO3溶液。过一会儿,观察到B和C中都产生白色沉淀
步骤4:实验完毕后,检验C中白色固体,白色固体是CaSO4。
回答下列问题:
(1)B装置中盐酸的作用是__ ;能证明A中产生的“酸雾”含有H2SO4的实验现象是___ 。
(2)A中硫酸表现出来的性质有__ 。
(3)步骤2中通入N2的目的是__ 。
(4)实验完毕后,经检验,D中溶液含有等物质的量浓度的两种还原性盐,写出总反应的离子方程式__ 。
(5)步骤4检验C中白色沉淀成分的操作是,取少量C中白色固体,滴加足量___ (填名称),振荡,白色固体不溶解,则白色固体是CaSO4。
(6)经分析,C中发生化学反应与反应物相对量有关:
若通入少量SO2,则发生反应为3Ca(ClO)2+2SO2+2H2O═2CaSO4↓+4HClO+CaCl2;
若通入过量SO2,则发生反应为Ca(ClO)2+2SO2+2H2O═CaSO4↓+H2SO4+2HCl,SO2+H2O⇌H2SO3。
设计实验证明上述C中通入过量SO2:__ 。

实验操作过程如下:
步骤1:连接装置并检查装置气密性,按如图所示装好药品;
步骤2:打开止水夹,向装置中通入一段时间N2,并关闭止水夹;
步骤3:取下分液漏斗的塞子,旋转活塞,向三颈瓶中滴加饱和Na2SO3溶液。过一会儿,观察到B和C中都产生白色沉淀
步骤4:实验完毕后,检验C中白色固体,白色固体是CaSO4。
回答下列问题:
(1)B装置中盐酸的作用是
(2)A中硫酸表现出来的性质有
(3)步骤2中通入N2的目的是
(4)实验完毕后,经检验,D中溶液含有等物质的量浓度的两种还原性盐,写出总反应的离子方程式
(5)步骤4检验C中白色沉淀成分的操作是,取少量C中白色固体,滴加足量
(6)经分析,C中发生化学反应与反应物相对量有关:
若通入少量SO2,则发生反应为3Ca(ClO)2+2SO2+2H2O═2CaSO4↓+4HClO+CaCl2;
若通入过量SO2,则发生反应为Ca(ClO)2+2SO2+2H2O═CaSO4↓+H2SO4+2HCl,SO2+H2O⇌H2SO3。
设计实验证明上述C中通入过量SO2:
您最近一年使用:0次
2020-03-06更新
|
222次组卷
|
3卷引用:江西省吉安市2020届高三上学期期末教学质量检测化学试题
江西省吉安市2020届高三上学期期末教学质量检测化学试题(已下线)考点16 非金属元素及其化合物-2020年高考化学命题预测与模拟试题分类精编广东省广州市海珠区为明学校2021-2022学年高一下学期期中考试化学试题
名校
解题方法
6 . 已知硫酸亚铁铵[ ](俗称莫尔盐)可溶于水,在
](俗称莫尔盐)可溶于水,在 时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
Ⅰ. 探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是_______ ,由此可知分解产物中有_______ (填化学式)。
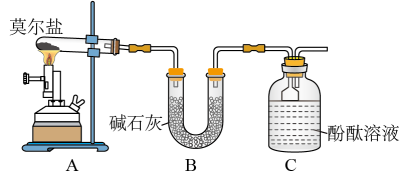
(2)乙同学认为莫尔盐晶体分解的产物中还可能含有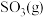 、
、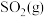 及
及 。为验证产物的存在,用下列装置进行实验。
。为验证产物的存在,用下列装置进行实验。
①乙同学的实验中,装置依次连按的合理顺序为:A→H→→→→G。_______
②证明含有 的实验现象是
的实验现象是_______ 。
Ⅱ. 为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成 溶液。甲、乙两位同学设计了如下两个实验方案。
溶液。甲、乙两位同学设计了如下两个实验方案。
甲方案:取 样品溶液用
样品溶液用 的酸性
的酸性 溶液分三次进行测定。
溶液分三次进行测定。
乙方案(通过 测定):实验设计装置如图所示。取
测定):实验设计装置如图所示。取 样品溶液进行该实验。
样品溶液进行该实验。
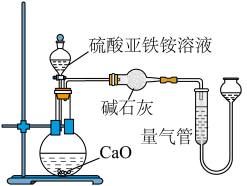
请回答:
(3)乙方案中量气管中最佳试剂是_______ 。
a. 水 b. 饱和 溶液 c.
溶液 c.  d. 饱和
d. 饱和 溶液
溶液
(4)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是_______ 。
(5)若测得 为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
为VL(已折算为标准状况下),则硫酸亚铁铵纯度为_______ (列出计算式)。
 ](俗称莫尔盐)可溶于水,在
](俗称莫尔盐)可溶于水,在 时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
时分解,其探究其化学性质,甲、乙两同学设计了如下实验。Ⅰ. 探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是

(2)乙同学认为莫尔盐晶体分解的产物中还可能含有
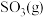 、
、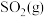 及
及 。为验证产物的存在,用下列装置进行实验。
。为验证产物的存在,用下列装置进行实验。 |  |  | 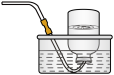 |  |
| D. 品红溶液 | E.  溶液 溶液 | F.  溶液和足量盐酸 溶液和足量盐酸 | G. 排水集气法 | H.安全瓶 |
②证明含有
 的实验现象是
的实验现象是Ⅱ. 为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成
 溶液。甲、乙两位同学设计了如下两个实验方案。
溶液。甲、乙两位同学设计了如下两个实验方案。甲方案:取
 样品溶液用
样品溶液用 的酸性
的酸性 溶液分三次进行测定。
溶液分三次进行测定。乙方案(通过
 测定):实验设计装置如图所示。取
测定):实验设计装置如图所示。取 样品溶液进行该实验。
样品溶液进行该实验。
请回答:
(3)乙方案中量气管中最佳试剂是
a. 水 b. 饱和
 溶液 c.
溶液 c.  d. 饱和
d. 饱和 溶液
溶液(4)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是
(5)若测得
 为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
您最近一年使用:0次
2023-01-21更新
|
764次组卷
|
3卷引用:江西省吉安市永丰县永丰中学2022-2023学年高一上学期期末考试化学(B班)试题



