名校
解题方法
1 . Ⅰ.如图是某学校实验室从化学试剂商店买回来的NaOH试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
标签上的有关数据回答下列问题:
(1)该NaOH溶液的物质的量浓度为___________ (保留两位小数);现在要配制480mL该浓度的NaOH溶液,应用托盘天平称取NaOH的质量为___________ 。
(2)配制上述溶液的过程中需要用到的主要玻璃仪器除了量筒、烧杯、玻璃棒外,还缺少的必要玻璃仪器为___________ 、___________ (填仪器名称)。
(3)若取5mL该溶液用水稀释到100mL,所得溶液 的物质的量浓度为
的物质的量浓度为___________ 。
(4)下列操作能使NaOH溶液的物质的量浓度偏高的有___________ (填字母)。
a.摇匀后发现液面低于刻度线再加水
b.NaOH溶解后未恢复至室温就注入容量瓶中
c.转移时没有洗涤烧杯、玻璃棒
d.定容时俯视刻度线
e.容量瓶未烘干
Ⅱ.某同学发现上个月做实验用的NaOH溶液忘记盖瓶塞。对于该溶液是否变质,该同学对此进行了探究。请你一起完成下列实验报告。
【提出问题1】该溶液是否变质?
【实验探究1】
(5)完成下列表格
【提出问题2】该溶液变质程度怎样?
【提出猜想】
(6)猜想一:已完全变质,该溶液中溶质只含 。
。
猜想二:部分变质,该溶液中溶质含有___________ 。
该同学探究该溶液是否完全变质,准备了两种试剂:①酚酞试液,②足量的 溶液(
溶液( 溶液为中性溶液),若加入顺序为②①,当出现
溶液为中性溶液),若加入顺序为②①,当出现___________ 现象时,说明NaOH溶液已完全变质,其中加入②时发生反应的化学方程式为___________ 。
| 氢氧化钠溶液 化学式:NaOH 相对分子质量:40 密度: 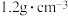 质量分数:20% |
(1)该NaOH溶液的物质的量浓度为
(2)配制上述溶液的过程中需要用到的主要玻璃仪器除了量筒、烧杯、玻璃棒外,还缺少的必要玻璃仪器为
(3)若取5mL该溶液用水稀释到100mL,所得溶液
 的物质的量浓度为
的物质的量浓度为(4)下列操作能使NaOH溶液的物质的量浓度偏高的有
a.摇匀后发现液面低于刻度线再加水
b.NaOH溶解后未恢复至室温就注入容量瓶中
c.转移时没有洗涤烧杯、玻璃棒
d.定容时俯视刻度线
e.容量瓶未烘干
Ⅱ.某同学发现上个月做实验用的NaOH溶液忘记盖瓶塞。对于该溶液是否变质,该同学对此进行了探究。请你一起完成下列实验报告。
【提出问题1】该溶液是否变质?
【实验探究1】
(5)完成下列表格
| 实验步骤 | 实验现象 | 解释与结论 |
| 取少量该溶液于试管中,滴加足量稀盐酸 | 有 | 说明该溶液已变质。变质的原因是 |
【提出问题2】该溶液变质程度怎样?
【提出猜想】
(6)猜想一:已完全变质,该溶液中溶质只含
 。
。猜想二:部分变质,该溶液中溶质含有
该同学探究该溶液是否完全变质,准备了两种试剂:①酚酞试液,②足量的
 溶液(
溶液( 溶液为中性溶液),若加入顺序为②①,当出现
溶液为中性溶液),若加入顺序为②①,当出现
您最近一年使用:0次
名校
解题方法
2 . 下列实验能达到实验目的的是


| A.图1装置可制备H2S气体 |
| B.图2装置可准确测定醋酸溶液的浓度 |
| C.图3装置可验证碳酸氢钠与柠檬酸反应的热效应 |
| D.图4装置可验证非金属性Cl>C>Si |
您最近一年使用:0次
2023-10-07更新
|
407次组卷
|
2卷引用:河北省石家庄市第一中学2024届高三上学期第一次月考化学试题
3 . 亚硝酸钠( )是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究
)是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究 的性质。
的性质。
(1) 中
中 元素的化合价是
元素的化合价是_____ ,根据 的化合价,推测
的化合价,推测 具有
具有_____ (填“氧化性”、“还原性”或“氧化性和还原性”)。
(2)该化学兴趣小组为了验证推测的结果,设计实验操作如下表所示,请完善表格中的实验现象和结论(已知 遇淀粉变蓝)。
遇淀粉变蓝)。
(3)通过上述实验可知, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_____ 。
(4)根据我国食品添加剂使用标准,亚硝酸钠在肉制品中的最大使用量是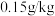 ;则
;则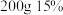 的
的 溶液最多可生产的肉制品的质量为
溶液最多可生产的肉制品的质量为_____ kg。
 )是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究
)是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究 的性质。
的性质。(1)
 中
中 元素的化合价是
元素的化合价是 的化合价,推测
的化合价,推测 具有
具有(2)该化学兴趣小组为了验证推测的结果,设计实验操作如下表所示,请完善表格中的实验现象和结论(已知
 遇淀粉变蓝)。
遇淀粉变蓝)。| 实验 | 实验操作及现象或结果 | 结论 |
| ① | 取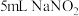 溶液于试管中,加入少量 溶液于试管中,加入少量 溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 |  具有 具有 |
| ② | 取 溶液(先酸化好)于试管中,滴加足量的 溶液(先酸化好)于试管中,滴加足量的 溶液,可观察到的实验现象为 溶液,可观察到的实验现象为 |  具有还原性 具有还原性 |
| ③ |  固体与70%硫酸反应生成了 固体与70%硫酸反应生成了 和 和 两种气体 两种气体 |  具有 具有 |
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(4)根据我国食品添加剂使用标准,亚硝酸钠在肉制品中的最大使用量是
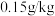 ;则
;则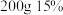 的
的 溶液最多可生产的肉制品的质量为
溶液最多可生产的肉制品的质量为
您最近一年使用:0次
2023-07-30更新
|
99次组卷
|
3卷引用:河北省石家庄市第四十二中学2023-2024学年高一上学期第一次月考化学试题
名校
4 . 某实验小组对Cu与 的反应进行研究,实验如下。
的反应进行研究,实验如下。

(1)试管①中反应的化学方程式是_______ 。
(2)已知绿色是棕色和蓝色的混合色,绿色溶液变蓝是因为 与水生成了
与水生成了 和
和_______ 。
(3)对比③和⑤中现象,为探究③中立即产生气泡的原因,实验小组提出如下假设,并设计实验验证。
假设1: 对该反应有催化作用。
对该反应有催化作用。
假设2: 对该反应有催化作用。
对该反应有催化作用。
假设3: 对该反应有催化作用。
对该反应有催化作用。
(4)得出实验结论后,有同学认为还应补充对比实验:向④溶液加入几滴较浓的硝酸后加入铜片。补充该实验的目的是_______ 。
(5)某工厂用硝酸溶解废铜屑制备 ,为避免
,为避免 的生成,实验小组提出还应加入
的生成,实验小组提出还应加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为_______ ;消耗含铜元素80%的废铜屑240 kg固体时,得到653.4 kg产品,产率为_______ 。
 的反应进行研究,实验如下。
的反应进行研究,实验如下。
(1)试管①中反应的化学方程式是
(2)已知绿色是棕色和蓝色的混合色,绿色溶液变蓝是因为
 与水生成了
与水生成了 和
和(3)对比③和⑤中现象,为探究③中立即产生气泡的原因,实验小组提出如下假设,并设计实验验证。
假设1:
 对该反应有催化作用。
对该反应有催化作用。假设2:
 对该反应有催化作用。
对该反应有催化作用。假设3:
 对该反应有催化作用。
对该反应有催化作用。| 序号 | 实验操作 | 实验现象 | 结论 |
| 3 | 向④中溶液加入少量 | 溶液蓝色加深,无其他明显现象 | 假设1不成立 |
| 4 | 铜片表面立即产生气泡 | 假设2成立 | |
| 5 | 向②中溶液通入少量 | 无明显变化 | |
| 6 | 向④中溶液加入少量 | 铜片表面立即产生气泡 | 假设3成立 |
(5)某工厂用硝酸溶解废铜屑制备
 ,为避免
,为避免 的生成,实验小组提出还应加入
的生成,实验小组提出还应加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为
您最近一年使用:0次
2023-05-04更新
|
602次组卷
|
10卷引用:河北省部分学校2023-2024学年上学期高三七调考试化学试题
河北省部分学校2023-2024学年上学期高三七调考试化学试题福建省龙岩市一级校2022-2023学年高三上学期期末联考化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)物质含量的测定辽宁省部分县级重点中学2023-2024学年高三上学期11月期中考试化学试题广东省佛山市2023-2024学年高三上学期12月月考化学试题广东省深圳外国语学校(集团)高中部 2023-2024学年高三上学期第四次月考化学试题广东省深圳市福田区福田中学2023-2024学年高三上学期12月月考化学考试甘肃省平凉市静宁县文萃中学2023-2024学年高三上学期第三次模拟考试化学试题(已下线)T12-实验综合题
名校
解题方法
5 . 某实验小组利用微型实验装置进行氯气的制备和性质探究,装置如图所示,下列有关说法错误的是
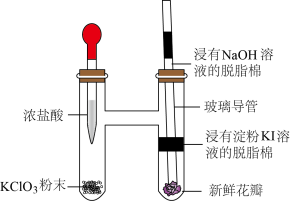
A. 与浓盐酸反应,HCl只体现还原性 与浓盐酸反应,HCl只体现还原性 |
B.浸有淀粉KI溶液的脱脂棉变蓝,说明氧化性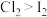 |
| C.新鲜花瓣褪色是因为氯气与水反应生成的HClO有漂白性 |
| D.浸有NaOH溶液的脱脂棉可吸收过量氯气 |
您最近一年使用:0次
2023-04-27更新
|
707次组卷
|
3卷引用:河北省邯郸市大名县第一中学2022-2023学年高二下学期6月月考化学试题
6 . 某实验小组要定量探究铁锈蚀的因素,设计如图所示实验装置,检查气密性,将5 g铁粉和2 g碳粉加入三颈烧瓶, 时刻,加入2 mL饱和氯化钠溶液后,再将一只装有5 mL稀盐酸的注射器插到烧瓶上,采集数据。下列说法错误的是
时刻,加入2 mL饱和氯化钠溶液后,再将一只装有5 mL稀盐酸的注射器插到烧瓶上,采集数据。下列说法错误的是

 时刻,加入2 mL饱和氯化钠溶液后,再将一只装有5 mL稀盐酸的注射器插到烧瓶上,采集数据。下列说法错误的是
时刻,加入2 mL饱和氯化钠溶液后,再将一只装有5 mL稀盐酸的注射器插到烧瓶上,采集数据。下列说法错误的是
| A.铁发生锈蚀的反应是放热反应 |
B. 温度降低是因为反应速率减慢了 温度降低是因为反应速率减慢了 |
| C.BC段压强减小是因为铁和氧气直接反应生成了氧化铁 |
D.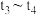 压强变大是因为发生了铁的析氢腐蚀 压强变大是因为发生了铁的析氢腐蚀 |
您最近一年使用:0次
2023-04-11更新
|
894次组卷
|
3卷引用:河北省保定市2023届一模考试化学试题
名校
解题方法
7 . 实验室用如下图所示装置探究 与
与 溶液的反应(实验前先通入
溶液的反应(实验前先通入 排除装置中的空气)。下列说法不正确的是
排除装置中的空气)。下列说法不正确的是
 与
与 溶液的反应(实验前先通入
溶液的反应(实验前先通入 排除装置中的空气)。下列说法不正确的是
排除装置中的空气)。下列说法不正确的是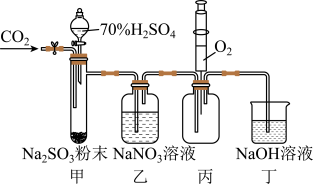
A.用装置甲产生 |
B.装置乙中无明显现象,则 与 与 未发生反应 未发生反应 |
C.装置丙中注入 ,产生红棕色气体,说明装置乙中 ,产生红棕色气体,说明装置乙中 发生了氧化反应 发生了氧化反应 |
| D.装置丁吸收尾气并防止空气进入装置丙 |
您最近一年使用:0次
2023-03-23更新
|
1382次组卷
|
7卷引用:专题12 化学实验基础
解题方法
8 . 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
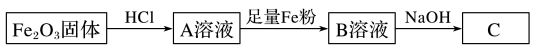
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色:A_________ ,B_________ 。
(2)写出上述过程中有关反应的化学方程式: →A
→A_________ ,A→B_________ 。
(3)向B溶液中逐滴加入NaOH得到C,此过程中可观察到的现象是_________ 。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_________ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为_________ 。
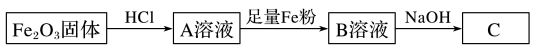
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色:A
(2)写出上述过程中有关反应的化学方程式:
 →A
→A(3)向B溶液中逐滴加入NaOH得到C,此过程中可观察到的现象是
(4)将A的饱和溶液滴入沸水中并不断加热,可制得
您最近一年使用:0次
2022-12-02更新
|
139次组卷
|
2卷引用:河北省石家庄市卓越中学2022-2023学年高一上学期期末考试化学试题
9 . 某同学用如图所示装量制取少量溴苯并证明该反应是取代反应。请回答:
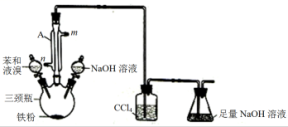
(1)仪器A的名称为____________ ,冷凝水的进水口为_________ ,(填“m”或“n”)。
(2)制取溴苯的化学方程式为___________________ 。
(3)锥形瓶中足量NaOH溶液的作用是_________ 。
(4)从实验安全的角度分析,该实验装置存在一处明显的缺陷请指出_________ 。
(5)反应结束后向三颈瓶中滴加氢氧化钠溶液,充分振荡,然后用__________ (填仪器名称)分离出溴苯(仍含有少量苯)。
(6)设计实验证明制取溴苯的反应是取代反应___________________ 。

(1)仪器A的名称为
(2)制取溴苯的化学方程式为
(3)锥形瓶中足量NaOH溶液的作用是
(4)从实验安全的角度分析,该实验装置存在一处明显的缺陷请指出
(5)反应结束后向三颈瓶中滴加氢氧化钠溶液,充分振荡,然后用
(6)设计实验证明制取溴苯的反应是取代反应
您最近一年使用:0次
2018-06-30更新
|
224次组卷
|
4卷引用:河北省河间市第十四中学2022-2023学年高一下学期5月月考化学试题



