1 . CH4、C2H4是重要的化工原料。回答下列问题:
(1) CH4的空间结构为______ ,反应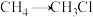 的化学方程式为
的化学方程式为______ 。
(2)实验室制备了一瓶C2H4(含少量SO2),设计如图实验验证C2H4的部分化学性质。______ ,装置B的作用为______ ,装置C的作用为______ 。
②装置D中反应的化学方程式为______ ,反应类型为______ 。
(3) 与C2H4化学性质相似,一定条件下由
与C2H4化学性质相似,一定条件下由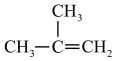 制备
制备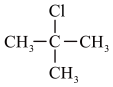 的化学方程式为
的化学方程式为______ ,该反应副产物的结构简式为______ 。
(1) CH4的空间结构为
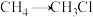 的化学方程式为
的化学方程式为(2)实验室制备了一瓶C2H4(含少量SO2),设计如图实验验证C2H4的部分化学性质。
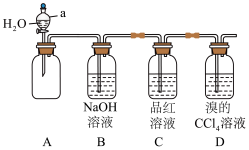
②装置D中反应的化学方程式为
(3)
 与C2H4化学性质相似,一定条件下由
与C2H4化学性质相似,一定条件下由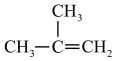 制备
制备 的化学方程式为
的化学方程式为
您最近一年使用:0次
名校
解题方法
2 . 下列各组实验中,实验操作、现象及结论或解释均正确的是
| 选项 | 实验操作 | 实验现象 | 结论或解释 |
| A | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 溶液中含Na元素 |
| B | 在干冰中央挖一个小穴,撒一些镁粉,用红热的铁棒把镁引燃,盖上另一块干冰 | 镁粉在干冰中继续燃烧,发出耀眼的白光 | CO2不能扑灭金属镁引起的火灾 |
| C | 向K2S溶液中通入足量的CO2,然后将产生的气体导入CuSO4溶液中 | CuSO4溶液中产生黑色沉淀 | Ka1(H2S)>Ka1(H2CO3) |
| D | 向蔗糖中加入适量浓硫酸,搅拌 | 产生黑色“面包” | 浓硫酸具有酸性和吸水性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-30更新
|
173次组卷
|
2卷引用:广东省深圳市光明区高级中学2023-2024学年高三下学期5月模拟考试化学试题
解题方法
3 . I、回答下列问题
(1)以太阳能为热源,利用纳米级 可获得氢气,过程如图所示,整个过程的催化剂为
可获得氢气,过程如图所示,整个过程的催化剂为___________ (填名称);过程I的化学方程式为___________ ;反应中生成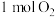 ,则同时生成
,则同时生成
___________ L(标准状况下)。
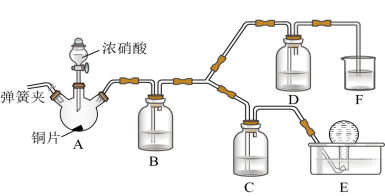
(2)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为___________ 。
②装置A中发生反应的化学方程式为___________ ;装置B的作用为___________ 。
③装置D中的现象为___________ ;C中盛放的试剂为___________ 。
(3)在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为___________ 。
(1)以太阳能为热源,利用纳米级
 可获得氢气,过程如图所示,整个过程的催化剂为
可获得氢气,过程如图所示,整个过程的催化剂为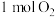 ,则同时生成
,则同时生成

(2)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为
②装置A中发生反应的化学方程式为
③装置D中的现象为
(3)在碱性条件下,
 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为
您最近一年使用:0次
解题方法
4 . 某化学兴趣小组为探究 的性质,按下图装置进行实验。回答下列问题:
的性质,按下图装置进行实验。回答下列问题:_______ ,A中发生反应的化学方程式为_______ 。
(2)B中出现淡黄色沉淀,则证明 具有
具有______ 性,发生反应的化学方程式为______ 。
(3)装置B、C、D中能够证明 具有还原性的是
具有还原性的是____ (填字母),观察到的现象为____ 。
(4)当反应进行一段时间后,装置E中最终生成少量红色沉淀,为确定红色沉淀的成分,进行以下实验:_______ (填“只有Cu”“只有 ”或“Cu和
”或“Cu和 的混合物”);E中出现少量红色沉淀的总反应的离子方程式为
的混合物”);E中出现少量红色沉淀的总反应的离子方程式为_______ 。
(5)在三颈烧瓶中加入 溶液和
溶液和 溶液,在加热条件下通入
溶液,在加热条件下通入 充分反应生成
充分反应生成 ,将含
,将含 的溶液进行结晶,可得到
的溶液进行结晶,可得到 晶体样品。用
晶体样品。用 溶液测定样品的纯度,步骤如下:称取5.00g样品,用蒸馏水溶解,配成100mL样品溶液。取
溶液测定样品的纯度,步骤如下:称取5.00g样品,用蒸馏水溶解,配成100mL样品溶液。取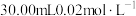 的
的 溶液,用稀硫酸酸化后加入过量KI溶液,然后滴加样品溶液至溶液呈淡黄绿色,再加入淀粉溶液作指示剂,继续滴加样品溶液,蓝色恰好完全消失时,共消耗样品溶液20.00mL。
溶液,用稀硫酸酸化后加入过量KI溶液,然后滴加样品溶液至溶液呈淡黄绿色,再加入淀粉溶液作指示剂,继续滴加样品溶液,蓝色恰好完全消失时,共消耗样品溶液20.00mL。
已知实验过程中发生的反应的计算关系式为: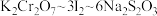 。则该样品的纯度为
。则该样品的纯度为_______ %(保留三位有效数字)。
 的性质,按下图装置进行实验。回答下列问题:
的性质,按下图装置进行实验。回答下列问题: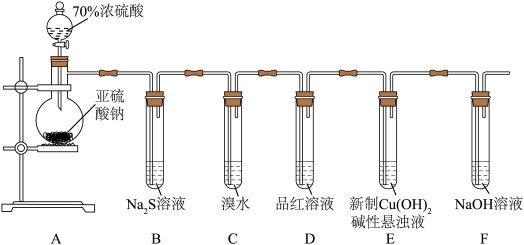
(2)B中出现淡黄色沉淀,则证明
 具有
具有(3)装置B、C、D中能够证明
 具有还原性的是
具有还原性的是(4)当反应进行一段时间后,装置E中最终生成少量红色沉淀,为确定红色沉淀的成分,进行以下实验:

 ”或“Cu和
”或“Cu和 的混合物”);E中出现少量红色沉淀的总反应的离子方程式为
的混合物”);E中出现少量红色沉淀的总反应的离子方程式为(5)在三颈烧瓶中加入
 溶液和
溶液和 溶液,在加热条件下通入
溶液,在加热条件下通入 充分反应生成
充分反应生成 ,将含
,将含 的溶液进行结晶,可得到
的溶液进行结晶,可得到 晶体样品。用
晶体样品。用 溶液测定样品的纯度,步骤如下:称取5.00g样品,用蒸馏水溶解,配成100mL样品溶液。取
溶液测定样品的纯度,步骤如下:称取5.00g样品,用蒸馏水溶解,配成100mL样品溶液。取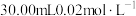 的
的 溶液,用稀硫酸酸化后加入过量KI溶液,然后滴加样品溶液至溶液呈淡黄绿色,再加入淀粉溶液作指示剂,继续滴加样品溶液,蓝色恰好完全消失时,共消耗样品溶液20.00mL。
溶液,用稀硫酸酸化后加入过量KI溶液,然后滴加样品溶液至溶液呈淡黄绿色,再加入淀粉溶液作指示剂,继续滴加样品溶液,蓝色恰好完全消失时,共消耗样品溶液20.00mL。已知实验过程中发生的反应的计算关系式为:
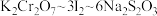 。则该样品的纯度为
。则该样品的纯度为
您最近一年使用:0次
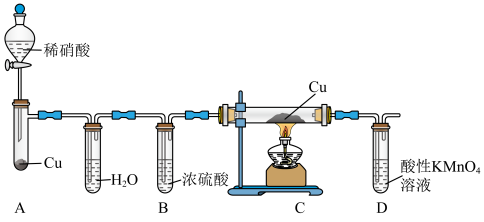
5 . 资料显示:NO和Cu反应生成CuO和N2。某小组设计如图所示的实验装置探究其真实性。
(1)装置A中盛放Cu的仪器名称是________ 。装置B的作用是_________ 。
(2)装置A中发生反应的化学方程式为_________ 。
(3)能证明NO和Cu反应的实验现象是_________ 。
(4)已知:酸性KMnO4溶液吸收NO生成Mn2+、 。实验中,观察到装置D中溶液的紫红色变浅,写出装置D中发生反应的离子方程式:
。实验中,观察到装置D中溶液的紫红色变浅,写出装置D中发生反应的离子方程式:__________ 。
(5)装置C中NO和Cu的反应中,氧化剂、还原剂的物质的量之比为__________ 。
(6)实验完毕后,过滤装置A中的混合物得到滤液,向滤液中加入适量H2O2溶液和足量NaOH溶液得到黄褐色固体M(只含Cu、O两种元素),提纯干燥后的M在惰性氛围中加热,agM完全分解生成bg黑色氧化物N,经测定:5a=6b。则加热M除生成N外,还生成的物质是________ (填化学式),M的化学式为________ 。
(1)装置A中盛放Cu的仪器名称是
(2)装置A中发生反应的化学方程式为
(3)能证明NO和Cu反应的实验现象是
(4)已知:酸性KMnO4溶液吸收NO生成Mn2+、
 。实验中,观察到装置D中溶液的紫红色变浅,写出装置D中发生反应的离子方程式:
。实验中,观察到装置D中溶液的紫红色变浅,写出装置D中发生反应的离子方程式:(5)装置C中NO和Cu的反应中,氧化剂、还原剂的物质的量之比为
(6)实验完毕后,过滤装置A中的混合物得到滤液,向滤液中加入适量H2O2溶液和足量NaOH溶液得到黄褐色固体M(只含Cu、O两种元素),提纯干燥后的M在惰性氛围中加热,agM完全分解生成bg黑色氧化物N,经测定:5a=6b。则加热M除生成N外,还生成的物质是
您最近一年使用:0次
解题方法
6 . 二氧化硫是一种使人们爱恨交加的物质,爱其作为一种化工原料,为人类提供物质基础,恨其有毒,对人类即环境的危害。联系工业生产中用碱液吸收含 制的尾气,某同学对实验室中
制的尾气,某同学对实验室中 制备与性质实验的尾气采用
制备与性质实验的尾气采用 溶液吸收,装置如下:
溶液吸收,装置如下: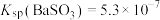 。
。
(1)利用85%的浓硫酸和 ,固体反应制备
,固体反应制备 ,下述“
,下述“ 制备装置”合理的是________。
制备装置”合理的是________。
(2) 溶液吸收
溶液吸收 后生成物与反应物的量有关,能生成
后生成物与反应物的量有关,能生成 或
或 。
。
某同学查阅资料:常温时, ,
,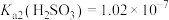 。
。
某次实验结束后,该同学通过数字实验,用pH传感器测得吸收液的 (常温),则该混合液中含硫物种物质的量浓度最大的是
(常温),则该混合液中含硫物种物质的量浓度最大的是________ (填微粒化学式)。
(3)“性质实验装置”中将 通入到
通入到 的
的 溶液中,生成白色沉淀,通过化学平衡常数计算,确定该沉淀不是
溶液中,生成白色沉淀,通过化学平衡常数计算,确定该沉淀不是 沉淀:
沉淀:________________ ;有同学结合“性质实验”反应物的组成及性质推断该沉淀为 ,若忽略空气中
,若忽略空气中 的影响,则该性质实验中生成
的影响,则该性质实验中生成 的离子方程式是
的离子方程式是________________ 。请你设计实验探究该反应的生成物是 ,而不是
,而不是 :
:________________ 。
(4)在“性质实验装置”中制备少量硫代硫酸钠( ),该装置中装有
),该装置中装有 、
、 混合液,发生的反应为
混合液,发生的反应为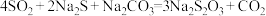 ,通入
,通入 的过程中,数字传感器测得溶液中
的过程中,数字传感器测得溶液中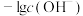 、
、 的质量变化关系如下图:
的质量变化关系如下图: 的生成量曲线为
的生成量曲线为________ (填“甲”或“乙”),曲线乙Q点后出现急剧下降的原因是________ 。
(5)化学反应速率不仅影响生产,还影响人们的生活质量,写出生活中减缓化学反应速率的一种应用________ 。
 制的尾气,某同学对实验室中
制的尾气,某同学对实验室中 制备与性质实验的尾气采用
制备与性质实验的尾气采用 溶液吸收,装置如下:
溶液吸收,装置如下: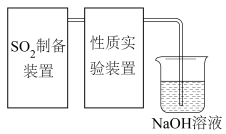
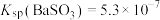 。
。(1)利用85%的浓硫酸和
 ,固体反应制备
,固体反应制备 ,下述“
,下述“ 制备装置”合理的是________。
制备装置”合理的是________。A.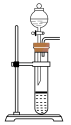 | B. | C.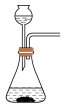 | D.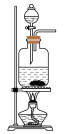 |
(2)
 溶液吸收
溶液吸收 后生成物与反应物的量有关,能生成
后生成物与反应物的量有关,能生成 或
或 。
。某同学查阅资料:常温时,
 ,
,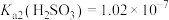 。
。某次实验结束后,该同学通过数字实验,用pH传感器测得吸收液的
 (常温),则该混合液中含硫物种物质的量浓度最大的是
(常温),则该混合液中含硫物种物质的量浓度最大的是(3)“性质实验装置”中将
 通入到
通入到 的
的 溶液中,生成白色沉淀,通过化学平衡常数计算,确定该沉淀不是
溶液中,生成白色沉淀,通过化学平衡常数计算,确定该沉淀不是 沉淀:
沉淀: ,若忽略空气中
,若忽略空气中 的影响,则该性质实验中生成
的影响,则该性质实验中生成 的离子方程式是
的离子方程式是 ,而不是
,而不是 :
:(4)在“性质实验装置”中制备少量硫代硫酸钠(
 ),该装置中装有
),该装置中装有 、
、 混合液,发生的反应为
混合液,发生的反应为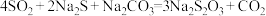 ,通入
,通入 的过程中,数字传感器测得溶液中
的过程中,数字传感器测得溶液中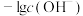 、
、 的质量变化关系如下图:
的质量变化关系如下图: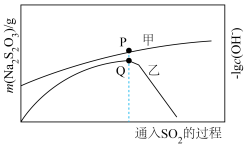
 的生成量曲线为
的生成量曲线为(5)化学反应速率不仅影响生产,还影响人们的生活质量,写出生活中减缓化学反应速率的一种应用
您最近一年使用:0次
7 . 某兴趣小组对FeSO4的一些性质进行探究实验。回答下列问题:
(1)在试管中加入少量FeSO4样品,加水溶解,滴加KSCN溶液,溶液逐渐变_____ 色,说明样品已变质。同学甲认为若要使变质的FeSO4溶液复原,可以向溶液中加入过量的Fe粉,发生反应的离子方程式为______________ 。
(2)已知FeSO4的分解产物中含有SO2和SO3。将纯净FeSO4和有关试剂放入如图所示的装置,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红棕色粉末。________________ 。
②装置C中盛放的溶液为________ ;装置D中盛放的溶液为________ (填标号)。
A.品红 B.NaOH C.BaCl2 D.浓H2SO4
③盛有NaOH溶液的装置的作用是_____________ 。
④实验时装置D中除有气泡冒出外,还可观察到的实验现象为_____________ 。
(1)在试管中加入少量FeSO4样品,加水溶解,滴加KSCN溶液,溶液逐渐变
(2)已知FeSO4的分解产物中含有SO2和SO3。将纯净FeSO4和有关试剂放入如图所示的装置,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红棕色粉末。

②装置C中盛放的溶液为
A.品红 B.NaOH C.BaCl2 D.浓H2SO4
③盛有NaOH溶液的装置的作用是
④实验时装置D中除有气泡冒出外,还可观察到的实验现象为
您最近一年使用:0次
8 . 某化学兴趣小组利用如图所示装置进行SO2的制备与性质探究的一体化实验,下列说法正确的是
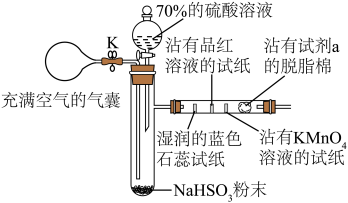
| A.分液漏斗中的硫酸溶液可用98%的浓硫酸代替以加快反应速率 |
| B.打开分液漏斗活塞一段时间后,会观察到湿润的蓝色石蕊试纸先变红后褪色 |
| C.试剂a可选择澄清石灰水以吸收多余的SO2,防止污染环境 |
| D.反应结束后,打开止水夹K并挤压气囊使装置内残留的SO2被充分吸收 |
您最近一年使用:0次
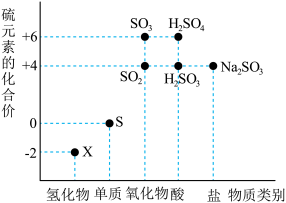
9 . 研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。回答下列问题:
Ⅰ.如图是硫元素的“价—类”二维图。______ ; 属于
属于______ (填“酸性氧化物”或“碱性氧化物”)。
(2) 的过度排放易造成硫酸型酸雨,减少酸雨的产生可采取的措施是______(填字母)。
的过度排放易造成硫酸型酸雨,减少酸雨的产生可采取的措施是______(填字母)。
(3) 易被氧化而变质,验证其已变质的实验操作及现象是
易被氧化而变质,验证其已变质的实验操作及现象是______ 。
Ⅱ.某化学兴趣小组,设计如图实验装置(夹持装置已省略),验证 的部分性质。
的部分性质。______ 。
(5)装置A中发生反应的化学方程式为______ ,该反应中氧化剂与还原剂的物质的量之比为______ 。
(6)装置B中湿润的品红溶液褪色,证明 有
有______ (填“漂白性”或“氧化性”);装置C中产生白色沉淀,该白色沉淀为______ (填化学式)。
Ⅰ.如图是硫元素的“价—类”二维图。
 属于
属于(2)
 的过度排放易造成硫酸型酸雨,减少酸雨的产生可采取的措施是______(填字母)。
的过度排放易造成硫酸型酸雨,减少酸雨的产生可采取的措施是______(填字母)。| A.把工厂烟囱造高 | B.煤使用之前先脱硫 |
| C.逐渐用新能源代替含硫煤 | D.加强空气中二氧化硫的监测 |
(3)
 易被氧化而变质,验证其已变质的实验操作及现象是
易被氧化而变质,验证其已变质的实验操作及现象是Ⅱ.某化学兴趣小组,设计如图实验装置(夹持装置已省略),验证
 的部分性质。
的部分性质。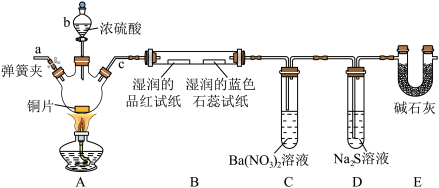
(5)装置A中发生反应的化学方程式为
(6)装置B中湿润的品红溶液褪色,证明
 有
有
您最近一年使用:0次
解题方法
10 . Ⅰ.铸铁的主要成分为Fe和C,用下图所示实验研究铸铁与热的浓硫酸的反应(夹持和加热装置已略去)。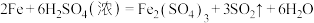 、
、________ 。
(2)实验现象:①________ ,证明确实有SO2生成。
②U型管b侧棉花的紫红色变化不明显、澄清石灰水中生成白色浑浊物。证明________ 。
(3)检测反应后A中所得溶液中含有 的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加
的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加________ ,现象为________ 证明有 。
。
(4)若取上述反应生成的0.56L(标准状况下)混合气体直接通入足量H2O2溶液中,反应完全后,向溶液中加入足量BaCl2溶液生成白色沉淀,分离、干燥后得到固体4.66g。混合气体中SO2的体积分数为________ 。
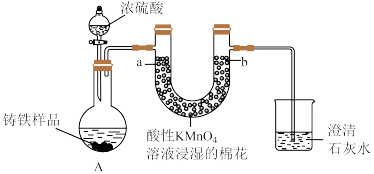
Ⅱ.纳米Fe具有很高的活性,易被氧化使其表面形成氧化层,对制备纳米Fe并对其还原去除水中的硝酸盐污染物进行研究,纳米Fe将 还原为
还原为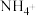 的转化关系如下:
的转化关系如下:

(5)纳米Fe制备原理: ,其中电负性H>B,反应中的氧化剂是
,其中电负性H>B,反应中的氧化剂是________ 。
(6)酸性条件下,纳米Fe和 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是________ 。
(7)检验溶液中 的操作和现象是
的操作和现象是________ 。
(8)溶液初始pH较低有利于 的去除,可能的原因是
的去除,可能的原因是________ (答1条)。
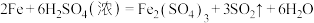 、
、(2)实验现象:①
②U型管b侧棉花的紫红色变化不明显、澄清石灰水中生成白色浑浊物。证明
(3)检测反应后A中所得溶液中含有
 的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加
的实验方法为:取少量待测溶液,将其加入适量水中稀释,滴加 。
。(4)若取上述反应生成的0.56L(标准状况下)混合气体直接通入足量H2O2溶液中,反应完全后,向溶液中加入足量BaCl2溶液生成白色沉淀,分离、干燥后得到固体4.66g。混合气体中SO2的体积分数为
Ⅱ.纳米Fe具有很高的活性,易被氧化使其表面形成氧化层,对制备纳米Fe并对其还原去除水中的硝酸盐污染物进行研究,纳米Fe将
 还原为
还原为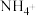 的转化关系如下:
的转化关系如下:
(5)纳米Fe制备原理:
 ,其中电负性H>B,反应中的氧化剂是
,其中电负性H>B,反应中的氧化剂是(6)酸性条件下,纳米Fe和
 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是(7)检验溶液中
 的操作和现象是
的操作和现象是(8)溶液初始pH较低有利于
 的去除,可能的原因是
的去除,可能的原因是
您最近一年使用:0次



