解题方法
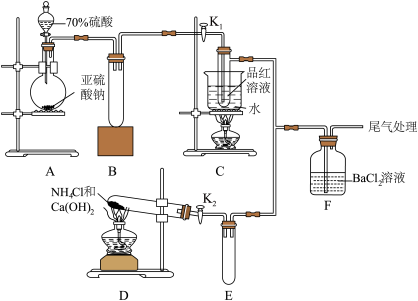
1 . 某研究性学习小组用如图所示的装置(部分夹持装置略)制取少量二氧化硫和氨气并探究其某些性质。 使
使 进入装置
进入装置 、
、 ,一段时间后停止滴加硫酸并关闭
,一段时间后停止滴加硫酸并关闭 ,打开
,打开 ,加热装置
,加热装置 ,将生成的
,将生成的 通入装置
通入装置 中,装置
中,装置 中产生白色沉淀。
中产生白色沉淀。
回答下列问题:
(1)盛放70%硫酸的仪器名称是___________ ,装置 制备
制备 时发生反应的化学方程式为
时发生反应的化学方程式为___________ 。
(2)装置 和
和 的作用相同,其作用为
的作用相同,其作用为___________ 。
(3)实验时装置 中品红溶液褪色体现了
中品红溶液褪色体现了 的
的___________ 性,若探究该反应具有不稳定性,接下来的操作及现象为___________ 。
(4)装置 中发生反应的化学方程式为
中发生反应的化学方程式为___________ ,装置F中的白色沉淀为___________ (填化学式),用化学方程式解释产生该沉淀的原因:___________ 。
 使
使 进入装置
进入装置 、
、 ,一段时间后停止滴加硫酸并关闭
,一段时间后停止滴加硫酸并关闭 ,打开
,打开 ,加热装置
,加热装置 ,将生成的
,将生成的 通入装置
通入装置 中,装置
中,装置 中产生白色沉淀。
中产生白色沉淀。回答下列问题:
(1)盛放70%硫酸的仪器名称是
 制备
制备 时发生反应的化学方程式为
时发生反应的化学方程式为(2)装置
 和
和 的作用相同,其作用为
的作用相同,其作用为(3)实验时装置
 中品红溶液褪色体现了
中品红溶液褪色体现了 的
的(4)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为
您最近一年使用:0次
解题方法
2 . 电路板广泛用于计算机、手机等电子产品中。我区某中学化学兴趣小组拟制作带有“COP15”标志的电路板并对铁及其化合物的性质进行探究。
I.制作电路板
兴趣小组同学取一小块覆铜板,用油性笔在铜板上画出“COP15”标志(图1),然后浸入 溶液(图2)。过一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板(图3)和废液。
溶液(图2)。过一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板(图3)和废液。

(1)在覆铜板上制作出“COP15”图案过程中发生反应的化学方程式为_______ 。取少量废液于试管中,滴加几滴KSCN溶液,溶液出现红色,则废液中含有_______ (填离子符号)。
II.探究铁及其化合物的性质
(2)填写下表。
III.回收废液
(3)对腐蚀废液进行回收可有效利用金属资源。一种回收利用金属铜并获得氯化铁晶体的部分工艺流程如下:
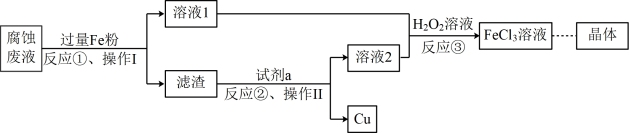
操作I为_______ ,试剂a是_______ 。反应③中加入 溶液的目的是
溶液的目的是_______ 。
I.制作电路板
兴趣小组同学取一小块覆铜板,用油性笔在铜板上画出“COP15”标志(图1),然后浸入
 溶液(图2)。过一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板(图3)和废液。
溶液(图2)。过一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板(图3)和废液。
(1)在覆铜板上制作出“COP15”图案过程中发生反应的化学方程式为
II.探究铁及其化合物的性质
(2)填写下表。
| 实验 | 实验操作 | 实验现象 | 离子方程式 | 实验结论 |
| a | 取少量废液于试管中,加入足量Fe粉 | 铁粉部分溶解,溶液呈浅绿色 | ① | ② |
| b | 取少量实验a中反应后的上层清液于试管中,滴加几滴氯水 | ③ |  |  具有还原性 具有还原性 |
III.回收废液
(3)对腐蚀废液进行回收可有效利用金属资源。一种回收利用金属铜并获得氯化铁晶体的部分工艺流程如下:

操作I为
 溶液的目的是
溶液的目的是
您最近一年使用:0次
3 . 苯酚是生产某些树脂、染料、防腐剂以及药物的重要化工原料。实验室常用氯化铁溶液检验苯酚(或酚类)。某小组为研究外界条件的改变对苯酚显色反应的影响而进行下列实验。
(一)制备无水氯化铁
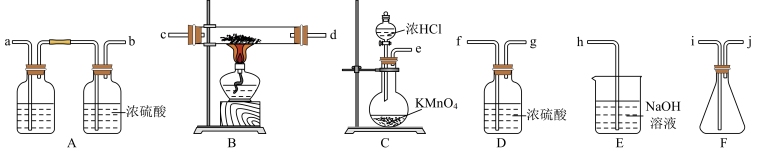
已知:FeCl3易潮解,100℃左右时升华。请利用下列装置制备无水FeCl3并回答下列问题。
(1)装置C中发生反应的化学方程式为_______ 。
(2)实验室制备无水氯化铁时,导管连接顺序为为e→_____→____c→d→____→____→_____→___→h。(填字母)_______
(二)探究外界条件的改变对苯酚显色反应的影响
已知:I.苯酚显色反应的原理为 。
。
II.苯酚易溶于苯,难溶于石油醚。石油醚无色且密度小于水。
探究有机溶剂对氯化铁的苯酚紫色混合液的影响,相关实验记录如下:
(3)x值为_______ ,结合上述实验,预测实验④中的现象为_______ 。
(4)对比实验①②的现象,颜色变化的原因为_______ ;对比实验③④的现象,颜色变化的原因为_______ 。
(5)若想探究pH对显色反应的影响,不可加入____ (填“稀盐酸”、“稀硫酸”或“硝酸”)进行调节。
(一)制备无水氯化铁

已知:FeCl3易潮解,100℃左右时升华。请利用下列装置制备无水FeCl3并回答下列问题。
(1)装置C中发生反应的化学方程式为
(2)实验室制备无水氯化铁时,导管连接顺序为为e→_____→____c→d→____→____→_____→___→h。(填字母)
(二)探究外界条件的改变对苯酚显色反应的影响
已知:I.苯酚显色反应的原理为
 。
。II.苯酚易溶于苯,难溶于石油醚。石油醚无色且密度小于水。
探究有机溶剂对氯化铁的苯酚紫色混合液的影响,相关实验记录如下:
| 序号 | 一定浓度的苯酚水溶液的体积/mL |   溶液 溶液 | 加入物质 | 实验现象 |
| ① | x | 2滴 | 无 | 溶液呈深紫色 |
| ② | 2 | 2滴 | 1mL | 溶液呈紫色 |
| ③ | 2 | 2滴 | 1mL苯 | 溶液分层,上层为无色,下层为浅紫色 |
| ④ | 2 | 2滴 | 1mL石油醚 | _______ |
(4)对比实验①②的现象,颜色变化的原因为
(5)若想探究pH对显色反应的影响,不可加入
您最近一年使用:0次
2022-07-06更新
|
311次组卷
|
2卷引用:云南省楚雄州2021-2022学年高二下学期期末考试化学试题
名校
解题方法
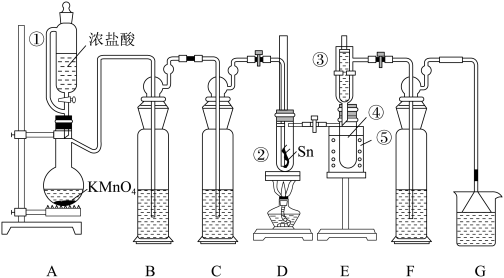
4 . 熔融的金属锡(熔点231℃)在300℃左右能直接与氯气作用生成无水四氯化锡:Sn+2Cl2 SnCl4。纯SnCl4是无色液体(沸点114℃),在空气中极易水解生成SnO2•xH2O。某化学小组利用如图装置制备SnCl4,并对其性质进行探究。
SnCl4。纯SnCl4是无色液体(沸点114℃),在空气中极易水解生成SnO2•xH2O。某化学小组利用如图装置制备SnCl4,并对其性质进行探究。
回答下列问题:
(1)装置A中烧瓶内反应的离子方程式为____ ;仪器①中导管的作用是___ 。
(2)B、C、F、G盛装的试剂应依次选用下列中的____ (填标号)。
a.浓H2SO4 b.饱和NaHCO3溶液 c.饱和NaCl溶液 d.NaOH浓溶液
(3)取少量Sn片切成丝状,放入D装置反应器②中。冷阱③和小烧杯⑤内都装入冷水,按图将仪器连接好后,再一次检验整个装置,确证系统不漏气。先打开恒压滴液漏斗活塞使反应发生,排尽装置中的空气后,再加热D装置中试管②使Sn丝熔化,并与Cl2发生反应。能说明装置中的空气被排尽的现象是____ ;生成的SnCl4经冷凝后,收集于E装置的试管④中,该液体常常呈黄绿色,原因是___ 。
(4)用玻璃棒蘸取少量产物SnCl4,放置在空气中,片刻即产生白色烟雾,产物为SnO2•xH2O和____ (填化学式)。
(5)0.500gSn完全反应,制得SnCl41.03g,产率为____ 。
 SnCl4。纯SnCl4是无色液体(沸点114℃),在空气中极易水解生成SnO2•xH2O。某化学小组利用如图装置制备SnCl4,并对其性质进行探究。
SnCl4。纯SnCl4是无色液体(沸点114℃),在空气中极易水解生成SnO2•xH2O。某化学小组利用如图装置制备SnCl4,并对其性质进行探究。
回答下列问题:
(1)装置A中烧瓶内反应的离子方程式为
(2)B、C、F、G盛装的试剂应依次选用下列中的
a.浓H2SO4 b.饱和NaHCO3溶液 c.饱和NaCl溶液 d.NaOH浓溶液
(3)取少量Sn片切成丝状,放入D装置反应器②中。冷阱③和小烧杯⑤内都装入冷水,按图将仪器连接好后,再一次检验整个装置,确证系统不漏气。先打开恒压滴液漏斗活塞使反应发生,排尽装置中的空气后,再加热D装置中试管②使Sn丝熔化,并与Cl2发生反应。能说明装置中的空气被排尽的现象是
(4)用玻璃棒蘸取少量产物SnCl4,放置在空气中,片刻即产生白色烟雾,产物为SnO2•xH2O和
(5)0.500gSn完全反应,制得SnCl41.03g,产率为
您最近一年使用:0次
2022-06-25更新
|
282次组卷
|
4卷引用:云南省昆明一中教育集团2023届高二升高三诊断性考试化学试题
名校
解题方法
5 . 化学实验是研究物质性质的主要手段,某化学兴趣小组做以下实验
I.为研究X单质的性质,特设计如图所示装置进行实验。装置III中夹持装置已略去。其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)写出装置I中发生反应的离子方程式___________ 。
(2)写出IV中发生反应的离子方程式___________ 。
II.证明过氧化钠可在呼吸面具和潜水艇中做供氧剂(C中盛放的是过氧化钠)。

(3)写出过氧化钠与二氧化碳反应的化学方程式___________
(4)D中盛放的试剂是___________
III.验证铝及化合物性质
(5)铝与碱反应的离子方程式:___________ 。
(6)偏铝酸钠中通入过量的二氧化碳方程式:___________ 。
I.为研究X单质的性质,特设计如图所示装置进行实验。装置III中夹持装置已略去。其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)写出装置I中发生反应的离子方程式
(2)写出IV中发生反应的离子方程式
II.证明过氧化钠可在呼吸面具和潜水艇中做供氧剂(C中盛放的是过氧化钠)。

(3)写出过氧化钠与二氧化碳反应的化学方程式
(4)D中盛放的试剂是
III.验证铝及化合物性质
(5)铝与碱反应的离子方程式:
(6)偏铝酸钠中通入过量的二氧化碳方程式:
您最近一年使用:0次
2022-01-05更新
|
187次组卷
|
2卷引用:云南省腾冲市第一中学2022-2023学年高一下学期期末考试化学试题
解题方法
6 . 利用如图所示装置(夹持装置省略)进行“铁与水蒸气反应”的实验。
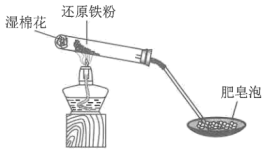
回答下列问题:
(1)湿棉花的作用是___________ 。
(2)该反应的化学方程式是___________ 。
(3)利用上述反应后的固体制备无水 ,设计流程如图所示:固体
,设计流程如图所示:固体 滤液
滤液 ……
…… 无水FeCl3
无水FeCl3
①固体和盐酸反应的化学方程式是___________ 。
②通入 的作用是
的作用是___________ 。
③ 会腐蚀钢铁设备,除
会腐蚀钢铁设备,除 作用外,另一主要原因是
作用外,另一主要原因是___________ (用离子方程式表示)。
④ 可做净水剂原因是
可做净水剂原因是___________ ,与处理中性废水相比, 处理强酸性废水的效果
处理强酸性废水的效果___________ (填“更好”“更差”或“无差别”)。

回答下列问题:
(1)湿棉花的作用是
(2)该反应的化学方程式是
(3)利用上述反应后的固体制备无水
 ,设计流程如图所示:固体
,设计流程如图所示:固体 滤液
滤液 ……
…… 无水FeCl3
无水FeCl3①固体和盐酸反应的化学方程式是
②通入
 的作用是
的作用是③
 会腐蚀钢铁设备,除
会腐蚀钢铁设备,除 作用外,另一主要原因是
作用外,另一主要原因是④
 可做净水剂原因是
可做净水剂原因是 处理强酸性废水的效果
处理强酸性废水的效果
您最近一年使用:0次
7 . 实验室利用 与浓盐酸制备干燥纯净的
与浓盐酸制备干燥纯净的 ,并进行有关氯气的性质实验,装置图如下:
,并进行有关氯气的性质实验,装置图如下:
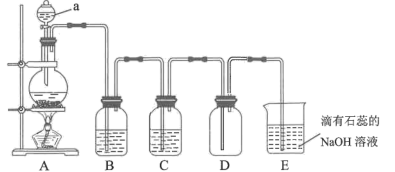
回答下列问题:
(1)写出上图中制备氯气的化学方程式_______ ,该反应中盐酸体现的化学性质是_______ 。
(2)仪器a的名称是_______ ,B装置中装有的试剂是_______ 。
(3)E中持续通入氯气可能观察到的现象是_______ 。
(4)甲同学向D装置中加入蒸馏水溶解氯气,再用强光照射氯水,同时使用数据采集器采集数据如下:
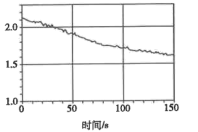
甲同学采集的数据是_______ (填字母)。
a.氯水的pH b.氯离子的浓度 c.氧气的体积分数
(5)反应结束后,乙同学为测定A装置中残余液中盐酸的浓度,设计了如下实验方案:
①配制 溶液;
溶液;
②取A装置中10mL残余液(锰离子已去除)稀释至250mL,取20mL于锥形瓶中;
③向锥形瓶中加入 溶液中和,记录所消耗NaOH溶液的体积。
溶液中和,记录所消耗NaOH溶液的体积。
乙同学3次测定所消耗的NaOH溶液的体积如下:
根据乙同学的实验数据,测得残余液中盐酸的浓度是_______  。
。
 与浓盐酸制备干燥纯净的
与浓盐酸制备干燥纯净的 ,并进行有关氯气的性质实验,装置图如下:
,并进行有关氯气的性质实验,装置图如下:
回答下列问题:
(1)写出上图中制备氯气的化学方程式
(2)仪器a的名称是
(3)E中持续通入氯气可能观察到的现象是
(4)甲同学向D装置中加入蒸馏水溶解氯气,再用强光照射氯水,同时使用数据采集器采集数据如下:

甲同学采集的数据是
a.氯水的pH b.氯离子的浓度 c.氧气的体积分数
(5)反应结束后,乙同学为测定A装置中残余液中盐酸的浓度,设计了如下实验方案:
①配制
 溶液;
溶液;②取A装置中10mL残余液(锰离子已去除)稀释至250mL,取20mL于锥形瓶中;
③向锥形瓶中加入
 溶液中和,记录所消耗NaOH溶液的体积。
溶液中和,记录所消耗NaOH溶液的体积。乙同学3次测定所消耗的NaOH溶液的体积如下:
| 测定次数 | 第1次 | 第2次 | 第3次 |
| V(NaOH)/mL | 24.00 | 24.10 | 23.90 |
 。
。
您最近一年使用:0次
8 . 应用分类的方法可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。某小同学通过实验探究Na2CO3和NaHCO3的性质,请你与他们一起完成实验探究过程,并回答问题。
[观察]
(1)Na2CO3和 NaHCO3均为_______ 色的固体,
(2)从物质的类别来看, Na2CO3和NaHCO3均属于化合物中的_______ 类,能溶于水,可与部分_______ 、_______ 、盐等类别的物质发生反应。
[实验过程]
(3)实验II试管B中的现象为_______ 。
[分析与解释]
(4)实验I所得实验数据证明,溶解时吸收热量的物质是_______ 。
(5)实验II中的现象证明,Na2CO3的热稳定性_______ (填“强”或“弱”)于NaHCO3
(6)实验III中的现象证明,Na2CO3盐酸反应是分步进行的,发生反应的离子方程式为:
第一步:CO + H+=HCO
+ H+=HCO ;第二步:
;第二步:_______ 。
[观察]
(1)Na2CO3和 NaHCO3均为
(2)从物质的类别来看, Na2CO3和NaHCO3均属于化合物中的
[实验过程]
| 编号 | 实验内容 | 实验数据或者现象 |
| 实验I | 利用传感器探究两种物质分别溶水时的温度变化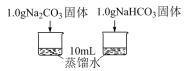 |  |
| 实验II | 探究两种物质得到热稳定性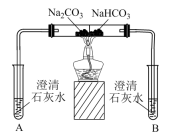 | 一段时间后,A中无明显现象,B中… |
| 实验III | 探究两种物质分别与盐酸反应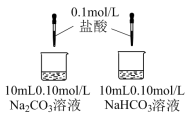 | A中开始无大量气泡,一段时间后产生大量气泡;B中立即产生大量气泡。 |
[分析与解释]
(4)实验I所得实验数据证明,溶解时吸收热量的物质是
(5)实验II中的现象证明,Na2CO3的热稳定性
(6)实验III中的现象证明,Na2CO3盐酸反应是分步进行的,发生反应的离子方程式为:
第一步:CO
 + H+=HCO
+ H+=HCO ;第二步:
;第二步:
您最近一年使用:0次
2021-07-11更新
|
701次组卷
|
5卷引用:云南省 2020-2021学年高二下学期期末普通高中学业水平考试化学试题



