名校
解题方法
1 . FeBr2是有机催化剂,易潮解。在加热条件下Fe与HBr反应可生成FeBr2。某实验小组用下列装置设计实验制备FeBr2(F的加热装置已省略)。
已知:银氨溶液中存在平衡[Ag(NH3)2]+(aq) Ag+(aq)+2NH3(aq)。
Ag+(aq)+2NH3(aq)。
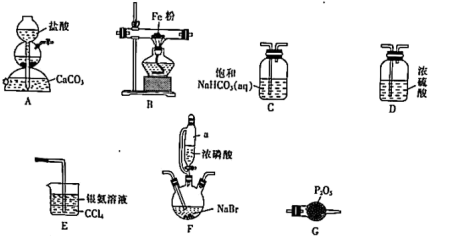
请回答下列问题:
(1)装置A的名称是___ 。
(2)气流从左到右,装置连接顺序为A→______→_____→F→______→______→E(填标号)___ 。
(3)实验中观察到装置E中银氨溶液变浑浊,其原因是____ (用必要的文字和化学用语解释)。
(4)实验室不用浓硝酸与溴化钠反应制备溴化氢,其主要原因是____ 。
(5)设计简易实验检验FeBr2中是否混有Fe单质:___ 。
(6)为了探究FeBr2的性质,设计如下实验:
取21.6gFeBr2溶于水,缓慢通入V1mLCl2 (标准状况),充分反应后,加入适量CCl4,振荡、静置。四氯化碳层呈无色,在水层中滴加KSCN溶液,溶液变红色。由此推知,还原性:Fe2+___ (填“>”“<”或“=”)Br-,V1的最大值为___ 。
(7)测定FeBr2产品纯度:取xgFeBr2产品溶于水,配成250mL溶液,取25.00mL配制的溶液,加入过量的AgNO3溶液中,充分反应后过滤、洗涤、干燥、称重,固体质量为m1g。产品纯度为____ (只列计算式)。
已知:银氨溶液中存在平衡[Ag(NH3)2]+(aq)
 Ag+(aq)+2NH3(aq)。
Ag+(aq)+2NH3(aq)。
请回答下列问题:
(1)装置A的名称是
(2)气流从左到右,装置连接顺序为A→______→_____→F→______→______→E(填标号)
(3)实验中观察到装置E中银氨溶液变浑浊,其原因是
(4)实验室不用浓硝酸与溴化钠反应制备溴化氢,其主要原因是
(5)设计简易实验检验FeBr2中是否混有Fe单质:
(6)为了探究FeBr2的性质,设计如下实验:
取21.6gFeBr2溶于水,缓慢通入V1mLCl2 (标准状况),充分反应后,加入适量CCl4,振荡、静置。四氯化碳层呈无色,在水层中滴加KSCN溶液,溶液变红色。由此推知,还原性:Fe2+
(7)测定FeBr2产品纯度:取xgFeBr2产品溶于水,配成250mL溶液,取25.00mL配制的溶液,加入过量的AgNO3溶液中,充分反应后过滤、洗涤、干燥、称重,固体质量为m1g。产品纯度为
您最近一年使用:0次
2021-10-01更新
|
172次组卷
|
3卷引用:宁夏银川市唐徕中学2024届高三下学期一模理科综合化学试题
2 . 某研究小组为探究SO2和Fe(NO3)3溶液反应的实质,设计了如图所示装置进行实验。已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1。请回答下列问题:
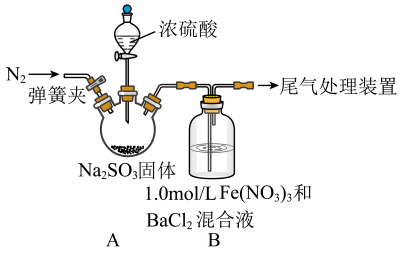
(1)装置A中用于滴加浓硫酸的仪器名称为_________ ,装置A中发生的化学方程式是________ 。
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是________________ 。
(3)装置B中产生了白色沉淀,其成分是______________ ,说明SO2具有____________ 性。
(4)分析B中产生白色沉淀的原因。
观点1:SO2与Fe3+反应;
观点2:在酸性条件下SO2与 反应。
反应。
观点3:___________________________ ;
①若观点1正确,装置B中反应的离子方程式是______________ ,证明该观点应进一步确认生成的新物质,其实验操作及现象是_______ 。
②按观点2,装置B中反应的离子方程式是___________ 。
③有人认为,如将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择最佳试剂是_________ (填字母)。
A.3.0 mol·L-1 NaNO3溶液和0.1 mol·L-1硫酸等体积混合的溶液
B.6.0 mol·L-1 NaNO3溶液和0.2 mol·L-1盐酸等体积混合的溶液
C.1.5 mol·L-1 Fe(NO3)2溶液
D.1 mol·L-1稀硝酸

(1)装置A中用于滴加浓硫酸的仪器名称为
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是
(3)装置B中产生了白色沉淀,其成分是
(4)分析B中产生白色沉淀的原因。
观点1:SO2与Fe3+反应;
观点2:在酸性条件下SO2与
 反应。
反应。观点3:
①若观点1正确,装置B中反应的离子方程式是
②按观点2,装置B中反应的离子方程式是
③有人认为,如将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择最佳试剂是
A.3.0 mol·L-1 NaNO3溶液和0.1 mol·L-1硫酸等体积混合的溶液
B.6.0 mol·L-1 NaNO3溶液和0.2 mol·L-1盐酸等体积混合的溶液
C.1.5 mol·L-1 Fe(NO3)2溶液
D.1 mol·L-1稀硝酸
您最近一年使用:0次
3 . 氯气是一种重要的化工原料.某学习小组在实验室中利用如图所示装置制取氯气并探究其性质.

(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有_____ 、_____ .
(2)装置A中盛有的试剂是:_____ ,作用是:_____ .
(3)若D中品红溶液褪色,则B装置发生反应的离子方程式是:_____ .
(4)证明FeBr2与Cl2发生了(3)中氧化还原反应的实验方法是:_____ (填操作方法).
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl﹣、OH﹣、CO32﹣和SO42﹣,对于可能存在的其他阴离子,研究小组提出以下3种假设:
假设1:只存在SO32﹣; 假设2:只存在ClO﹣; 假设3:既不存在SO32﹣,也不存在ClO﹣.
(5)学习小组判断同时存在SO32﹣和ClO﹣是不可能的,理由是:_____ .
(6)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.
a.3mol•L﹣1 H2SO4 b.0.01mol•L﹣1 KMnO4 c.1mol•L﹣1 BaCl2溶液 d.淀粉碘化钾溶液 e.酚酞试液
步骤一:取少量吸收液于试管中,滴加3mol•L﹣1 H2SO4至溶液呈中性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加少量_____ (填序号),若溶液_____ (填现象),则假设1成立.
步骤三:向B试管中滴加少量_____ (填序号),若溶液_____ (填现象),则假设2成立.

(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有
(2)装置A中盛有的试剂是:
(3)若D中品红溶液褪色,则B装置发生反应的离子方程式是:
(4)证明FeBr2与Cl2发生了(3)中氧化还原反应的实验方法是:
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl﹣、OH﹣、CO32﹣和SO42﹣,对于可能存在的其他阴离子,研究小组提出以下3种假设:
假设1:只存在SO32﹣; 假设2:只存在ClO﹣; 假设3:既不存在SO32﹣,也不存在ClO﹣.
(5)学习小组判断同时存在SO32﹣和ClO﹣是不可能的,理由是:
(6)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.
a.3mol•L﹣1 H2SO4 b.0.01mol•L﹣1 KMnO4 c.1mol•L﹣1 BaCl2溶液 d.淀粉碘化钾溶液 e.酚酞试液
步骤一:取少量吸收液于试管中,滴加3mol•L﹣1 H2SO4至溶液呈中性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加少量
步骤三:向B试管中滴加少量
您最近一年使用:0次
2010·宁夏银川·三模
4 . 为探究Cl2和SO2同时通入H2O中发生的反应,某化学兴趣小组设计了下图所示的实验装置。

(1)化学兴趣小组的同学采用Na2SO3粉末与70%的硫酸反应制取SO2气体,采用MnO2和浓盐酸反应制取Cl2。已知SO2的溶解度比Cl2大40倍,在此实验中,E仪器的作用是
________________ ;发生装置B应选择以下三种装置中的____________ (填序号)

(2)资料显示等物质的量的Cl2和SO2同时通入H2O中恰好反应生成两种酸,请写出反应的离子方程式___________________________________________ 。
(3)为了不影响产物的检验,小组成员认为上述整套装置有一处不合理,应在______ 装置之间(填代号)连接一装置,请在装置图右边的方框中画出简易装置图,并注明装置中盛有的试剂。
(4)已知干燥的SO2和Cl2在活性炭催化剂存在下反应生成液态的SO2Cl2,反应的方程式为:SO2(g)+Cl2(g) SO2Cl2(l) △H=" -" 97.3KJ/mol;SO2Cl2溶于水得到的产物与上述实验结果相同。
SO2Cl2(l) △H=" -" 97.3KJ/mol;SO2Cl2溶于水得到的产物与上述实验结果相同。
①为了提高上述反应中Cl2的平衡转化率,下列说法合理的是_________ (填序号)
②已知20℃时,AgCl的溶解度为1.5×10-4g,Ag2SO4的溶解度为0.796g,则SO2Cl2溶于水所得溶液中逐滴加入AgNO3稀溶液时,最先产生的沉淀是____________ 。

(1)化学兴趣小组的同学采用Na2SO3粉末与70%的硫酸反应制取SO2气体,采用MnO2和浓盐酸反应制取Cl2。已知SO2的溶解度比Cl2大40倍,在此实验中,E仪器的作用是

(2)资料显示等物质的量的Cl2和SO2同时通入H2O中恰好反应生成两种酸,请写出反应的离子方程式
(3)为了不影响产物的检验,小组成员认为上述整套装置有一处不合理,应在
(4)已知干燥的SO2和Cl2在活性炭催化剂存在下反应生成液态的SO2Cl2,反应的方程式为:SO2(g)+Cl2(g)
 SO2Cl2(l) △H=" -" 97.3KJ/mol;SO2Cl2溶于水得到的产物与上述实验结果相同。
SO2Cl2(l) △H=" -" 97.3KJ/mol;SO2Cl2溶于水得到的产物与上述实验结果相同。①为了提高上述反应中Cl2的平衡转化率,下列说法合理的是
| A.缩小容器体积 | B.使用催化剂 | C.增加SO2浓度 | D.升高温度 |
②已知20℃时,AgCl的溶解度为1.5×10-4g,Ag2SO4的溶解度为0.796g,则SO2Cl2溶于水所得溶液中逐滴加入AgNO3稀溶液时,最先产生的沉淀是
您最近一年使用:0次



