名校
解题方法
1 . 南宁二中“启天化学社”设计如下实验方案制备SO2 (装置图如下),并利用高中所学化学知识探究含硫化合物的相关性质。请回答下列问题:

(1)打开分液漏斗a的旋塞,浓硫酸不能顺利流下,原因可能是_______ ;加热前,圆底烧瓶中无需加入沸石,其原因是_______ 。
(2)实验室通常使用亚硫酸钠固体与70%硫酸溶液反应制备SO2,此方法与用浓硫酸与铜反应制备SO2相比,优点是:①_______ ,②_______ 。
(3)装置B的作用是_______ ,装置D的作用(请用化学方程式表示)_______ 。
(4)探究实验:向NaHSO3溶液中加入NaClO溶液时,反应有二种可能的情况:
I.NaHSO4与NaClO恰好完全反应,此时反应的离子方程式为_______ ;
II.NaHSO3过量;
III.NaClO过量。
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪种情况,请完成下表:
(已知: H2SO3;Ka1=1.54×10-2,Ka2=1.02×10-7;H2CO3:Ka1=4.3×10-7,Ka2=5.61×10-11;HClO:Ka=3×10-8)

(1)打开分液漏斗a的旋塞,浓硫酸不能顺利流下,原因可能是
(2)实验室通常使用亚硫酸钠固体与70%硫酸溶液反应制备SO2,此方法与用浓硫酸与铜反应制备SO2相比,优点是:①
(3)装置B的作用是
(4)探究实验:向NaHSO3溶液中加入NaClO溶液时,反应有二种可能的情况:
I.NaHSO4与NaClO恰好完全反应,此时反应的离子方程式为
II.NaHSO3过量;
III.NaClO过量。
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪种情况,请完成下表:
(已知: H2SO3;Ka1=1.54×10-2,Ka2=1.02×10-7;H2CO3:Ka1=4.3×10-7,Ka2=5.61×10-11;HClO:Ka=3×10-8)
| 序号 | 实验操作 | 现象 | 结论 |
| ① | 加入少量CaCO3粉末 | I或II | |
| ② | 滴加少量淀粉-KI溶液,振荡 | 溶液先变蓝后褪色 | |
| ③ | II |
您最近一年使用:0次
名校
解题方法
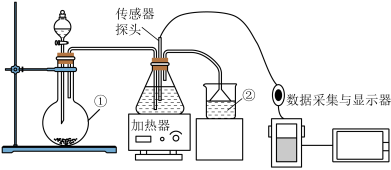
2 . 人们借助数字传感器可以进行更精准的定量实验研究。利用pH传感器研究CO2、SO2与水的反应,实验装置如图所示。
(1)CO2的电子式为___________ 。
(2)装置①的名称为___________ ,装置②中所装液体为___________ 。
(3)写出用以上装置制备SO2的化学方程式___________ 。
(4)通过pH传感器测定CO2和SO2分别溶于水后pH的变化,得到如图1;分别加热两溶液,测得pH随时间变化曲线如图2(已知在30°C101kPa下,CO2溶液度为1.26g/L;SO2溶解度为78g/L。)

①请解释图1中两溶液的pH不同的原因___________ 。
②请结合方程式解释图2中曲线④下降的原因:___________ 。
(5)利用SO2传感器来检测空气中SO2的含量,工作原理如下图所示,该装置的阴极电极反应式为:_________ 。
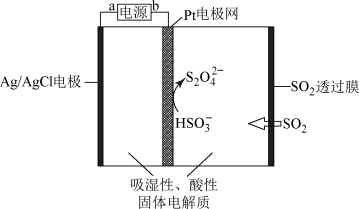
已知SO2穿过透过膜后能完全转化为 。若将标准状况下VL某待测空气通过传感器时,电路中电子转移a mol。则该空气中SO2的含量为
。若将标准状况下VL某待测空气通过传感器时,电路中电子转移a mol。则该空气中SO2的含量为___________ g/L。(用含V、a的式子表示) 。

(1)CO2的电子式为
(2)装置①的名称为
(3)写出用以上装置制备SO2的化学方程式
(4)通过pH传感器测定CO2和SO2分别溶于水后pH的变化,得到如图1;分别加热两溶液,测得pH随时间变化曲线如图2(已知在30°C101kPa下,CO2溶液度为1.26g/L;SO2溶解度为78g/L。)

①请解释图1中两溶液的pH不同的原因
②请结合方程式解释图2中曲线④下降的原因:
(5)利用SO2传感器来检测空气中SO2的含量,工作原理如下图所示,该装置的阴极电极反应式为:

已知SO2穿过透过膜后能完全转化为
 。若将标准状况下VL某待测空气通过传感器时,电路中电子转移a mol。则该空气中SO2的含量为
。若将标准状况下VL某待测空气通过传感器时,电路中电子转移a mol。则该空气中SO2的含量为
您最近一年使用:0次
3 . 硫酸铜主要用作纺织媒染剂、农业杀虫剂、杀真菌剂、防腐剂,还用于皮革鞣制、电镀铜、选矿等。回答下列有关问题:
(1)以印刷线路板的碱性蚀刻废液{主要成分为[Cu(NH3)4]Cl2)为原料制备CuSO4·5H2O晶体。取一定量蚀刻废液和稍过量的NaOH溶液加入如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气;待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体,所得固体经酸溶、结晶、过滤等操作,得到CuSO4·5H2O晶体。
①写出用蚀刻废液制备CuO反应的化学方程式:_______ 。
②检验CuO固体是否洗净的实验操作是_______ 。
③装置图中装置X的作用是_______ 。
④CuSO4溶液加热蒸干得到固体的主要成分是_______ 。
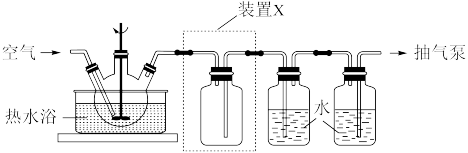
(2)为探究硫酸铜晶体的热稳定性,某学生取少量硫酸铜晶体进行实验,装置如下图所示。

观察到的实验现象:A中蓝色晶体逐渐变成白色粉末,最后变成黑色粉末;B中产生白色沉淀;D中无色溶液变红色溶液。B中用盐酸酸化的目的是_______ ;C中现象是_______ ;D中有单质参加反应的离子方程式:_______ 。
(3)通过下列方法测定产品纯度:准确称取0.5000gCuSO4·5H2O样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀硫酸酸化,以淀粉溶液为指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3的溶液19.80mL。测定过程中发生下列反应:2Cu2++4I-=2CuI↓+I2、2 +I2=
+I2= +2I-。计算CuSO4·5H2O样品的纯度:
+2I-。计算CuSO4·5H2O样品的纯度:_______ 。
(1)以印刷线路板的碱性蚀刻废液{主要成分为[Cu(NH3)4]Cl2)为原料制备CuSO4·5H2O晶体。取一定量蚀刻废液和稍过量的NaOH溶液加入如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气;待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体,所得固体经酸溶、结晶、过滤等操作,得到CuSO4·5H2O晶体。

①写出用蚀刻废液制备CuO反应的化学方程式:
②检验CuO固体是否洗净的实验操作是
③装置图中装置X的作用是
④CuSO4溶液加热蒸干得到固体的主要成分是
(2)为探究硫酸铜晶体的热稳定性,某学生取少量硫酸铜晶体进行实验,装置如下图所示。

观察到的实验现象:A中蓝色晶体逐渐变成白色粉末,最后变成黑色粉末;B中产生白色沉淀;D中无色溶液变红色溶液。B中用盐酸酸化的目的是
(3)通过下列方法测定产品纯度:准确称取0.5000gCuSO4·5H2O样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀硫酸酸化,以淀粉溶液为指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3的溶液19.80mL。测定过程中发生下列反应:2Cu2++4I-=2CuI↓+I2、2
 +I2=
+I2= +2I-。计算CuSO4·5H2O样品的纯度:
+2I-。计算CuSO4·5H2O样品的纯度:
您最近一年使用:0次
4 . 工业和居民生活向大气排放污染物使大气酸化,造成大气酸化的主要气体之一是SO2.某化学学习小组同学对SO2性质进行了探究。
(1)学习小组用图1装置制备SO2气体。_______ 。
②写出仪器A中发生反应的化学方程式_______ 。
③反应结束后,排除A瓶中残留的SO2气体,其具体操作是_______ 。
(2)学习小组用图2装置来检验SO2的性质,回答有关问题。
①甲同学欲检验SO2的漂白性,则B中应加入的试剂是_______ 。
②乙同学欲检验SO2的氧化性和还原性,分别在B、C中盛放Na2S溶液、FeCl3溶液,请描述在通入SO2气体过程中观察到的现象_______ 。
③丙同学欲检验H2SO3与HClO酸性强弱,应分别在B、C中盛放_______ (填标号)。
A.足量Ca (ClO)2溶液、Ba (OH)2溶液 B.足量NaClO、澄清石灰水
C.足量NaHCO3、NaClO溶液 D.足量NaHCO3、Ca (ClO)2溶液
(3)学习小组对Na2SO3固体的纯度进行了测定,取15. 0g Na2SO3固体样品配置成100 mL溶液,取25. 00mL放入锥形瓶中,加水稀释到50 mL,然后用1. 000 mol·L-1酸性KMnO4标准溶液进行滴定,消耗酸性KMnO4标准溶液10. 00mL。
①滴定终点的判断依据是_______ 。
②Na2SO3固体的纯度为_______ 。
(1)学习小组用图1装置制备SO2气体。

②写出仪器A中发生反应的化学方程式
③反应结束后,排除A瓶中残留的SO2气体,其具体操作是
(2)学习小组用图2装置来检验SO2的性质,回答有关问题。
①甲同学欲检验SO2的漂白性,则B中应加入的试剂是
②乙同学欲检验SO2的氧化性和还原性,分别在B、C中盛放Na2S溶液、FeCl3溶液,请描述在通入SO2气体过程中观察到的现象
③丙同学欲检验H2SO3与HClO酸性强弱,应分别在B、C中盛放
A.足量Ca (ClO)2溶液、Ba (OH)2溶液 B.足量NaClO、澄清石灰水
C.足量NaHCO3、NaClO溶液 D.足量NaHCO3、Ca (ClO)2溶液
(3)学习小组对Na2SO3固体的纯度进行了测定,取15. 0g Na2SO3固体样品配置成100 mL溶液,取25. 00mL放入锥形瓶中,加水稀释到50 mL,然后用1. 000 mol·L-1酸性KMnO4标准溶液进行滴定,消耗酸性KMnO4标准溶液10. 00mL。
①滴定终点的判断依据是
②Na2SO3固体的纯度为
您最近一年使用:0次
2022-05-24更新
|
1136次组卷
|
3卷引用:广西2022届高三第一次适应性测试理科综合化学试题
名校
解题方法
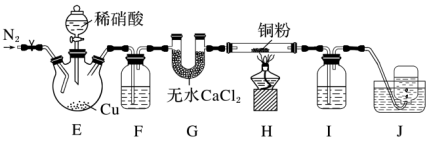
5 . 某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N2,排尽装置内的空气。 [Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法中不正确的是
[Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法中不正确的是
 [Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法中不正确的是
[Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法中不正确的是| A.装置F、I中的试剂依次为水、硫酸亚铁溶液 |
| B.若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应 |
| C.实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞 |
| D.装置J收集的气体中一定不含NO |
您最近一年使用:0次
2021-08-09更新
|
1420次组卷
|
24卷引用:【全国百强校】广西陆川县中学2018届高三下学期第二次质量检测理科综合化学试题
【全国百强校】广西陆川县中学2018届高三下学期第二次质量检测理科综合化学试题江西名校学术联盟(临川一中、景德镇一中、雁潭一中等)2018届高三教学质量检测考试(二)理综-化学试题江西省抚州市临川区第一中学2018届高三上学期教学质量检测(二)理科化学试题四川省资阳市高中2018届高三第二次诊断性考试理科综合化学试题江西省2018届高三六校联考理科综合化学试题2021年北京高考化学试题变式题1-10(已下线)黄金30题系列 高一化学 小题好拿分【提升版】(已下线)2017-2018学年第一学期期末复习备考之精准复习模拟题高三化学(理综)(B卷)(已下线)【中等生百日捷进提升系列-基础练测】专题2.15 物质的制备及实验方案设计与评价(已下线)2018年5月27日 每周一测——《每日一题》2018年高三化学四轮复习辽宁省盘锦市高级中学2017-2018学年高二下学期期末考试化学试题【全国百强校】四川省棠湖中学2019届高三上学期期末考试理综-化学试题(已下线)2019年5月26日 《每日一题》四轮复习——每周一测020届高三化学实验复习——仪器连接、实验操作顺序【选择突破】浙江省富阳中学2020-2021学年高二上学期第一次月考化学试题(已下线)【浙江新东方】42.(已下线)第14讲 氮及其化合物(精讲)-2022年一轮复习讲练测(已下线)课时23 氮及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省大庆实验中学2022届高三10月月考化学试题福建省三明市第一中学2022届高三10月月考化学试题(已下线)专题25 化学实验综合性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)福建省德化第一中学2024-2024学年高一下学期第一次月考化学试题
6 . 高氯酸铵(NH4ClO4)为白色晶体,具有不稳定性,在400 ℃时开始分解产生多种气体,常用于生产火箭推进剂。某化学兴趣小组同学利用下列装置对NH4ClO4的分解产物进行探究。(假设装置内药品均足量,部分夹持装置已省略。)
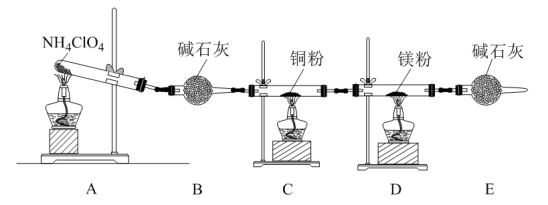
(1)在实验过程中发现C中铜粉由红色变为黑色,说明产物中有___________ (填化学式) 生成。
(2)实验完毕后,取D中硬质玻璃管中的固体物质于试管中,滴加蒸馏水,产生能使湿润的红色石蕊试纸变蓝色的气体,产生该气体的化学方程式为___________ 。
(3)某同学认为产物中还应有H2O和Cl2.该同学从理论上分析认为有Cl2存在的理由是___________ 。
(4)为了证明H2O和Cl2的存在,选择上述部分装置和下列提供的装置进行实验:
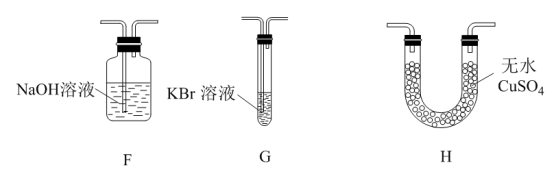
①按气流从左至右,装置的连接顺序为A→___________ 。
②实验过程中G中的现象为:___________ 。
(5)实验结论:NH4ClO4分解时产生了上述几种物质,则高氯酸铵分解的化学方程式为___________ 。
(6)在实验过程中仪器E中装有碱石灰的目的是___________ ;实验结束后,某同学拟通过称量D中镁粉质量的变化,计算高氯酸铵的分解率,会造成计算结果___________ (“偏大”“偏小”或“无法判断”) 。

(1)在实验过程中发现C中铜粉由红色变为黑色,说明产物中有
(2)实验完毕后,取D中硬质玻璃管中的固体物质于试管中,滴加蒸馏水,产生能使湿润的红色石蕊试纸变蓝色的气体,产生该气体的化学方程式为
(3)某同学认为产物中还应有H2O和Cl2.该同学从理论上分析认为有Cl2存在的理由是
(4)为了证明H2O和Cl2的存在,选择上述部分装置和下列提供的装置进行实验:

①按气流从左至右,装置的连接顺序为A→
②实验过程中G中的现象为:
(5)实验结论:NH4ClO4分解时产生了上述几种物质,则高氯酸铵分解的化学方程式为
(6)在实验过程中仪器E中装有碱石灰的目的是
您最近一年使用:0次
2021-06-15更新
|
1393次组卷
|
6卷引用:广西南宁市三中2021届高三收网题理科综合化学试题
广西南宁市三中2021届高三收网题理科综合化学试题福建省三明市第一中学2022届高三10月月考化学试题(已下线)专题10 化学实验综合—2022年高考化学二轮复习讲练测(全国版)-测试湖南省桂东县第一中学2021-2022学年高三下学期5月月考化学试题山东省临沂市罗庄区2021-2022学年高一下学期5月期中考试化学试题四川省成都市第七中学2021-2022学年高三上学期11月第三次理科综合化学试题
名校
解题方法
7 . 用如图所示装置进行下列实验,装置正确并能达到实验目的的是
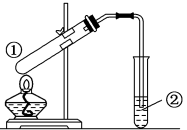

| 选项 | ①中试剂 | ②中溶液 | 实验目的 |
| A | 浓硫酸、木炭粒 | 澄清石灰水 | 检验反应生成物有CO2气体 |
| B | 乙醇、乙酸、浓硫酸 | 饱和碳酸钠溶液 | 制取乙酸乙酯 |
| C | NaHCO3(s) | 澄清石灰水 | 验证NaHCO3(s)的热稳定性 |
| D | Na2SO3(s),25%H2SO4 | 溴 水 | 验证SO2的还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
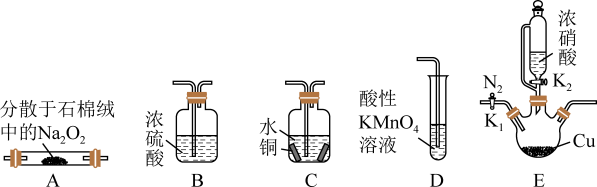
8 . 亚硝酸钠(NaNO2)是一种重要化工原料,外观酷似食盐且有咸味,是一种常用的防腐剂,其广泛存在于自然环境中,如蔬菜、肉类、豆类、腌制品等都可以测出一定量的亚硝酸钠。某化学兴趣小组设计如图所示装置(省略夹持装置)制备NaNO2并探究其性质。
已知:①2NO+Na2O2 =2NaNO2;
②NaNO2易被空气氧化,NO能被酸性高锰酸钾溶液氧化为NO ;
;
③HNO2为弱酸,室温下存在反应3HNO2=HNO3 +2NO↑+ H2O。
回答下列问题:
(1)A中盛Na2O2的玻璃仪器名称是_______ 。
(2)上述实验装置中,依据气流从左至右,装置连接顺序(可重复使用)为_______ 。
(3)连接仪器并检查气密性,检查气密性的具体操作是_______ 。
(4)打开活塞K2之前先通入氮气,其理由是_______ 。
(5)实验时观察到C中溶液变为蓝色,其离子方程式为_______ 。
(6)探究NaNO2性质:实验完毕后,甲同学取少量A中白色粉末(假设为纯净物)溶于水,并滴加几滴稀盐酸,然后加入KI淀粉溶液,溶液变蓝色,甲同学得出结论NaNO2有氧化性,乙同学认为甲同学的结论不严谨,其理由是_______ 。
(7)家里腌制的咸菜中含有一定量的亚硝酸盐,为测定咸菜中亚硝酸根离子的含量,取1 kg咸菜榨汁,将榨出的液体收集后,加入提取剂,过滤得到无色滤液,将该滤液稀释至1 L,取50. 00 mL滤液与过量的稀硫酸和碘化钾溶液的混合液反应,再滴加几滴指示剂,用0. 100 mol·L-1 Na2S2O3溶液进行滴定,共消耗20. 00 mL。计算该咸菜中亚硝酸根离子的含量为______ mg·kg-1。
已知:①2NO +4H++2I- =2NO↑ +I2 +2H2O
+4H++2I- =2NO↑ +I2 +2H2O
②I2+2Na2S2O3=2NaI+Na2S4O6

已知:①2NO+Na2O2 =2NaNO2;
②NaNO2易被空气氧化,NO能被酸性高锰酸钾溶液氧化为NO
 ;
;③HNO2为弱酸,室温下存在反应3HNO2=HNO3 +2NO↑+ H2O。
回答下列问题:
(1)A中盛Na2O2的玻璃仪器名称是
(2)上述实验装置中,依据气流从左至右,装置连接顺序(可重复使用)为
(3)连接仪器并检查气密性,检查气密性的具体操作是
(4)打开活塞K2之前先通入氮气,其理由是
(5)实验时观察到C中溶液变为蓝色,其离子方程式为
(6)探究NaNO2性质:实验完毕后,甲同学取少量A中白色粉末(假设为纯净物)溶于水,并滴加几滴稀盐酸,然后加入KI淀粉溶液,溶液变蓝色,甲同学得出结论NaNO2有氧化性,乙同学认为甲同学的结论不严谨,其理由是
(7)家里腌制的咸菜中含有一定量的亚硝酸盐,为测定咸菜中亚硝酸根离子的含量,取1 kg咸菜榨汁,将榨出的液体收集后,加入提取剂,过滤得到无色滤液,将该滤液稀释至1 L,取50. 00 mL滤液与过量的稀硫酸和碘化钾溶液的混合液反应,再滴加几滴指示剂,用0. 100 mol·L-1 Na2S2O3溶液进行滴定,共消耗20. 00 mL。计算该咸菜中亚硝酸根离子的含量为
已知:①2NO
 +4H++2I- =2NO↑ +I2 +2H2O
+4H++2I- =2NO↑ +I2 +2H2O②I2+2Na2S2O3=2NaI+Na2S4O6
您最近一年使用:0次
9 . 用下列装置进行相应实验,能达到实验目的的是


| A.用装置甲验证浓硫酸的脱水性和强氧化性 | B.用装置乙验证浓硝酸的强氧化性 |
| C.用装置丙可实现控制CO2发生和停止 | D.用装置丁验证镁片与稀盐酸反应放热 |
您最近一年使用:0次
解题方法
10 . 某实验小组设计实验制备NaHSO2·HCHO·2H2O[次硫酸氢钠甲醛(雕白块)]。回答下列问题:
⑴甲同学用下列装置制备实验原料Na2S2O5(焦亚硫酸钠),装置如图:
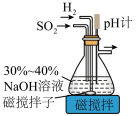
已知pH=4.1的过饱和NaHSO3溶液能自动脱水生成Na2S2O5。
①通入H2的目的是___ 。
②通入SO2发生反应的化学方程式依次为___ 、___ 和2NaHSO3=Na2S2O5↓十H2O。
③从环境保护和安全考虑,尾气处理方法正确的是___ (填字母)。
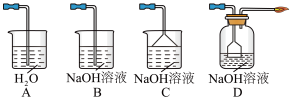
④实验若用稀NaOH溶液,则不能制得Na2S2O5,其原因是___ 。
⑵乙同学用甲同学制得的Na2S2O5通过下列装置(夹持装置已略)合成雕白块。
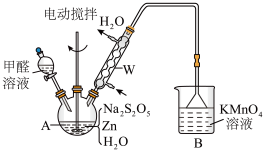
①仪器W的名称是___ 。
②合成反应温度需保持在75℃,采用的合适加热方式是___ ,已知反应中Zn转化为ZnO和Zn(OH)2,三口烧瓶中发生反应的化学方程式为___ 。
③三口烧瓶中的反应液需经过过滤、___ 、过滤、洗涤及干燥,得雕白块。
⑴甲同学用下列装置制备实验原料Na2S2O5(焦亚硫酸钠),装置如图:

已知pH=4.1的过饱和NaHSO3溶液能自动脱水生成Na2S2O5。
①通入H2的目的是
②通入SO2发生反应的化学方程式依次为
③从环境保护和安全考虑,尾气处理方法正确的是

④实验若用稀NaOH溶液,则不能制得Na2S2O5,其原因是
⑵乙同学用甲同学制得的Na2S2O5通过下列装置(夹持装置已略)合成雕白块。

①仪器W的名称是
②合成反应温度需保持在75℃,采用的合适加热方式是
③三口烧瓶中的反应液需经过过滤、
您最近一年使用:0次



