1 . 证明亚硫酸钠已经被氧化的实验方法___________
您最近一年使用:0次
2 . 为证明AgCl溶于水存在溶解平衡,取1 mo/LKCl溶液10 mL,向其中加入0.2 mol/LAgNO3溶液1 mL,充分反应后将浊液过滤进行如下实验:
已知:①AgOH不稳定,立即分解为Ag2O (棕褐色或棕黑色),Ag粉为黑色;
②AgCl、Ag2O可溶于浓氨水生成 [Ag(NH3)2]+(银氨溶液),Mg、Ag不溶于浓氨水。
(1)实验A中的滤液所属分散系为___________ 。现象ii中无色气泡是___________ (填化学式)。
(2)现象iii中,导致产生气泡的速率下降的主要原因是___________ 。
(3)判断Mg条表面的棕褐色物质中含有Ag和Ag2O。
①设计实验检验Ag:取实验A中表面变为棕褐色的Mg条于试管中,向其中加入足量稀盐酸,反应结束后,继续加入浓硝酸,产生棕色气体和白色不溶物。用离子方程式表示棕褐色固体中产生Ag的原因:___________ 。实验中加入稀盐酸的目的:___________ 。
②设计检验棕褐色物质中有Ag2O,实验方案是:取实验A中表面变为棕褐色的Mg条用蒸馏水洗净后,加入___________ (填化学式)中浸泡,取上层清液于葡萄糖溶液中,水浴加热,若有___________ (填实验现象),则证明Ag2O存在。
(4)探究AgI转化为AgCl,设计实验如下:
已知:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
①电压表读数a>b,其原因是___________ 。
②综合实验现象能说明AgI转化为AgCl,则a、b、c三者的大小关系为___________ 。
| 序号 | 实验装置 | 实验操作 | 实验现象 |
| A |  | 向滤液中放入Mg条 | ⅰ.滤液澄清透明,用激光照射有丁达尔现象。 ⅱ.放入Mg条后,立即有无色气泡产生,气体可燃,滤液中出现白色浑浊,ⅲ.一段时间后开始出现棕褐色浑浊物。Mg条表面也逐渐变为棕褐色。产生气泡的速率变缓慢 |
已知:①AgOH不稳定,立即分解为Ag2O (棕褐色或棕黑色),Ag粉为黑色;
②AgCl、Ag2O可溶于浓氨水生成 [Ag(NH3)2]+(银氨溶液),Mg、Ag不溶于浓氨水。
(1)实验A中的滤液所属分散系为
(2)现象iii中,导致产生气泡的速率下降的主要原因是
(3)判断Mg条表面的棕褐色物质中含有Ag和Ag2O。
①设计实验检验Ag:取实验A中表面变为棕褐色的Mg条于试管中,向其中加入足量稀盐酸,反应结束后,继续加入浓硝酸,产生棕色气体和白色不溶物。用离子方程式表示棕褐色固体中产生Ag的原因:
②设计检验棕褐色物质中有Ag2O,实验方案是:取实验A中表面变为棕褐色的Mg条用蒸馏水洗净后,加入
(4)探究AgI转化为AgCl,设计实验如下:
| 装置 | 步骤 | 电压表读数 |
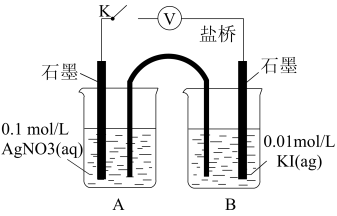 | ⅰ.如图连接装置并加入试剂,闭合K | a |
| ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | |
| ⅲ.再向B中投入一定量NaCl(s) | c | |
| ⅳ.重复ⅰ,再向B中加入与iii等量NaCl(s) | d |
已知:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
①电压表读数a>b,其原因是
②综合实验现象能说明AgI转化为AgCl,则a、b、c三者的大小关系为
您最近一年使用:0次
解题方法
3 . 某班同学用如下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)分别取一定量氯化铁、硫酸亚铁固体,均配制成0.1mol/L的溶液。请简述配制 溶液的方法:
溶液的方法:_______ 。
(2)甲组同学探究 与
与 的反应。取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L
的反应。取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L  溶液混合。分别取2mL此溶液于4支试管中进行如下实验:
溶液混合。分别取2mL此溶液于4支试管中进行如下实验:
①第一支试管中加入3滴硝酸酸化的 溶液,生成黄色沉淀;②第二支试管中加入1mL
溶液,生成黄色沉淀;②第二支试管中加入1mL  充分振荡、静置,
充分振荡、静置, 层呈紫色;
层呈紫色;
③第三支试管中加入3滴某黄色溶液,生成蓝色沉淀;
④第四支试管中加入3滴KSCN溶液,溶液变红。
实验③加入的试剂为_______ (填化学式);实验_______ (填序号)的现象可以证明该氧化还原反应为可逆反应。
(3)乙组同学设计如下实验探究亚铁盐的性质。
①实验I中由白色沉淀生成红褐色沉淀的化学方程式为_______ 。
②对实验II所得白色沉淀展开研究:
i.取II中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;
ii.向i所得溶液中滴入KSCN试剂,溶液几乎不变红;
iii.向ii溶液中再滴入少量氯水,溶液立即变为红色。
根据以上现象,实验中生成的白色沉淀的化学式为_______ 。若向ⅱ溶液中再加入少量 固体,溶液也立即变为红色。发生反应的离子方程式为
固体,溶液也立即变为红色。发生反应的离子方程式为_______ 。
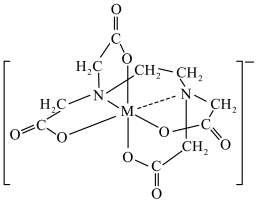
(4)丙组同学向乙组同学得到的红色溶液中滴入EDTA试剂,溶液红色立即褪去。通过查阅资料,发现可能是EDTA的配合能力比 更强,加入EDTA后,EDTA与三价铁形成了更稳定的配合物,血红色消失。该配合物阴离子的结构如图所示,图中M代表
更强,加入EDTA后,EDTA与三价铁形成了更稳定的配合物,血红色消失。该配合物阴离子的结构如图所示,图中M代表 。配合物中C、N、O元素的第一电离能由大到小的顺序为
。配合物中C、N、O元素的第一电离能由大到小的顺序为_______ , 的配位数为
的配位数为_______ 。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)分别取一定量氯化铁、硫酸亚铁固体,均配制成0.1mol/L的溶液。请简述配制
 溶液的方法:
溶液的方法:(2)甲组同学探究
 与
与 的反应。取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L
的反应。取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L  溶液混合。分别取2mL此溶液于4支试管中进行如下实验:
溶液混合。分别取2mL此溶液于4支试管中进行如下实验:①第一支试管中加入3滴硝酸酸化的
 溶液,生成黄色沉淀;②第二支试管中加入1mL
溶液,生成黄色沉淀;②第二支试管中加入1mL  充分振荡、静置,
充分振荡、静置, 层呈紫色;
层呈紫色;③第三支试管中加入3滴某黄色溶液,生成蓝色沉淀;
④第四支试管中加入3滴KSCN溶液,溶液变红。
实验③加入的试剂为
(3)乙组同学设计如下实验探究亚铁盐的性质。
| 实验方案 | 现象 | 查阅资料 | |
| I | 1.0mL0.1mol/L 溶液中滴加1.0mL 0.5mol/L NaOH溶液 溶液中滴加1.0mL 0.5mol/L NaOH溶液 | 生成白色沉淀,后沉淀基本变为红褐色 | 在溶液中不存在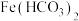 |
| II | 1.0mL 0.1mol/L  溶液中滴加1.0mL0.5mol/L 溶液中滴加1.0mL0.5mol/L  溶液 溶液 | 生成白色沉淀,后沉淀颜色几乎不变 |
②对实验II所得白色沉淀展开研究:
i.取II中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡;
ii.向i所得溶液中滴入KSCN试剂,溶液几乎不变红;
iii.向ii溶液中再滴入少量氯水,溶液立即变为红色。
根据以上现象,实验中生成的白色沉淀的化学式为
 固体,溶液也立即变为红色。发生反应的离子方程式为
固体,溶液也立即变为红色。发生反应的离子方程式为(4)丙组同学向乙组同学得到的红色溶液中滴入EDTA试剂,溶液红色立即褪去。通过查阅资料,发现可能是EDTA的配合能力比
 更强,加入EDTA后,EDTA与三价铁形成了更稳定的配合物,血红色消失。该配合物阴离子的结构如图所示,图中M代表
更强,加入EDTA后,EDTA与三价铁形成了更稳定的配合物,血红色消失。该配合物阴离子的结构如图所示,图中M代表 。配合物中C、N、O元素的第一电离能由大到小的顺序为
。配合物中C、N、O元素的第一电离能由大到小的顺序为 的配位数为
的配位数为
您最近一年使用:0次
4 .  是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备
是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备 ,并探究其有关性质。
,并探究其有关性质。
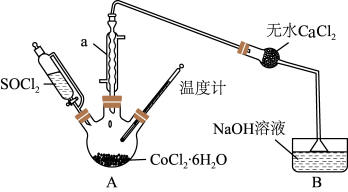
某同学向无水氯化钴中加入95%乙醇溶液,得到蓝色溶液,滴加蒸馏水溶液由蓝色变为粉红色【查阅资料得知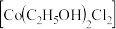 为蓝色、
为蓝色、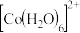 为粉红色】。资料显示变色反应为可逆反成,请选取合适试剂设计实验进行证明,简述实验方案
为粉红色】。资料显示变色反应为可逆反成,请选取合适试剂设计实验进行证明,简述实验方案_______ (可进用的试剂,浓盐酸、蒸馏水、稀硫酸)。
 是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备
是制备新能源汽车钴酸锂电池的重要原料。某化学学习小组设计如图实验装置制备 ,并探究其有关性质。
,并探究其有关性质。
某同学向无水氯化钴中加入95%乙醇溶液,得到蓝色溶液,滴加蒸馏水溶液由蓝色变为粉红色【查阅资料得知
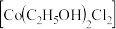 为蓝色、
为蓝色、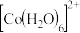 为粉红色】。资料显示变色反应为可逆反成,请选取合适试剂设计实验进行证明,简述实验方案
为粉红色】。资料显示变色反应为可逆反成,请选取合适试剂设计实验进行证明,简述实验方案
您最近一年使用:0次
5 . (一)用 和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水
和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水 ,装置如下图所示。
,装置如下图所示。
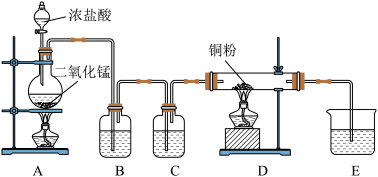
回答下列问题:
(1)写出在A中发生反应的化学方程式为:_______________________________________________
(2)B中选用的试剂是______________ ,其作用是________________________ ;C中选用的试剂是______________ ,其作用是________________________ ;E中选用的试剂是_____________ ,其作用是________________________ ;
(3)D中反应的化学方程式是________________________________________________
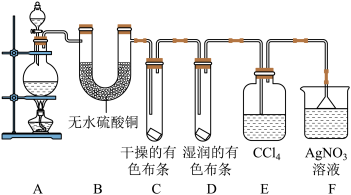
(二)某校化学实验兴趣小组为了探究在实验室制备 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
(4)若用含有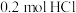 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积(标准状况下)总是小于
体积(标准状况下)总是小于 的原因是
的原因是____________________________________________________ 。
(5)①装置B的作用是_______________________________________________ ,现象是_______________________________________________ 。
②装置C和D出现的不同现象说明的问题是_______________________________________________ 。
③装置E的作用是_______________________________________________ 。
(6)乙同学认为甲同学的实验有缺陷,不能确保最终通入 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在_________ 与_________ 之间(填装置字母序号),装置中应放入____________________________________________ 。
 和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水
和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水 ,装置如下图所示。
,装置如下图所示。
回答下列问题:
(1)写出在A中发生反应的化学方程式为:
(2)B中选用的试剂是
(3)D中反应的化学方程式是
(二)某校化学实验兴趣小组为了探究在实验室制备
 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
(4)若用含有
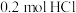 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得的
,制得的 体积(标准状况下)总是小于
体积(标准状况下)总是小于 的原因是
的原因是(5)①装置B的作用是
②装置C和D出现的不同现象说明的问题是
③装置E的作用是
(6)乙同学认为甲同学的实验有缺陷,不能确保最终通入
 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
您最近一年使用:0次
6 . 某化学小组用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。
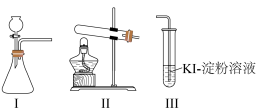
供选试剂:质量分数为30%的H2O2溶液、0.1 mol·L-1的H2SO4溶液、MnO2固体、KMnO4固体。
(1)小组同学设计甲、乙、丙三组实验,记录如下:
(2)丙实验中O2与KI溶液反应的离子方程式为___________________________________ 。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是__________ 。为进一步探究该条件对反应速率的影响,可采取的实验措施是____________________________ 。
(4)由甲、乙、丙三组实验推测,甲实验中可能是I中的白雾使溶液变蓝。为了验证推测,可将装置I中产生的气体通入_________ (填字母)溶液中,依据实验现象来证明白雾中含有H2O2。
A.酸性KMnO4B.FeCl2C.H2S
(5)资料显示:KI溶液在空气中久置的过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应___________________________________ (写离子方程式)造成的,请设计实验证明他们的猜想是否正确:___________________________________ 。

供选试剂:质量分数为30%的H2O2溶液、0.1 mol·L-1的H2SO4溶液、MnO2固体、KMnO4固体。
(1)小组同学设计甲、乙、丙三组实验,记录如下:
| 操作 | 现象 | |
| 甲 | 向装置I的锥形瓶中加入MnO2固体,向装置I的 | 装置I中产生无色气体并伴随大量白雾;装置Ⅲ中有气泡冒出,溶液迅速变蓝 |
| 乙 | 向装置Ⅱ中加入KMnO4固体,连接装置Ⅱ、Ⅲ,点燃酒精灯 | 装置Ⅲ中有气泡冒出,溶液不变蓝 |
| 丙 | 向装置Ⅱ中加入 | 装置Ⅲ中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式为
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是
(4)由甲、乙、丙三组实验推测,甲实验中可能是I中的白雾使溶液变蓝。为了验证推测,可将装置I中产生的气体通入
A.酸性KMnO4B.FeCl2C.H2S
(5)资料显示:KI溶液在空气中久置的过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应
您最近一年使用:0次
2019-12-25更新
|
548次组卷
|
2卷引用:2021年广东省高考化学试卷变式题11-21
名校
7 . 某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、酸性KMnO4溶液、MnO2。该同学取一定量Na2O2样品与过量水反应,待完全反应后,得到溶液X和一定量O2,该同学推测反应中可能生成了H2O2,并进行实验探究。
(1)写出Na2O2与水反应的化学方程式_______________________________________ 。
(2)试设计实验证明溶液X中含过氧化氢____________________________________ 。
(3)通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:______ H2O2+______ Fe2++_____ OH-===______ Fe(OH)3↓,该反应中H2O2表现了_______ (填“氧化”或“还原”)性。
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了______ (填“氧化”或“还原”)性。该反应的离子方程式为____________________ 。
(1)写出Na2O2与水反应的化学方程式
(2)试设计实验证明溶液X中含过氧化氢
(3)通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了
您最近一年使用:0次
8 . 如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞试液的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中。回答下列问题:
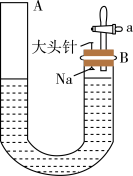
(1)钠与水反应的化学方程式为_____________ 。
(2)钠与水反应的现象有很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是_________ 。
②能证明钠的熔点低的现象是_________ 。
③能证明有氢氧化钠生成的现象是__________ 。
④能证明有气体产生的现象是A端液面________ (填“上升”“下降”或“不变”,下同),B端液面________ 。

(1)钠与水反应的化学方程式为
(2)钠与水反应的现象有很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
④能证明有气体产生的现象是A端液面
您最近一年使用:0次
2019-08-31更新
|
1847次组卷
|
15卷引用:甘肃省庄浪县阳川中学2021-2022学年高三上学期第二次月考化学试题
甘肃省庄浪县阳川中学2021-2022学年高三上学期第二次月考化学试题第二课时 研究物质性质的基本方法 练习内蒙古集宁一中(西校区)2019-2020学年高一上学期期末考试化学试题甘肃省古浪县第二中学2019-2020学年高一12月基础知识竞赛化学试题(已下线)1.2.1 研究物质性质的基本方法 练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)3.2.1 钠的性质与制备练习(1)——《高中新教材同步备课》(苏教版 必修第一册)陕西省西安市第八十五中学2019-2020学年高一上学期期末考试化学试题安徽省肥东县高级中学2020-2021学年高一上学期第二次月考化学试题湖北省黄冈市2020-2021学年高一上学期期中联考化学试题甘肃省武威市民勤县第四中学2020-2021学年高一上学期期末考试(普通班)化学试题四川省自贡市田家炳中学2020-2021学年高一下学期开学考试化学试题安徽省亳州市第五完全中学2021-2022学年高一上学期期中考试化学试题重庆市万州纯阳中学校2021-2022学年高一10月月考化学(B卷)试题广东省华南师范大学附属中学2020-2021学年高一上学期期中考试化学试题湖北省武汉海淀外国语实验学校2022-2023学年高一上学期10月月考化学试题
9 . 草酸亚铁晶体(化学组成为FeC2O4·2H2O)是一种淡黄色晶体粉末,是生产锂电池的原材料。已知FeC2O4·2H2O在300 ℃左右完全分解生成FeO、CO2、CO、H2O四种氧化物。某学习小组欲验证草酸亚铁晶体的分解产物。
I.甲组同学设计了如下实验装置:
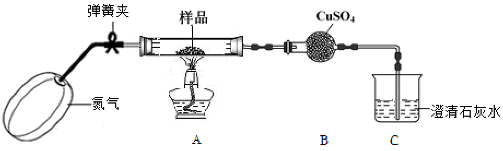
(1)实验开始前,鼓入氮气排出空气的目的是_____________________________ 。
(2)检验水和二氧化碳的装置分别是_______ 和_______ 。
(3)设计实验验证装置A中黑色残留物不含有Fe3O4_______________________________________________________________ (简要说明实验操作,现象和结论)。
II.乙组同学选用甲组实验中的装置A(接口用x表示)和下图所示的装置(可以重复选用)验证分解产物CO。

(4)乙组同学的实验装置中,依次连接的合理顺序为x→______ g→h→a(用接口字母和“→”表示)。装置G反应管中盛有的物质是氧化铜。能证明草酸晶体分解产物中有CO的现象是___________ 。
(5)按照题目提供的装置和要求设计的实验明显存在的一个不足是________________________ 。
I.甲组同学设计了如下实验装置:

(1)实验开始前,鼓入氮气排出空气的目的是
(2)检验水和二氧化碳的装置分别是
(3)设计实验验证装置A中黑色残留物不含有Fe3O4
II.乙组同学选用甲组实验中的装置A(接口用x表示)和下图所示的装置(可以重复选用)验证分解产物CO。

(4)乙组同学的实验装置中,依次连接的合理顺序为x→
(5)按照题目提供的装置和要求设计的实验明显存在的一个不足是
您最近一年使用:0次
10 . 某研究性学习小组选用以下装置进行实验设计和探究(图中a、b、c均为止水夹):
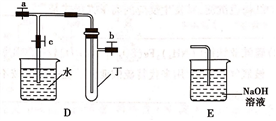
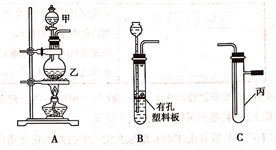
(1)在进行气体制备时,应先检验装置的气密性。将A装置中导管末端密封后,在分液漏斗甲内装一定量的蒸馏水,然后__________________________________________ ,则证明A装置的气密性良好。
(2)利用E装置能吸收的气体有__________________________________ (任写两种即可)。
(3)用锌粒和稀硫酸制备H2时应选用装置________ 作为发生装置(填所选装置的字母序号),实验时先在稀硫酸中加入少量硫酸铜晶体可使反应速率加快,原因是___________________________ 。
(4)某同学将A、C、E装置连接后设计实验比较Cl-和S2-的还原性强弱。
①A中玻璃仪器乙的名称为______________________ ,A装置中发生反应的离子方程式为
_____________________________________________ 。
②C中说明Cl-和S2-的还原性强弱的实验现象是_______________________________________ 。
(5)另一同学将B、D、E装置连接后,在B装置中加入铜片和浓硝酸,制取NO2,然后进行NO2气体与水反应的实验,并观察相关现象:
①B装置中发生反应的离子方程式为________________________________________________ 。
②反应一段时间后D装置中的具支试管丁中收集满NO2气体,若进行NO2气体与水反应的实验,应____________________________________ (填对a、b、c三个止水夹进行的操作),然后再适当加热丁。实验现象为____________________________________________________________ 。


(1)在进行气体制备时,应先检验装置的气密性。将A装置中导管末端密封后,在分液漏斗甲内装一定量的蒸馏水,然后
(2)利用E装置能吸收的气体有
(3)用锌粒和稀硫酸制备H2时应选用装置
(4)某同学将A、C、E装置连接后设计实验比较Cl-和S2-的还原性强弱。
①A中玻璃仪器乙的名称为
②C中说明Cl-和S2-的还原性强弱的实验现象是
(5)另一同学将B、D、E装置连接后,在B装置中加入铜片和浓硝酸,制取NO2,然后进行NO2气体与水反应的实验,并观察相关现象:
①B装置中发生反应的离子方程式为
②反应一段时间后D装置中的具支试管丁中收集满NO2气体,若进行NO2气体与水反应的实验,应
您最近一年使用:0次



