1 . 某小组为探究 与
与 之间的反应,进行了如下实验。
之间的反应,进行了如下实验。
已知: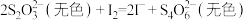 ;
; 为白色沉淀,可吸附
为白色沉淀,可吸附 ;
;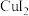 在溶液中不存在;
在溶液中不存在;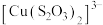 呈无色,
呈无色,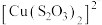 呈黄色。
呈黄色。
下列结论或推断不合理 的是
 与
与 之间的反应,进行了如下实验。
之间的反应,进行了如下实验。实验 |
|
|
现象 | ①产生土黄色沉淀,溶液为棕黄色 ②变为白色悬浊液,最后得到无色澄清溶液 | ①产生土黄色沉淀,溶液为蓝绿色 ②开始变为浅蓝色悬浊液,逐渐变为黄绿色悬浊液,然后变为黄色溶液,最后得到无色溶液 |
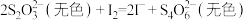 ;
; 为白色沉淀,可吸附
为白色沉淀,可吸附 ;
;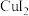 在溶液中不存在;
在溶液中不存在;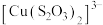 呈无色,
呈无色,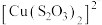 呈黄色。
呈黄色。下列结论或推断
A. 与 与 能发生反应: 能发生反应: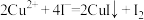 |
B. 与 与 反应的速率快于 反应的速率快于 与 与 反应的速率 反应的速率 |
C.黄绿色悬浊液变为黄色溶液时,有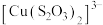 、 、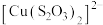 生成 生成 |
D.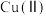 与 与 生成配合物反应的限度小于二者发生氧化还原反应的限度 生成配合物反应的限度小于二者发生氧化还原反应的限度 |
您最近一年使用:0次
名校
解题方法
2 . 下列各组实验中,实验操作、现象及结论或解释均正确的是
| 选项 | 实验操作 | 实验现象 | 结论或解释 |
| A | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 溶液中含Na元素 |
| B | 在干冰中央挖一个小穴,撒一些镁粉,用红热的铁棒把镁引燃,盖上另一块干冰 | 镁粉在干冰中继续燃烧,发出耀眼的白光 | CO2不能扑灭金属镁引起的火灾 |
| C | 向K2S溶液中通入足量的CO2,然后将产生的气体导入CuSO4溶液中 | CuSO4溶液中产生黑色沉淀 | Ka1(H2S)>Ka1(H2CO3) |
| D | 向蔗糖中加入适量浓硫酸,搅拌 | 产生黑色“面包” | 浓硫酸具有酸性和吸水性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 下列实验操作和现象所得结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 浓硫酸滴在滤纸上 | 滤纸变黑 | 浓硫酸具有脱水性 |
| B |  通入酸性 通入酸性 溶液中 溶液中 | 酸性 溶液褪色 溶液褪色 |  具有还原性 具有还原性 |
| C |
| 溴水褪色,生成白色沉淀 | 发生了加成反应 |
| D |  通入 通入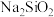 溶液 溶液 | 溶液变浑浊 |  的酸性比 的酸性比 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列关于实验的描述说法错误的是

A.图1:验证 的漂白性 的漂白性 |
| B.图2:做钠在氯气中燃烧性质实验时,先将盛有氯气的集气瓶倒扣在钠块上,后加热 |
| C.图3:用碱石灰和无水醋酸钠固体制取甲烷 |
| D.图4:配制银氨溶液要振荡试管,进行银镜实验时不能振荡试管 |
您最近一年使用:0次
5 . 某课题组为探究0.1 的
的 与
与 溶液反应,进行了如下三个实验:
溶液反应,进行了如下三个实验:
实验一:
实验二: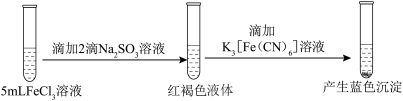
实验三: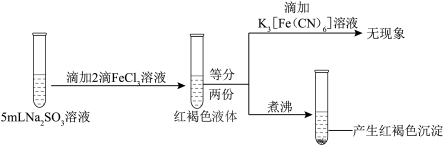
分析实验现象,下列说法中不合理的是
 的
的 与
与 溶液反应,进行了如下三个实验:
溶液反应,进行了如下三个实验:实验一:

实验二:

实验三:

分析实验现象,下列说法中不合理的是
| A.实验一的红褐色液体可产生丁达尔效应 |
B.实验二说明 既发生了水解反应也被 既发生了水解反应也被 还原 还原 |
C.实验三说明 发生了水解反应但未被还原 发生了水解反应但未被还原 |
D.以上三个实验说明 对 对 的水解无影响 的水解无影响 |
您最近一年使用:0次
6 . 按照下图进行铜与浓硫酸反应的探究实验,下列说法正确的是
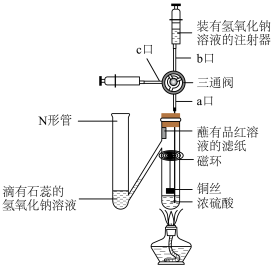
A.蘸有品红溶液的滤纸褪色,说明 具有强氧化性 具有强氧化性 |
| B.N形管溶液变为红色,说明有酸性气体进入N形管 |
| C.反应后,从c口抽取反应液加到足量的氨水中最终产生蓝色沉淀 |
| D.实验结束后从b口注入足量NaOH溶液,会有2种物质与NaOH反应 |
您最近一年使用:0次
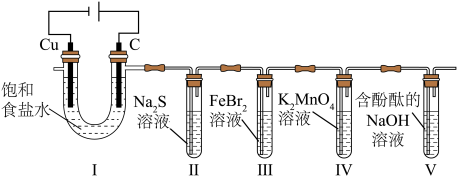
7 . 某小组利用电解原理探究一系列物质性质,装置如图所示。 呈绿色,能被氯气氧化。实验发现:Ⅱ中溶液先变浑浊,后变澄清;V中溶液由红色变无色。下列叙述正确的是
呈绿色,能被氯气氧化。实验发现:Ⅱ中溶液先变浑浊,后变澄清;V中溶液由红色变无色。下列叙述正确的是
 呈绿色,能被氯气氧化。实验发现:Ⅱ中溶液先变浑浊,后变澄清;V中溶液由红色变无色。下列叙述正确的是
呈绿色,能被氯气氧化。实验发现:Ⅱ中溶液先变浑浊,后变澄清;V中溶液由红色变无色。下列叙述正确的是| A.I中铜电极和石墨电极可以互换 |
B.用 溶液可检验Ⅱ中是否生成了 溶液可检验Ⅱ中是否生成了 |
C.Ⅲ中 最多能消耗 最多能消耗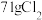 |
| D.Ⅳ中现象可能是绿色变为无色 |
您最近一年使用:0次
8 . 实验室用如图所示装置检验草酸晶体( )分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入
)分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入 的盐酸溶液中生成黑色Pd粉。下列说法错误的是
的盐酸溶液中生成黑色Pd粉。下列说法错误的是
 )分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入
)分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入 的盐酸溶液中生成黑色Pd粉。下列说法错误的是
的盐酸溶液中生成黑色Pd粉。下列说法错误的是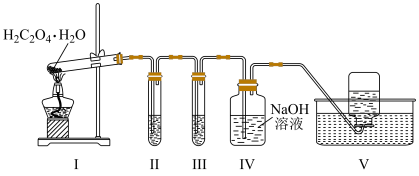
| A.Ⅰ中大试管口向上倾斜,可能因为草酸晶体的熔点低于分解温度 |
| B.由Ⅱ中现象可推断草酸晶体分解生成CO |
| C.Ⅱ、Ⅲ中现象可推断草酸晶体分解反应存在元素化合价变化 |
| D.可用燃烧法代替Ⅴ进行尾气处理 |
您最近一年使用:0次
名校
解题方法
9 . 实验小组探究溶液酸碱性对含锰化合物和 氧化还原反应的影响。
氧化还原反应的影响。
资料: .
. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。
 .
. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。
 .
. 的还原产物与溶液酸碱性有关,通常酸性条件下被还原为
的还原产物与溶液酸碱性有关,通常酸性条件下被还原为 ,中性条件下被还原为
,中性条件下被还原为 ,碱性条件下被还原为
,碱性条件下被还原为 。
。
 .
.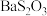 为微溶物。
为微溶物。
已知:实验 、
、 、
、 中
中 均被氧化为
均被氧化为 。下列说法不正确的是
。下列说法不正确的是
 氧化还原反应的影响。
氧化还原反应的影响。资料:
 .
. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。 .
. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。 .
. 的还原产物与溶液酸碱性有关,通常酸性条件下被还原为
的还原产物与溶液酸碱性有关,通常酸性条件下被还原为 ,中性条件下被还原为
,中性条件下被还原为 ,碱性条件下被还原为
,碱性条件下被还原为 。
。 .
. 为微溶物。
为微溶物。| 实验 | 序号 | 试剂 | 现象 |
| i.先加试剂a ii.再加试剂b
|  | a:10滴3mol/LH2SO4溶液 b:20滴0.002mol/LNa2S2O3溶液 | 溶液紫色变浅至接近无色,静置一段时间后出现乳白色浑浊 |
 | a:10滴蒸馏水 b:20滴0.002mol/LNa2S2O3溶液 | 产生棕黑色沉淀 | |
 | a:x滴6mol/LNaOH溶液 b:20滴0.002mol/LNa2S2O3溶液 | 溶液变为绿色,无沉淀生成;静置5min,绿色变浅,有棕黑色沉淀生成 |
 、
、 、
、 中
中 均被氧化为
均被氧化为 。下列说法不正确的是
。下列说法不正确的是A.实验 中出现乳白色浑浊发生反应:S2O 中出现乳白色浑浊发生反应:S2O +2H+=SO2↑+S↓+H2O +2H+=SO2↑+S↓+H2O |
B.实验 所得溶液中 所得溶液中 的检验:取少量溶液加入足量 的检验:取少量溶液加入足量 ,若有白色沉淀生成,则说明有 ,若有白色沉淀生成,则说明有 |
| C.x=10 |
D.实验 产生棕黑色沉淀可能原因是 产生棕黑色沉淀可能原因是 碱性减弱后不稳定生成 碱性减弱后不稳定生成 棕黑色沉淀 棕黑色沉淀 |
您最近一年使用:0次
10 . 按图装置进行实验。将浓硫酸全部加入Ⅰ中的试管,关闭活塞。下列说法不正确的是
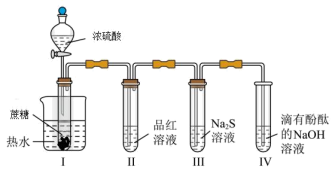
| A.Ⅰ中试管内有“黑面包”生成,说明浓硫酸体现了吸水性 |
| B.Ⅱ中品红溶液褪色,说明在Ⅰ中浓硫酸还体现了强氧化性 |
C.Ⅲ中的溶液一段时间后才会变浑浊,说明 有氧化性 有氧化性 |
| D.撤掉水浴,重做实验,Ⅳ中红色褪去变慢 |
您最近一年使用:0次



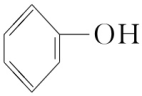 加入溴水中
加入溴水中


