解题方法
1 . 设计如下实验验证氧化性: 。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
下列说法错误的是
 。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)| 实验① | 实验② | 实验③ | 实验④ |
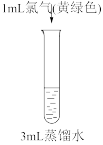 | 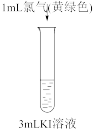 | 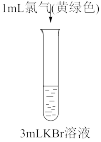 | 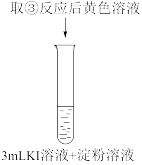 |
| 溶液变为浅黄绿色 | 溶液变为棕黄色 | 溶液变为黄色 | 溶液变为蓝色 |
A.实验①中发生反应: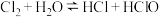 |
B.实验①②的现象可以证明氧化性: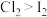 |
C.实验③发生反应: |
D.实验③④能证明氧化性: |
您最近一年使用:0次
2 . 为探究铁和硫反应产物中铁的化合价,某同学设计了如下实验过程:
Fe、S混合粉末 黑色固体
黑色固体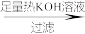 滤渣
滤渣 溶液A
溶液A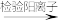 ……
……
已知:①铁和硫反应产物不溶于碱,能溶于硫酸;
②硫可溶于热碱溶液,发生类似Cl2和NaOH溶液的化学反应。
下列说法不正确的是
Fe、S混合粉末
 黑色固体
黑色固体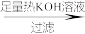 滤渣
滤渣 溶液A
溶液A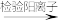 ……
……已知:①铁和硫反应产物不溶于碱,能溶于硫酸;
②硫可溶于热碱溶液,发生类似Cl2和NaOH溶液的化学反应。
下列说法不正确的是
| A.混合粉末应在N2氛围中进行加热,所用H2SO4溶液应先煮沸 |
| B.取溶液A,滴加KSCN溶液,未出现红色,可证明铁和硫反应只有+2价铁生成 |
| C.滤渣用稀H2SO4溶解时应在通风橱中进行 |
D.硫溶于热碱溶液可能发生的离子反应是3S+6OH-  2S2-+ 2S2-+ +3H2O +3H2O |
您最近一年使用:0次
解题方法
3 . 设计实验证明酸性强弱顺序:HCl> H2CO3>H2SiO3,下列说法中正确的是

| A.装置A中的分液漏斗,使用时只需打开活塞 |
| B.装置B中的药品为浓硫酸,作用是吸收挥发出的氯化氢 |
| C.该实验设计原理为强酸制弱酸 |
| D.该装置可以不设计尾气处理装置 |
您最近一年使用:0次
2021-06-22更新
|
415次组卷
|
3卷引用:山东省六校(泰安一中、菏泽一中、章丘四中、东营一中、济宁一中、聊城一中、胜利一中)2020-2021学年高一6月“山东学情”联考化学试题
山东省六校(泰安一中、菏泽一中、章丘四中、东营一中、济宁一中、聊城一中、胜利一中)2020-2021学年高一6月“山东学情”联考化学试题山东省潍坊高密市第三中学2022-2023学年高一4月月考(创新学院)化学试题(已下线)专题38 CO2与盐或碱溶液反应产物的判断-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
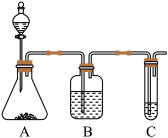
4 . 某同学用下列装置制备并检验Cl2的性质。下列说法中正确的是( )
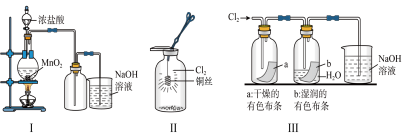

| A.Ⅰ图中如果MnO2过量,浓盐酸就可全部消耗完 |
| B.将Ⅰ图中MnO2换成浓硫酸,撤去酒精灯后可以用于制取少量HCl气体 |
| C.Ⅱ图中铜丝在氯气中燃烧,生成棕黄色的烟 |
| D.若将Ⅲ图装置直接与Ⅰ图发生装置连接,可用于证明干燥的氯气无漂白性 |
您最近一年使用:0次
2019-09-30更新
|
414次组卷
|
4卷引用:山东省菏泽市单县第五中学希望部2021-2022学年高三上学期第一次月考化学试题
山东省菏泽市单县第五中学希望部2021-2022学年高三上学期第一次月考化学试题第2章 总结与检测(1)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)专题06 氯及其化合物(核心素养卷)——【新教材精创】2019-2020学年高中化学新教材知识讲学(已下线)第2章 总结与检测(1)——《高中新教材同步备课》(鲁科版 必修第一册)
5 . 氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。

(1)能证明氯水具有漂白性的是________ (填“a”、“b”、“c”或“d”);
(2)c过程中的现象是_________________ ;d过程中的现象是__________________ ;e过程中的现象是___________________ ;b过程中的化学方程式为______________________ ;e过程的反应方程式____________________ ;
(3)久置的氯水变为______ ,用化学反应方程式表示为_______________ ;
(4)实验室保存饱和氯水的方法是_____________________ 。

(1)能证明氯水具有漂白性的是
(2)c过程中的现象是
(3)久置的氯水变为
(4)实验室保存饱和氯水的方法是
您最近一年使用:0次
6 . 回答下列问题。
(1)过氧化氢(H2O2)的水溶液俗称双氧水,双氧水是一种高效绿色消毒剂,在生活中常用作人体消毒。针对以下①~⑤四个涉及H2O2的反应。
①H2O2+2I—+2H+=I2+2H2O;
②3H2O2+2 =2MnO2↓+3O2↑+2OH—+2H2O;
=2MnO2↓+3O2↑+2OH—+2H2O;
③H2O2+2Fe2++2H+=2Fe3++2H2O;
④2H2O2 O2↑+2H2O;
O2↑+2H2O;
⑤H2O2+SO2=H2SO4
H2O2中O元素的化合价为_______ ,H2O2仅体现还原性的反应是_______ (填序号),H2O2既体现氧化性又体现还原性的反应是_______ (填字母)。
(2)为探究氯化亚铁的性质,某学习小组进行了如下探究。
①溶液配制:配制FeCl2溶液,并加入铁粉,其目的是_______ 。
②科学预测:Fe2+既有氧化性,又有还原性。
③实验探究:实验室提供了下列试剂:0.1mol·L-1FeCl2溶液,新制氯水,KSCN溶液,锌片,铜片,铁粉。根据以上试剂回答:
步骤I:向0.1mol·L-1FeCl2溶液中加入_______ ,可探究FeCl2的还原性,此现象不明显,是因反应产物浓度太低,可在反应后的溶液中再滴入_______ ,看到_______ 现象,证明Fe2+具有还原性。
步骤II:向0.1mol·L-1FeCl2溶液中加入_______ ,可证明Fe2+具有氧化性。
④性质应用:除去FeCl2溶液中少量的FeCl3需加入_______ ,除去FeCl3溶液中少量的FeCl2需加入_______ 。
(1)过氧化氢(H2O2)的水溶液俗称双氧水,双氧水是一种高效绿色消毒剂,在生活中常用作人体消毒。针对以下①~⑤四个涉及H2O2的反应。
①H2O2+2I—+2H+=I2+2H2O;
②3H2O2+2
 =2MnO2↓+3O2↑+2OH—+2H2O;
=2MnO2↓+3O2↑+2OH—+2H2O;③H2O2+2Fe2++2H+=2Fe3++2H2O;
④2H2O2
 O2↑+2H2O;
O2↑+2H2O;⑤H2O2+SO2=H2SO4
H2O2中O元素的化合价为
(2)为探究氯化亚铁的性质,某学习小组进行了如下探究。
①溶液配制:配制FeCl2溶液,并加入铁粉,其目的是
②科学预测:Fe2+既有氧化性,又有还原性。
③实验探究:实验室提供了下列试剂:0.1mol·L-1FeCl2溶液,新制氯水,KSCN溶液,锌片,铜片,铁粉。根据以上试剂回答:
步骤I:向0.1mol·L-1FeCl2溶液中加入
步骤II:向0.1mol·L-1FeCl2溶液中加入
④性质应用:除去FeCl2溶液中少量的FeCl3需加入
您最近一年使用:0次
7 . 下列实验中,利用图中装置不能达到实验目的的是
| 选项 | A | B |
| 装置 | 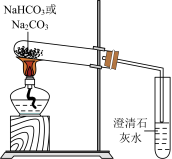 | 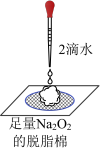 |
| 目的 | 鉴别碳酸钠和碳酸氢钠 | 证明Na2O2与水反应放热 |
| 选项 | C | D |
| 装置 |  |  |
| 目的 | 钠置换铜,金属活动性Na>Cu | 证明Cl2无漂白性,HClO有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-26更新
|
318次组卷
|
2卷引用:山东省青岛第二中学2021-2022学年高一上学期期中考试化学试题
8 . 钠、碳及它们的化合物在生产、生活中有着重要的用途。
(1)将金属钠放入CuSO4溶液中会产生蓝色沉淀,用方程式解释这一现象_______ 。
(2)利用下图,比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为_______ ,若要除去碳酸钠固体中的碳酸氢钠,发生反应的化学方程式为_______ 。

(3)在呼吸面具和潜水艇中,可用过氧化钠作供氧剂。采用下图所示实验装置进行实验,证明过氧化钠可用做供氧剂。
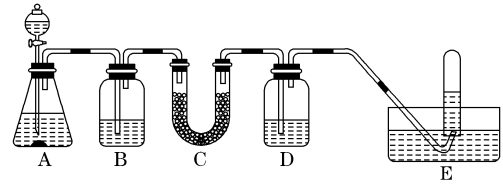
已知:A中加入碳酸钙和稀盐酸,B中加入饱和NaHCO3溶液;C中加入Na2O2,D中加入NaOH溶液,E中加入水。回答下列问题:
①B的作用是除去CO2中混有的HCl,反应的化学方程式为_______ 。
②C中Na2O2与CO2反应的化学方程式为_______ 。
③D的作用为_______ ,E中收集到的气体成分为_______ 。
(1)将金属钠放入CuSO4溶液中会产生蓝色沉淀,用方程式解释这一现象
(2)利用下图,比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为

(3)在呼吸面具和潜水艇中,可用过氧化钠作供氧剂。采用下图所示实验装置进行实验,证明过氧化钠可用做供氧剂。

已知:A中加入碳酸钙和稀盐酸,B中加入饱和NaHCO3溶液;C中加入Na2O2,D中加入NaOH溶液,E中加入水。回答下列问题:
①B的作用是除去CO2中混有的HCl,反应的化学方程式为
②C中Na2O2与CO2反应的化学方程式为
③D的作用为
您最近一年使用:0次
解题方法
9 . 钠及其化合物在人类生产生活中有着重大的作用。
(1)金属钠要隔绝空气密封保存,请用化学方程式表示原因(Na参与的反应)_______ 。
(2)加热条件下,钠可以在氧气中燃烧,现象是_______ 。
过氧化钠可用于呼吸面具中的氧气供给,某课外活动小组设计如图装置,证明二氧化碳跟过氧化钠反应时需要与水接触。

(3)装置①中反应的离子方程式是_______ 。
(4)装置②中的试剂的作用是_______ 。
(5)装置③中的试剂是_______ 。
(6)进行实验。步骤1:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。a处带火星的木条复燃的是步骤
,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。a处带火星的木条复燃的是步骤_______ (填“1”或“2”)。
(7)用单线桥表示过氧化钠跟二氧化碳反应的电子转移情况_______ 。
(1)金属钠要隔绝空气密封保存,请用化学方程式表示原因(Na参与的反应)
(2)加热条件下,钠可以在氧气中燃烧,现象是
过氧化钠可用于呼吸面具中的氧气供给,某课外活动小组设计如图装置,证明二氧化碳跟过氧化钠反应时需要与水接触。

(3)装置①中反应的离子方程式是
(4)装置②中的试剂的作用是
(5)装置③中的试剂是
(6)进行实验。步骤1:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。a处带火星的木条复燃的是步骤
,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。a处带火星的木条复燃的是步骤(7)用单线桥表示过氧化钠跟二氧化碳反应的电子转移情况
您最近一年使用:0次
名校
解题方法
10 . 用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是
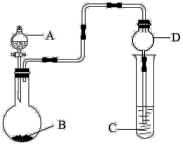

| A.若A为浓盐酸,B为Na2CO3,C中盛有Na2SiO3溶液,则C中溶液出现白色沉淀,证明非金属性:Cl > C > Si |
| B.若A为较浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液紫色褪去 |
| C.若A为较浓硫酸,B为Na2SO3固体,C中盛有Na2S溶液,则C中溶液变浑浊 |
| D.装置D起干燥气体作用 |
您最近一年使用:0次
2021-12-21更新
|
999次组卷
|
3卷引用:山东省滕州第一中学2021-2022学年高三上学期第一学段模块考试(期中)化学试题



