1 . 氧化还原反应可拆分为氧化和还原两个“半反应”,某小组同学从“半反应”的角度探究反应规律。
(1)已知: 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。
①该转化的还原半反应是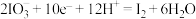 ,则相应的氧化半反应是
,则相应的氧化半反应是___________ 。
②分析上述还原半反应可知:增大 可促进
可促进 得到电子,使其
得到电子,使其___________ 性增强,进而与 发生反应。
发生反应。
(2)探究 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。
①有同学认为 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是___________ 。
用如下装置进行实验【硫酸与浓盐酸中 接近】。
接近】。
②甲实验的目的是___________ 。
③a.丙中气球变鼓是因为生成了___________ 气体(填化学式)。
b.经检测,丙中反应后溶液中存在 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:___________ 。
(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧 电极表面有
电极表面有 析出。
析出。
①该装置中左侧  电极作
电极作___________ (填“正”或“负”)极。
②写出该装置右侧 烧杯中的电极反应式___________ 。
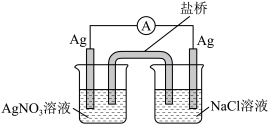
对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池__________ 。
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
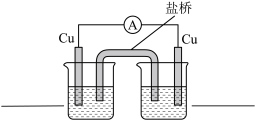
a.若能,在右装置图中填写烧杯中的试剂,并标出电子的移动方向 。
b.若不能,说明原因。
(1)已知:
 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。①该转化的还原半反应是
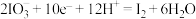 ,则相应的氧化半反应是
,则相应的氧化半反应是②分析上述还原半反应可知:增大
 可促进
可促进 得到电子,使其
得到电子,使其 发生反应。
发生反应。(2)探究
 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。①有同学认为
 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是用如下装置进行实验【硫酸与浓盐酸中
 接近】。
接近】。| 装置 | 序号 | 试管内药品 | 现象 |
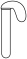 | 甲 | 浓盐酸 | 24小时后仍无明显变化 |
| 乙 |  粉+硫酸 粉+硫酸 | 24小时后仍无明显变化 | |
| 丙 |  粉+浓盐酸 粉+浓盐酸 | 24小时后气球变鼓 |
③a.丙中气球变鼓是因为生成了
b.经检测,丙中反应后溶液中存在
 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧
 电极表面有
电极表面有 析出。
析出。①该装置中
 电极作
电极作②写出该装置

对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
a.若能,在右装置图中填写烧杯中的试剂,
b.若不能,说明原因。
您最近一年使用:0次
名校
解题方法
2 . 某学习小组通过下列装置探究 与
与 能否反应产生
能否反应产生 。
。
已知:①溴水为橙色
②三氯化铁常温下为固体,熔点为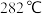 ,沸点为
,沸点为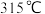 ,在
,在 以上易升华;易溶于水。
以上易升华;易溶于水。
(1)现象ⅰ中的白雾成分是___________ (化学式)。
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热 ,产生白雾和黄色气体。
,产生白雾和黄色气体。
b.用 溶液检验现象ⅱ和a中的黄色气体,溶液均变红。
溶液检验现象ⅱ和a中的黄色气体,溶液均变红。
通过该实验说明现象ⅱ中黄色气体含有___________ (化学式)。
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是___________ ,实验证实此推测成立。
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过实验进一步验证与空气无关。
(4)为进一步确认黄色气体是否含有 ,小组提出两种方案,并证实了
,小组提出两种方案,并证实了 的存在。
的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中 淀粉溶液替换为
淀粉溶液替换为 溶液,并检验反应后是否存在
溶液,并检验反应后是否存在 。现象如下:
。现象如下:
①方案1的C中盛放的试剂是___________ 。
②方案2中检验 的原因是
的原因是___________ 。
③综合方案1、2的现象,说明选择 溶液是由氧化剂氧化性的强弱决定,其氧化剂的氧化性由强到弱的顺序为
溶液是由氧化剂氧化性的强弱决定,其氧化剂的氧化性由强到弱的顺序为___________ 。
 与
与 能否反应产生
能否反应产生 。
。已知:①溴水为橙色
②三氯化铁常温下为固体,熔点为
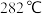 ,沸点为
,沸点为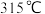 ,在
,在 以上易升华;易溶于水。
以上易升华;易溶于水。| 操作 | 现象 | 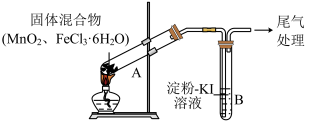 |
| 点燃酒精灯,加热 | ⅰ.A中部分固体溶解,上方出现白雾 ⅱ.稍后,产生黄色气体,管壁附着黄色液滴 ⅲ.B中溶液变蓝 |
(1)现象ⅰ中的白雾成分是
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热
 ,产生白雾和黄色气体。
,产生白雾和黄色气体。b.用
 溶液检验现象ⅱ和a中的黄色气体,溶液均变红。
溶液检验现象ⅱ和a中的黄色气体,溶液均变红。通过该实验说明现象ⅱ中黄色气体含有
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过实验进一步验证与空气无关。
(4)为进一步确认黄色气体是否含有
 ,小组提出两种方案,并证实了
,小组提出两种方案,并证实了 的存在。
的存在。方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中
 淀粉溶液替换为
淀粉溶液替换为 溶液,并检验反应后是否存在
溶液,并检验反应后是否存在 。现象如下:
。现象如下:| 方案1 | B中溶液变为蓝色 |
| 方案2 | B中溶液呈橙色;未检出 |
②方案2中检验
 的原因是
的原因是③综合方案1、2的现象,说明选择
 溶液是由氧化剂氧化性的强弱决定,其氧化剂的氧化性由强到弱的顺序为
溶液是由氧化剂氧化性的强弱决定,其氧化剂的氧化性由强到弱的顺序为
您最近一年使用:0次
2024-02-27更新
|
118次组卷
|
3卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
3 . 某研究小组同学为探究锌与硫酸反应生成 、
、 的临界浓度(浓硫酸能与锌反应生成
的临界浓度(浓硫酸能与锌反应生成 的最低浓度)设计了如图实验(加热和夹持装置已省略)。
的最低浓度)设计了如图实验(加热和夹持装置已省略)。
已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。
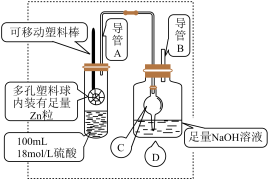
移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D装置中加入足量的 溶液,再加入足量的
溶液,再加入足量的 溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
(1)加入H₂O₂溶液发生反应的离子方程式是___________ 。
(2)浓硫酸与锌反应的临界浓度为___________ mol·L-1(用含a的计算式表示,忽略溶液体积变化)。
 、
、 的临界浓度(浓硫酸能与锌反应生成
的临界浓度(浓硫酸能与锌反应生成 的最低浓度)设计了如图实验(加热和夹持装置已省略)。
的最低浓度)设计了如图实验(加热和夹持装置已省略)。已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。

移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D装置中加入足量的
 溶液,再加入足量的
溶液,再加入足量的 溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。(1)加入H₂O₂溶液发生反应的离子方程式是
(2)浓硫酸与锌反应的临界浓度为
您最近一年使用:0次
4 . 某学习小组将酚酞试液滴入Na2O2与水反应后的溶液中,发现溶液先变红后迅速褪色,为探究原因,查阅资料后做了分析和实验。
【查阅资料】
①Na2O2与水反应先生成H2O2,然后H2O2分解;
②H2O2类似于二元弱酸,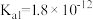 ,且具有强氧化性;
,且具有强氧化性;
③酚酞在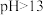 的溶液中变为无色。
的溶液中变为无色。
(1)探究一:褪色原因
【提出猜想】
假设一:反应产生的O2将酚酞氧化;
假设二:反应产生的H2O2将酚酞氧化;
假设三:NaOH溶液浓度过高导致酚酞试液褪色。
实验如下表,请填写空白:
【提出猜想】
(2)针对假设二,有同学提出还应补充实验才能证明Na2O2与水反应生成了 H2O2,则补充的实验操作为:________
(3)探究二:H2O2的性质及应用
①H2O2的酸性
用化学用语表示H2O2显酸性的原因______ 。
②H2O2的还原性
某实验用量筒量取浓H2O2溶液配制 溶液,所需玻璃仪器除量筒、烧杯、玻璃棒外,还有
溶液,所需玻璃仪器除量筒、烧杯、玻璃棒外,还有______ 。现用 酸性KMnO4液滴定所配H2O2溶液,取25.00mL H2O2溶液于锥形瓶中,完成三次实验平均消耗KMnO4标准溶液22.50mL,该反应的离子方程式为:
酸性KMnO4液滴定所配H2O2溶液,取25.00mL H2O2溶液于锥形瓶中,完成三次实验平均消耗KMnO4标准溶液22.50mL,该反应的离子方程式为:______ ,标定的H2O2溶液浓度为______  。
。
③若滴定时出现以下情况,将导致测定结果偏高的是______ 。
A.装入标准酸性KMnO4溶液时,未润洗滴定管
B.滴入最后半滴标准液出现颜色变化就立即停止滴定
C.滴定前盛标准液的滴定管尖嘴处有气泡,滴定后气泡消失
D.记录标准液体积时,滴定前仰视读数,滴定后俯视读数
【查阅资料】
①Na2O2与水反应先生成H2O2,然后H2O2分解;
②H2O2类似于二元弱酸,
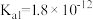 ,且具有强氧化性;
,且具有强氧化性;③酚酞在
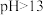 的溶液中变为无色。
的溶液中变为无色。
(1)探究一:褪色原因
【提出猜想】
假设一:反应产生的O2将酚酞氧化;
假设二:反应产生的H2O2将酚酞氧化;
假设三:NaOH溶液浓度过高导致酚酞试液褪色。
实验如下表,请填写空白:
| 实验编号 | 实验操作 | 实验现象 | 实验结论 |
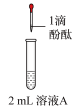
| ① | 在5mLpH=10的NaOH溶液中滴加5滴酚酞试液,再通入足量O2 | 溶液变红后不褪色 | 假设一: |
| ② | 在5mLpH=10的NaOH溶液中滴加5滴酚酞试液,再滴加1mL3%的H2O2溶液 | 假设二:成立 | |
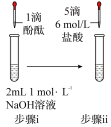
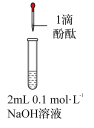
| ③ | 在5mL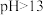 的NaOH溶液中滴加5滴酚酞试液 的NaOH溶液中滴加5滴酚酞试液 | 溶液先变红,后褪色 | 假设三:成立 |
【提出猜想】
(2)针对假设二,有同学提出还应补充实验才能证明Na2O2与水反应生成了 H2O2,则补充的实验操作为:
(3)探究二:H2O2的性质及应用
①H2O2的酸性
用化学用语表示H2O2显酸性的原因
②H2O2的还原性
某实验用量筒量取浓H2O2溶液配制
 溶液,所需玻璃仪器除量筒、烧杯、玻璃棒外,还有
溶液,所需玻璃仪器除量筒、烧杯、玻璃棒外,还有 酸性KMnO4液滴定所配H2O2溶液,取25.00mL H2O2溶液于锥形瓶中,完成三次实验平均消耗KMnO4标准溶液22.50mL,该反应的离子方程式为:
酸性KMnO4液滴定所配H2O2溶液,取25.00mL H2O2溶液于锥形瓶中,完成三次实验平均消耗KMnO4标准溶液22.50mL,该反应的离子方程式为: 。
。③若滴定时出现以下情况,将导致测定结果偏高的是
A.装入标准酸性KMnO4溶液时,未润洗滴定管
B.滴入最后半滴标准液出现颜色变化就立即停止滴定
C.滴定前盛标准液的滴定管尖嘴处有气泡,滴定后气泡消失
D.记录标准液体积时,滴定前仰视读数,滴定后俯视读数
您最近一年使用:0次
解题方法
5 . 实验小组对Mg与NH4Cl溶液的反应进行探究。
(1)用pH计测定1.0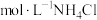 溶液约为4.6,分析NH4Cl溶液呈酸性的原因
溶液约为4.6,分析NH4Cl溶液呈酸性的原因______ (用化学用语表示)。
(2)探究镁与NH4Cl溶液的反应:实验Ⅰ、Ⅱ所取镁粉质量均为0.5g,分别加入选取的实验试剂中。
①实验Ⅰ中发生反应的化学方程式为______ 。
②经检验实验Ⅱ中刺激性气味气体为NH3和H2的混合气体,用平衡移动原理解释产生NH3的原因______ 。
③已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后的固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有______ ,灰白色固体可能是______ (填化学式)。
④针对实验Ⅱ比实验Ⅰ反应剧烈的原因,小组同学提出了两种假设:
假设l:NH4Cl溶液中的H+溶解了Mg(OH)2;
假设2:NH4Cl溶液中的 溶解了Mg(OH)2。
溶解了Mg(OH)2。
为证明假设的合理性.小组同学做了如下对比实验:
实验结论是______ 。
(3)甲同学通过深入思考,认为Mg与NH4Cl溶液反应剧烈.可能还与 有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为
有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为______ 。
(4)由上述实验得出的结论是______ 。
(1)用pH计测定1.0
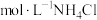 溶液约为4.6,分析NH4Cl溶液呈酸性的原因
溶液约为4.6,分析NH4Cl溶液呈酸性的原因(2)探究镁与NH4Cl溶液的反应:实验Ⅰ、Ⅱ所取镁粉质量均为0.5g,分别加入选取的实验试剂中。
实验 | 实验试剂 | 实验现象 |
Ⅰ | 5mL蒸馏水 | 反应缓慢,有少量气泡产生(经检验为H2) |
Ⅱ | 5mL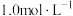 NH4Cl溶液(pH=4.6) | 剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
②经检验实验Ⅱ中刺激性气味气体为NH3和H2的混合气体,用平衡移动原理解释产生NH3的原因
③已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后的固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有
④针对实验Ⅱ比实验Ⅰ反应剧烈的原因,小组同学提出了两种假设:
假设l:NH4Cl溶液中的H+溶解了Mg(OH)2;
假设2:NH4Cl溶液中的
 溶解了Mg(OH)2。
溶解了Mg(OH)2。为证明假设的合理性.小组同学做了如下对比实验:
实验 | 实验方案 | 实验现象 |
Ⅲ | 取2根覆盖了Mg(OH)2的Mg条,分别同时放入相同体积相同pH的盐酸和饱和NH4Cl溶液中。 | 饱和NH4Cl溶液中反应更剧烈。 |
Ⅳ | 向饱和NH4Cl溶液中滴加浓氨水,使溶液呈中性或略显碱性,再放入覆盖了Mg(OH)2的镁条。 | 剧烈反应,但是比实验Ⅲ饱和NH4Cl溶液略慢,产生刺激性气味气体和灰白色难溶固体。 |
(3)甲同学通过深入思考,认为Mg与NH4Cl溶液反应剧烈.可能还与
 有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为
有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为(4)由上述实验得出的结论是
您最近一年使用:0次
2024-01-24更新
|
85次组卷
|
2卷引用:北京市顺义区2023-2024学年高二上学期期末质量监测化学试题
6 . 常温下,某小组同学用如下实验探究 的沉淀溶解平衡
的沉淀溶解平衡
已知:酚酞的变色范围:pH<8.2无色;8.2≤pH≤10.0粉红色;pH>10红色
下列说法不正确 的是
 的沉淀溶解平衡
的沉淀溶解平衡实验装置 |
| |
实验序号 | Ⅰ | Ⅱ |
| 传感器种类 | 导电率传感器 | pH传感器 |
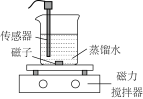
| 实验操作 | 向蒸馏水中加入足量的 粉末,一段时间后再加蒸馏水 粉末,一段时间后再加蒸馏水 | 向滴有酚酞的蒸馏水中加入 粉末,隔一段时间后,再向所得悬浊液中加入一定量稀硫酸 粉末,隔一段时间后,再向所得悬浊液中加入一定量稀硫酸 |
| 实验数据 |  | 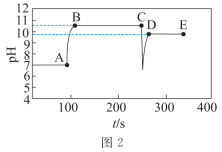 |
下列说法
A.图1中a点导电率不为0的原因是: |
B.图1中d点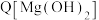 小于 小于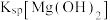 |
| C.实验Ⅱ中,溶液颜色先变红,后变为无色,最后溶液呈粉红色 |
D.实验Ⅱ中:加入 的物质的量小于加入硫酸的物质的量 的物质的量小于加入硫酸的物质的量 |
您最近一年使用:0次
2024-01-20更新
|
76次组卷
|
2卷引用:北京市顺义区2023-2024学年高二上学期期末质量监测化学试题
名校
解题方法
7 . 以海水为原料可获得钠、镁等金属及其化合物。
(1)将金属钠分别放入下列溶液中,既有气体产生,又有沉淀产生的是_____ (填序号,下同)
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④CuSO4溶液 ⑤饱和石灰水
溶液 ④CuSO4溶液 ⑤饱和石灰水
(2)某实验小组通过如图所示实验,探究 与水的反应,下列说法正确的是_____。
与水的反应,下列说法正确的是_____。

(3)某膨松剂中发挥作用的物质为碳酸氢钠,学校兴趣小组为研究该膨松剂在加热情况下放出气体的量,设计了如图所示实验(装置A、C、D、E中的试剂足量)。
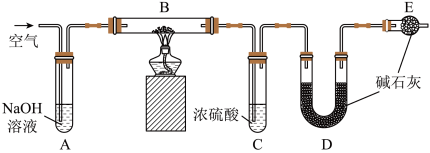
①加热前,需向装置内通入空气,用离子反应方程式解释装置A的作用_______ ,停止加热后,还需继续通入一段时间的空气,目的是_______ 。
②将一定质量的膨松剂样品装入装置B中,装置B中可能发生反应的化学反应方程式为___________ ;样品产生的二氧化碳的质量可通过测定实验前后装置_____ (填装置对应的标号)的质量测得。
③若没有装置E,可能会造成测定结果_______ (填“偏大”、“偏小”或“不变”)。
④实验测得二氧化碳的质量为13.2 g,则二氧化碳的体积(标准状况)为______ L,膨松剂样品中所含碳酸氢钠的物质的量为_____ mol。
(1)将金属钠分别放入下列溶液中,既有气体产生,又有沉淀产生的是
①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④CuSO4溶液 ⑤饱和石灰水
溶液 ④CuSO4溶液 ⑤饱和石灰水(2)某实验小组通过如图所示实验,探究
 与水的反应,下列说法正确的是_____。
与水的反应,下列说法正确的是_____。
| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
D.⑤中 的主要作用是降低了水中氧气的溶解度 的主要作用是降低了水中氧气的溶解度 |
(3)某膨松剂中发挥作用的物质为碳酸氢钠,学校兴趣小组为研究该膨松剂在加热情况下放出气体的量,设计了如图所示实验(装置A、C、D、E中的试剂足量)。

①加热前,需向装置内通入空气,用离子反应方程式解释装置A的作用
②将一定质量的膨松剂样品装入装置B中,装置B中可能发生反应的化学反应方程式为
③若没有装置E,可能会造成测定结果
④实验测得二氧化碳的质量为13.2 g,则二氧化碳的体积(标准状况)为
您最近一年使用:0次
名校
解题方法
8 . 研究小组探究 与水反应。取
与水反应。取 粉末加入到
粉末加入到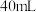 水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。
水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。
下列说法不正确的是
 与水反应。取
与水反应。取 粉末加入到
粉末加入到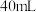 水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。
水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。编号 | ① | ② | ③ | ④ |
操作 |
|
|
|
|
现象 | 溶液变红色,20秒后褪色 | ⅰ.产生大量能使带火星木条复燃的气体 ⅱ.溶液变红色,10分钟后褪色 | ⅰ.溶液变红色,10分钟后溶液褪色 ⅱ.变红色 | 溶液变红色,2小时后无明显变化 |
A.由②中现象ⅰ可知, 与水反应有 与水反应有 生成 生成 |
B.由③、④可知,②中溶液红色褪去是因为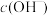 大 大 |
C.由②、③、④可知,①中溶液红色褪去的主要原因不是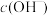 大 大 |
D.向①中褪色后的溶液中滴加5滴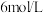 盐酸,溶液最终变成红色 盐酸,溶液最终变成红色 |
您最近一年使用:0次
2023-12-15更新
|
116次组卷
|
21卷引用:北京市第八中学2022-2023学年高一下学期期末考试化学试题
北京市第八中学2022-2023学年高一下学期期末考试化学试题北京师范大学附属实验中学2020-2021学年高一上学期期末考试化学试题四川省德阳市德阳五中2021-2022学年高一上学期期末考试化学试题北京师范大学附属实验中学2021-2022学年高一上学期1月期末测试化学试题北京市清华大学附属中学2023-2024学年高三上学期开学考试化学(A)试题福建省厦门外国语学校2023-2024学年高一上学期10月第一次月考化学试题天津市第一中学2023-2024学年高一上学期11月期中化学试题北京市第二十中学2023-2024学年高一上学期期中考试化学试题北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题北京市日坛中学2023-2024学年高一上学期期中考试化学试题北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题北京师范大学燕化附属中学2023-2024学年高一上学期期中考试化学试卷河南省唐河县鸿唐高级中学2023-2024学年高三上学期9月月考化学试题北京市第一五九中学2023-2024学年高一上学期期中考试化学试题山东省菏泽市郓城县第一中学2023-2024学年高一上学期9月月考化学试题北京市海淀区2021届高三上学期期中考试化学试题安徽省示范高中培优联盟2020-2021学年高一上学期冬季联赛化学试题北京一零一中学2021-2022学年高三上学期 9月开学练习化学试题北京交通大学附属中学2021-2022学年高一上学期期中考试化学试题(已下线)北京市第四中学2022-2023学年高一上学期期中考试化学试题北京市首都师范大学附属中学2022-2023学年高一上学期12月月考化学试题
名校
解题方法
9 . 为检验某加碘食盐中是否含有 ,取相同食盐样品进行下表所示实验:
,取相同食盐样品进行下表所示实验:
已知:
下列说法中正确的是
 ,取相同食盐样品进行下表所示实验:
,取相同食盐样品进行下表所示实验:已知:

| 实验① | 实验② | 实验③ |
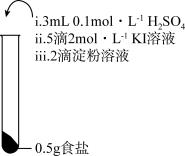 | 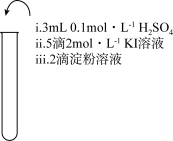 | 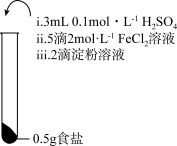 |
| 振荡,溶液迅速变为蓝色 | 振荡,一段时间后溶液变为浅蓝色 | 振荡,溶液变为浅黄色 |
A.仅由实验①就能证明食盐样品中存在 |
B.以上实验说明离子的还原性: |
C.实验③能证明食盐样品中不存在 |
D.实验②中发生反应的离子方程式为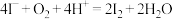 |
您最近一年使用:0次
2023-11-04更新
|
296次组卷
|
2卷引用:广东省深圳市南头中学2023-2024学年高一上学期期末调研考试(模拟)化学试题
10 . 2021年在四川广汉三星堆新发现大量青铜器,如青铜面具、青铜神树等等。如图中的文物是三星堆出土的青铜面具之一,由于时间久远,表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、O2、CO2作用产生的,其化学式为Cu2(OH)2CO3,请用学过的方法对其展开探究。

(1)根据以上信息,可以获知的Cu2(OH)2CO3的物理性质有___________ 、___________ (选取其中两点)。
(2)从不同的物质分类标准的角度分析,“铜绿”不属于___________ 。
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐 F.碱
(3)从“铜绿”的组成、类别和性质的关联角度,预测它可能具有的化学性质,并用化学方程式加以表达(注:选写两个你认为可以实现的反应方程式,并且尽可能使得到的产物形态不同)
①___________ ,②___________ 。
(4)以“铜绿”为反应物可以实现以下物质转化:

反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式___________ 。

(1)根据以上信息,可以获知的Cu2(OH)2CO3的物理性质有
(2)从不同的物质分类标准的角度分析,“铜绿”不属于
A.铜盐 B.碳酸盐 C.碱式盐 D.碱 E.含氧酸盐 F.碱
(3)从“铜绿”的组成、类别和性质的关联角度,预测它可能具有的化学性质,并用化学方程式加以表达(注:选写两个你认为可以实现的反应方程式,并且尽可能使得到的产物形态不同)
①
(4)以“铜绿”为反应物可以实现以下物质转化:

反应④使用的是气体还原剂,且得到的产物之一,可以使澄清石灰水变浑浊。请写出反应④的化学方程式
您最近一年使用:0次
2023-11-02更新
|
336次组卷
|
3卷引用:卷一 物质及其变化 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末复习检测卷