1 .  具有氧化性、还原性和漂白性,某同学在实验室利用
具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问题:
做相关验证和探究实验。回答下列问题:
(1)用如图1装置(夹持仪器已省略)验证 具有氧化性。
具有氧化性。 的名称为
的名称为___________ 。
②装置甲试管中反应的离子方程式为___________ 。
③说明 具有氧化性的现象为
具有氧化性的现象为___________ 。
(2)该同学设计如图2所示装置(夹持仪器已省略)制备 (难溶解于水中)。
(难溶解于水中)。 的作用是
的作用是___________ 。
②三颈烧瓶中反应的化学方程式为___________ 。
(3)该实验体现了 的性质是
的性质是___________ 。
(4)实验表明,将纯净的 缓缓地通入到
缓缓地通入到 溶液中,得到
溶液中,得到 沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
假设Ⅰ:溶液中的 ;
;
假设Ⅱ:溶解在水中的氧气。
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
实验i现象为___________ ,实验ii的现象为___________ 。
②验证假设Ⅱ。请完成下列表格:
实验iv的步骤为___________ ,实验目的是___________ 。
 具有氧化性、还原性和漂白性,某同学在实验室利用
具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问题:
做相关验证和探究实验。回答下列问题:(1)用如图1装置(夹持仪器已省略)验证
 具有氧化性。
具有氧化性。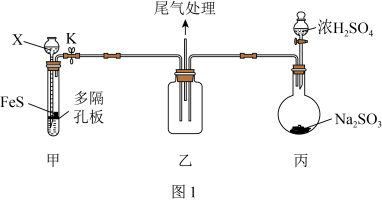
 的名称为
的名称为②装置甲试管中反应的离子方程式为
③说明
 具有氧化性的现象为
具有氧化性的现象为(2)该同学设计如图2所示装置(夹持仪器已省略)制备
 (难溶解于水中)。
(难溶解于水中)。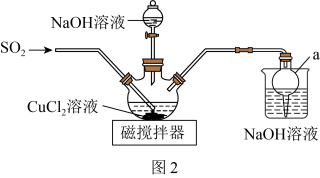
 的作用是
的作用是②三颈烧瓶中反应的化学方程式为
(3)该实验体现了
 的性质是
的性质是(4)实验表明,将纯净的
 缓缓地通入到
缓缓地通入到 溶液中,得到
溶液中,得到 沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:假设Ⅰ:溶液中的
 ;
;假设Ⅱ:溶解在水中的氧气。
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
实验 | 向 溶液中缓慢通入纯净的 溶液中缓慢通入纯净的 气体 气体 | 假设I成立 | |
实验 | 向 溶液的烧杯中缓慢通入纯净的 溶液的烧杯中缓慢通入纯净的 气体 气体 |
②验证假设Ⅱ。请完成下列表格:
| 实验步骤 | 实验现象 | 实验目的 | |
| 实验iii | 同实验 步骤 步骤 | 同实验 的相关现象 的相关现象 | 作对照实验 |
| 实验iv | 产生白色沉淀 | ||
您最近一年使用:0次
2024-02-23更新
|
724次组卷
|
10卷引用:四川省绵阳中学2023-2024学年高三下学期2月开学考理科综合-高中化学
四川省绵阳中学2023-2024学年高三下学期2月开学考理科综合-高中化学河南省郑州市第五高级中学2023-2024学年高三2月开学考理综试题-高中化学河南省周口市部分学校2023-2024学年高三下学期2月开学摸底考试理科综合试题-高中化学江西省部分学校2023-2024学年高三上学期2月月考化学试题(已下线)专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)(已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)2024届内蒙古自治区乌海市第六中学高三下学期第三次模拟考试理综试题-高中化学四川省广元市川师大万达中学2023-2024学年高一下学期3月月考化学试题黑龙江省牡丹江市第一高级中学2023-2024学年高一下学期5月期中考试化学试题甘肃省2023-2024学年高三上学期第一次诊断考试模拟预测化学试题
名校
2 . 碳中和是指碳的排放与吸收达到平衡,基本实现碳的零排放:碳“捕集”是助力碳中和的重要途径。为此,兴趣小组同学围绕着 的吸收进行了实验探究。
的吸收进行了实验探究。
活动一:寻找吸收 的试剂
的试剂
【设计与实验】
(1)甲、乙、丙三组分别利用所提供的实验用品设计了如下方案并进行实验:
【解释与分析】
(2)甲组实验中软塑料瓶变瘪,是因为瓶内气压_______ 。
(3)小礼同学对丙组的实验结论提出质疑,为了证明 与氢氧化钠发生了反应,他向丙组所得溶液中滴加足量的
与氢氧化钠发生了反应,他向丙组所得溶液中滴加足量的_______ ,观察到有气泡产生,从而证明 能与氢氧化钠反应。
能与氢氧化钠反应。
【得出结论】水、饱和石灰水和氢氧化钠溶液均能吸收 。
。
活动二:比较吸收 的效果
的效果
【提出问题】水、饱和石灰水和氢氧化钠浓溶液,哪个吸收 的效果更好?
的效果更好?
【讨论交流】
(4)饱和石灰水、水吸收 的效果差不多,从物质的溶解性的角度分析,原因是
的效果差不多,从物质的溶解性的角度分析,原因是_______ 。同学们一致认为,只需要比较氢氧化钠浓溶液、水吸收 的效果。
的效果。
【设计方案】
(5)请你利用下列提供的实验用品,帮助他们设计实验并写出实验方案:_______ 。
(实验用品:氢氧化钠浓溶液、水、装满 的软塑料瓶若干个,其它仪器自选)
的软塑料瓶若干个,其它仪器自选)
【实验与结论】通过实验,同学们得出氢氧化钠浓溶液吸收 的效果比水的好。
的效果比水的好。
【迁移应用】 气体排放到空气中也会造成环境问题。同学们查阅资料。并利用下图所示装置和用品进行实验,来比较氢氧化钠浓溶液、水吸收
气体排放到空气中也会造成环境问题。同学们查阅资料。并利用下图所示装置和用品进行实验,来比较氢氧化钠浓溶液、水吸收 的效果。
的效果。
(6)请你分析,该实验能?”达到实验目的。并阐述理由_______ (已知实验装置气密性良好且操作均正确)。
【表达与交流】通过以上探究,同学们认识到科学探究需要严谨的思维。
 的吸收进行了实验探究。
的吸收进行了实验探究。活动一:寻找吸收
 的试剂
的试剂【设计与实验】
(1)甲、乙、丙三组分别利用所提供的实验用品设计了如下方案并进行实验:
| 组别 | 实验方案 | 现象 | 结论 |
| 甲组 | 向一个集满 的软塑料瓶中加入适量的水,立即旋紧瓶盖,振荡 的软塑料瓶中加入适量的水,立即旋紧瓶盖,振荡 | 软塑料瓶变瘪 |  能被水吸收 能被水吸收 |
| 乙组 | 向盛有饱和的澄清石灰水的试管中。通入适量的 |  能被澄清石灰水吸收 能被澄清石灰水吸收 | |
| 丙组 | 组向盛有氢氧化钠溶液的试管中,通入适量的 | 无明显现象 |  不能被氢氧化钠溶液吸收 不能被氢氧化钠溶液吸收 |
【解释与分析】
(2)甲组实验中软塑料瓶变瘪,是因为瓶内气压
(3)小礼同学对丙组的实验结论提出质疑,为了证明
 与氢氧化钠发生了反应,他向丙组所得溶液中滴加足量的
与氢氧化钠发生了反应,他向丙组所得溶液中滴加足量的 能与氢氧化钠反应。
能与氢氧化钠反应。【得出结论】水、饱和石灰水和氢氧化钠溶液均能吸收
 。
。活动二:比较吸收
 的效果
的效果【提出问题】水、饱和石灰水和氢氧化钠浓溶液,哪个吸收
 的效果更好?
的效果更好?【讨论交流】
(4)饱和石灰水、水吸收
 的效果差不多,从物质的溶解性的角度分析,原因是
的效果差不多,从物质的溶解性的角度分析,原因是 的效果。
的效果。【设计方案】
(5)请你利用下列提供的实验用品,帮助他们设计实验并写出实验方案:
(实验用品:氢氧化钠浓溶液、水、装满
 的软塑料瓶若干个,其它仪器自选)
的软塑料瓶若干个,其它仪器自选) 【实验与结论】通过实验,同学们得出氢氧化钠浓溶液吸收
 的效果比水的好。
的效果比水的好。【迁移应用】
 气体排放到空气中也会造成环境问题。同学们查阅资料。并利用下图所示装置和用品进行实验,来比较氢氧化钠浓溶液、水吸收
气体排放到空气中也会造成环境问题。同学们查阅资料。并利用下图所示装置和用品进行实验,来比较氢氧化钠浓溶液、水吸收 的效果。
的效果。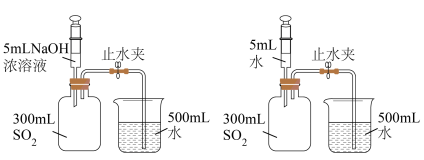
| 资料卡片 I.通常状况下,1体积水约能溶解40体积  II.  与 与 的化学性质相似,也能与氢氧化钠反应: 的化学性质相似,也能与氢氧化钠反应: |
(6)请你分析,该实验能?”达到实验目的。并阐述理由
【表达与交流】通过以上探究,同学们认识到科学探究需要严谨的思维。
您最近一年使用:0次
名校
解题方法
3 . 硫酸亚铁可用于治疗缺铁性贫血症。某兴趣小组为探究硫酸亚铁的分解产物,设计实验方案如下:
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有 的硬质玻璃管;
的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有___________ 和___________ 。
(2)将装置B、C顺序颠倒能否达到原来的实验目的___________ (填“能”或“不能”),原因是___________ 。
(3)D装置中发生的主要反应的离子方程式是___________ 。
(4)通过计算确定已分解的FeSO4物质的量(写出计算过程)___________ 。
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有
 的硬质玻璃管;
的硬质玻璃管;③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有
(2)将装置B、C顺序颠倒能否达到原来的实验目的
(3)D装置中发生的主要反应的离子方程式是
(4)通过计算确定已分解的FeSO4物质的量(写出计算过程)
您最近一年使用:0次
2024-03-15更新
|
154次组卷
|
2卷引用:江苏省盐城市建湖高级中学2023-2024学年高一下学期期初测试(2月)化学试题
4 . 某实验小组用如图装置制备氯气并探究其性质(夹持装置已省略),下列分析错误的是
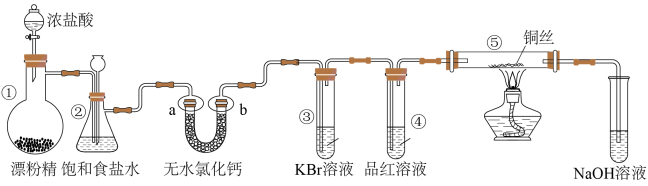
| A.用MnO2代替装置中的漂粉精也可以达到实验目的 |
| B.a、b处分别放干燥和湿润的有色布条,无法说明干燥的Cl2不具有漂白性 |
| C.反应开始后可观察到③中溶液变黄,④中溶液褪色,说明氯水具有氧化性和漂白性 |
| D.反应开始后点燃酒精灯,可在⑤号硬质玻璃管中观察到棕黄色烟 |
您最近一年使用:0次
名校
解题方法
5 . 实验室用下图所示装置制备氯气,并进行氯气性质实验,请回答下列问题:___________ 。
(2)B和C中出现的不同现象可得出的结论是___________ 。
(3)D发生反应的离子方程式___________ 。
(4)使用氯气对饮用水消毒,会使水中的有机物发生氯化,生成有机含氯化合物对人体有害,现已发现新的自来水消毒剂,如ClO2:
①实验室可以用下列方法制备ClO2:NaClO3+H2O2+H2SO4→ClO2+Na2SO4+O2+H2O(未配平),若反应中有0.2mol电子转移,则产生的ClO2的物质的量为___________ 。
②用ClO2在处理含有Mn2+废水时,ClO2可将废水中的Mn2+转化为MnO2除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为___________ 。
(5)某实验小组探究新制氯水与铁的反应。实验操作过程及实验现象如图所示。___________ 。
②实验iii中观察到溶液无明显变化,可推知上层清液中不含Fe3+,其原因是___________ (用离子方程式表示)。
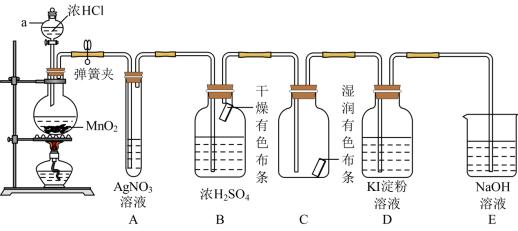
(2)B和C中出现的不同现象可得出的结论是
(3)D发生反应的离子方程式
(4)使用氯气对饮用水消毒,会使水中的有机物发生氯化,生成有机含氯化合物对人体有害,现已发现新的自来水消毒剂,如ClO2:
①实验室可以用下列方法制备ClO2:NaClO3+H2O2+H2SO4→ClO2+Na2SO4+O2+H2O(未配平),若反应中有0.2mol电子转移,则产生的ClO2的物质的量为
②用ClO2在处理含有Mn2+废水时,ClO2可将废水中的Mn2+转化为MnO2除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
(5)某实验小组探究新制氯水与铁的反应。实验操作过程及实验现象如图所示。
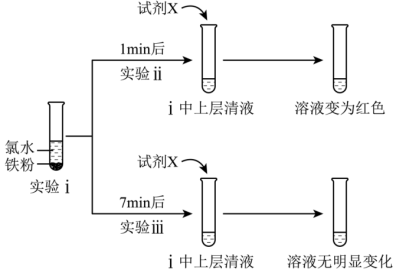
②实验iii中观察到溶液无明显变化,可推知上层清液中不含Fe3+,其原因是
您最近一年使用:0次
名校
6 . 碘化亚铁 在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。
在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。 )
)
(1)装置中盛碱石灰的仪器名称为_____ 。若无此装置,写出铁粉参与的副反应的化学方程式:_____ 。
(2)收集器浸泡在冷水中的原因是_____ 。
(3)试剂a为_____ ,其作用是_____ 。
Ⅱ、化学兴趣小组为了探究 的还原性,进行了如下实验:取一定量的
的还原性,进行了如下实验:取一定量的 溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。同学们对溶液变成黄色的原因提出了不同的看法:
溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。同学们对溶液变成黄色的原因提出了不同的看法:
甲同学认为:是因为被 氧化成
氧化成 ;乙同学认为:是因为被
;乙同学认为:是因为被 氧化成
氧化成 。
。
随后化学兴趣小组进行如下实验进行验证。
(4)上述实验②中现象为_____ 。化学兴趣小组得到的结论: 的还原性
的还原性_____  的还原性(填“
的还原性(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(5)依据(4)中所得结论,试写出往过量 溶液中通入少量氯气后所发生反应的离子反应方程式:
溶液中通入少量氯气后所发生反应的离子反应方程式:_____ 。
 在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。
在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。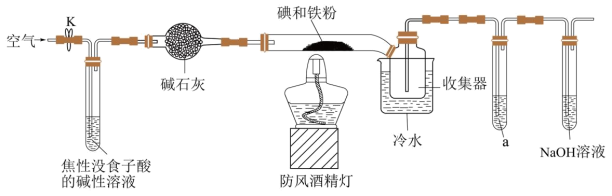
 )
)(1)装置中盛碱石灰的仪器名称为
(2)收集器浸泡在冷水中的原因是
(3)试剂a为
Ⅱ、化学兴趣小组为了探究
 的还原性,进行了如下实验:取一定量的
的还原性,进行了如下实验:取一定量的 溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。同学们对溶液变成黄色的原因提出了不同的看法:
溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。同学们对溶液变成黄色的原因提出了不同的看法:甲同学认为:是因为被
 氧化成
氧化成 ;乙同学认为:是因为被
;乙同学认为:是因为被 氧化成
氧化成 。
。随后化学兴趣小组进行如下实验进行验证。
| 实验步骤 | 现象 | 结论 |
| ①取少量黄色溶液于试管中,滴加淀粉溶液 | 试管中溶液变蓝色 | 甲同学观点正确 |
②取少量黄色溶液于试管中,滴加 溶液 溶液 | 乙同学观点不正确 |
(4)上述实验②中现象为
 的还原性
的还原性 的还原性(填“
的还原性(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。(5)依据(4)中所得结论,试写出往过量
 溶液中通入少量氯气后所发生反应的离子反应方程式:
溶液中通入少量氯气后所发生反应的离子反应方程式:
您最近一年使用:0次
2024-02-16更新
|
200次组卷
|
3卷引用:安徽省淮北市第一中学2023-2024学年高一下学期开学考试 化学试卷
7 .  常作有机反应的催化剂。某实验小组拟制备
常作有机反应的催化剂。某实验小组拟制备 并探究其性质。
并探究其性质。
实验(一)制备 。
。
装置如图1所示。已知: 沸点为58.8℃。实验中,观察到烧瓶中产生红棕色气体。
沸点为58.8℃。实验中,观察到烧瓶中产生红棕色气体。_______ (填“溴水”或“液溴”)。用铁粉替代铁片的目的是_______ 。
(2)装置中利用到的四氯化碳的性质是_______ 。实验完毕后,将烧瓶中混合物经_______ (填实验操作名称)得到 固体。
固体。
实验(二)探究性质。
为了探究的稳定性,进行如图2实验。_______ (填实验现象)时,可以确认 发生分解反应,生成了
发生分解反应,生成了 。
。
(4)实验过程中,先通入一会儿 ,再点燃酒精灯,这样操作的目的是
,再点燃酒精灯,这样操作的目的是_______ 。
(5)为确认玻璃管中残留物有 ,宜选择试剂
,宜选择试剂_______ (填标号)。
a. 溶液 b.酸性
溶液 b.酸性 溶液
溶液
c.KSCN溶液,氯水 d. 溶液
溶液
(6)为了探究浓度对 氧化性的影响,实验操作及现象如下:
氧化性的影响,实验操作及现象如下:
已知: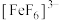 呈无色。
呈无色。
写出实验ⅰ中离子反应方程式:_______ 。
实验ⅱ“不变蓝色”的原因是_______ (结合必要化学用语和文字解释)。
 常作有机反应的催化剂。某实验小组拟制备
常作有机反应的催化剂。某实验小组拟制备 并探究其性质。
并探究其性质。实验(一)制备
 。
。装置如图1所示。已知:
 沸点为58.8℃。实验中,观察到烧瓶中产生红棕色气体。
沸点为58.8℃。实验中,观察到烧瓶中产生红棕色气体。
(2)装置中利用到的四氯化碳的性质是
 固体。
固体。实验(二)探究性质。
为了探究的稳定性,进行如图2实验。
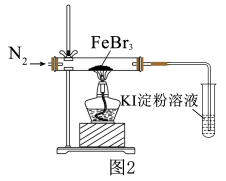
 发生分解反应,生成了
发生分解反应,生成了 。
。(4)实验过程中,先通入一会儿
 ,再点燃酒精灯,这样操作的目的是
,再点燃酒精灯,这样操作的目的是(5)为确认玻璃管中残留物有
 ,宜选择试剂
,宜选择试剂a.
 溶液 b.酸性
溶液 b.酸性 溶液
溶液c.KSCN溶液,氯水 d.
 溶液
溶液(6)为了探究浓度对
 氧化性的影响,实验操作及现象如下:
氧化性的影响,实验操作及现象如下:实验 | 操作 | 现象 |
ⅰ | 向2mL0.1mol 溶液中滴加KI淀粉溶液 溶液中滴加KI淀粉溶液 | 溶液变蓝色 |
ⅱ | 向2mL0.1mol 溶液中先加入适量NaF固体,后滴加KI淀粉溶液 溶液中先加入适量NaF固体,后滴加KI淀粉溶液 | 溶液不变蓝色 |
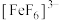 呈无色。
呈无色。写出实验ⅰ中离子反应方程式:
实验ⅱ“不变蓝色”的原因是
您最近一年使用:0次
2024-09-11更新
|
200次组卷
|
2卷引用:河南省驻马店市新蔡县新蔡县第一高级中学2024-2025学年高三上学期开学化学试题
8 . 碱式碳酸铜[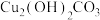 ]俗称铜绿,是一种蓝绿色固体,难溶于水,应用广泛。化学兴趣小组以“碱式碳酸铜的组成、结构、性质、应用和制备”为主题,开展项目式学习。
]俗称铜绿,是一种蓝绿色固体,难溶于水,应用广泛。化学兴趣小组以“碱式碳酸铜的组成、结构、性质、应用和制备”为主题,开展项目式学习。
【任务一】认识铜绿的组成与结构
(1)铜绿的结构如图1所示,其中“ ”表示铜离子,“
”表示铜离子,“ ”,表示碳酸根离子,则“
”,表示碳酸根离子,则“ ”表示
”表示___________ (填微粒名称)。
(2)探究铜绿的性质与转化
①铜绿呈蓝绿色,易被发现和识别,这利用的是铜绿的___________ (选填“物理”或“化学”)性质。
② 。X的化学式为
。X的化学式为___________ 。
③兴趣小组基于“结构决定性质”的学科观念,猜想铜绿能与盐酸反应生成 气体:猜想的依据是铜绿中含有
气体:猜想的依据是铜绿中含有___________ (填离子符号)。
④兴趣小组用图2所示装置进行验证。若猜想正确,能观察到的现象是___________ 。
铜绿是一种农业上常用的杀菌剂,可用硫酸铜和碳酸钠溶液混合加热进行制备:
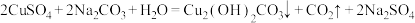 。
。
为了探究适宜反应温度,进行如下三个实验:
【实验分析】
(3)实验2中所用 溶液的体积x为
溶液的体积x为___________ mL。
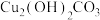 ]俗称铜绿,是一种蓝绿色固体,难溶于水,应用广泛。化学兴趣小组以“碱式碳酸铜的组成、结构、性质、应用和制备”为主题,开展项目式学习。
]俗称铜绿,是一种蓝绿色固体,难溶于水,应用广泛。化学兴趣小组以“碱式碳酸铜的组成、结构、性质、应用和制备”为主题,开展项目式学习。【任务一】认识铜绿的组成与结构
(1)铜绿的结构如图1所示,其中“
 ”表示铜离子,“
”表示铜离子,“ ”,表示碳酸根离子,则“
”,表示碳酸根离子,则“ ”表示
”表示
(2)探究铜绿的性质与转化
①铜绿呈蓝绿色,易被发现和识别,这利用的是铜绿的
②
 。X的化学式为
。X的化学式为③兴趣小组基于“结构决定性质”的学科观念,猜想铜绿能与盐酸反应生成
 气体:猜想的依据是铜绿中含有
气体:猜想的依据是铜绿中含有④兴趣小组用图2所示装置进行验证。若猜想正确,能观察到的现象是

铜绿是一种农业上常用的杀菌剂,可用硫酸铜和碳酸钠溶液混合加热进行制备:
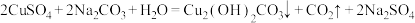 。
。为了探究适宜反应温度,进行如下三个实验:
| 编号 |  溶液体积/mL 溶液体积/mL |  溶液体积/mL 溶液体积/mL | 反应温度℃ | 实验现象 |
| 1 | 2.4 | 2.0 | 20 | 反应速度慢,得到蓝色沉淀 |
| 2 | x | 2.0 | 50 | 反应速度适中,得到蓝绿色沉淀 |
| 3 | 2.4 | 2.0 | 90 | 反应速度快,得到浅蓝色沉淀,逐渐变为黑褐色 |
(3)实验2中所用
 溶液的体积x为
溶液的体积x为
您最近一年使用:0次
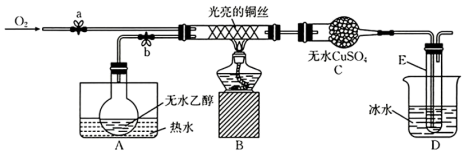
9 . 某同学设计了如图所示装置(夹持装置已省略)进行乙醇的催化氧化实验。先按图示安装好实验装置,关闭活塞a、b,在铜丝的中间部分加热片刻,然后通过控制活塞a和b,有节奏(间歇性)地通入气体。已知:乙醛可被氧化为乙酸,乙醛的沸点为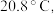 乙酸的沸点为
乙酸的沸点为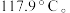
(1)实验室常用 快速制备氧气,写出
快速制备氧气,写出 的结构式:
的结构式:___________ 。
(2)从硬质玻璃管中可观察到受热的铜丝交替出现变黑、变红的现象,请写出实验过程中乙醇催化氧化的化学方程式:___________ 。实验开始后,实验小组将酒精灯去掉之后,依然能观察到铜丝交替出现变黑、变红的现象,试解释其原因:___________ 。
(3)实验中A和D均用到了水浴作用。A的作用是_____ ,D的作用是_____ 。
(4)C中的实验现象是___________ 。
(5)经检测,实验小组发现E中收集到的液体除含有乙醛(易溶于水)外还含有杂质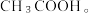 要除去乙醛中的
要除去乙醛中的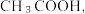 ,可采取的方法为
,可采取的方法为___________ 。
(6)该小组通过以上实验探究做出了如下猜想,你认为正确的是___________ (填标号)。
a.表面被氧化为黑色的铜丝在酒精灯焰心处灼烧,可闻到刺激性气味
b.乙醇催化氧化生成乙醛时,乙醇分子中只有O—H键发生断裂
c.利用金属钠能检验试管E中有没有未反应的乙醇
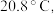 乙酸的沸点为
乙酸的沸点为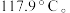
(1)实验室常用
 快速制备氧气,写出
快速制备氧气,写出 的结构式:
的结构式:(2)从硬质玻璃管中可观察到受热的铜丝交替出现变黑、变红的现象,请写出实验过程中乙醇催化氧化的化学方程式:
(3)实验中A和D均用到了水浴作用。A的作用是
(4)C中的实验现象是
(5)经检测,实验小组发现E中收集到的液体除含有乙醛(易溶于水)外还含有杂质
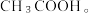 要除去乙醛中的
要除去乙醛中的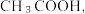 ,可采取的方法为
,可采取的方法为(6)该小组通过以上实验探究做出了如下猜想,你认为正确的是
a.表面被氧化为黑色的铜丝在酒精灯焰心处灼烧,可闻到刺激性气味
b.乙醇催化氧化生成乙醛时,乙醇分子中只有O—H键发生断裂
c.利用金属钠能检验试管E中有没有未反应的乙醇
您最近一年使用:0次
2024-08-21更新
|
76次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2024-2025学年高二上学期开学考试化学试题
名校
解题方法
10 . 某化学活动小组利用如下装置制备氯气并进行相关的性质验证。
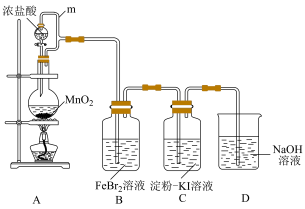
已知:
① 易溶于有机溶剂四氯化碳(
易溶于有机溶剂四氯化碳( ),且所得溶液呈橙红色;
),且所得溶液呈橙红色;
② 不溶于水,密度比水大。
不溶于水,密度比水大。
(1)装置A中发生反应的化学方程式为
(2)m的作用是
(3)装置C中的现象是
(4)装置D中发生反应的离子方程式为
(5)取少量反应后的B中溶液,向其中加入
 ,振荡后静置,若出现
,振荡后静置,若出现 被氧化。
被氧化。(6)另取少量反应后的B中溶液于试管中,向其中加入少量
 被氧化。
被氧化。(7)已知氧化性
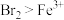 ,向200mL 0.1mol/L
,向200mL 0.1mol/L  溶液中通入标准状况下0.56L
溶液中通入标准状况下0.56L  时反应的离子方程式为
时反应的离子方程式为
您最近一年使用:0次



