1 . (1)茶叶、肉松、膨化食品等常采用真空充气包装,即将食品装入包装袋,抽出包装袋内的空气,再充入防止食品变质的气体,然后封口。真空充气包装能使食品保持原有的色、香、味及营养价值,防止食品受压而破碎变形。
提出问题:充入食品包装袋中的气体是什么?
猜想与验证:可能是 。实验初步验证的方法及现象:
。实验初步验证的方法及现象:________________________________ 。充入的气体还可能是_________ 。
(2)亚硝酸钠可作为食品的着色剂和防腐剂,但若用量超标,会危害人体健康。亚硝酸钠具有咸味,外形与食盐相似。亚硝酸钠的水溶液呈碱性,食盐的水溶液呈中性。如果请你鉴别亚硝酸钠溶液和食盐溶液,你将选用________ 来鉴别。
提出问题:充入食品包装袋中的气体是什么?
猜想与验证:可能是
 。实验初步验证的方法及现象:
。实验初步验证的方法及现象:(2)亚硝酸钠可作为食品的着色剂和防腐剂,但若用量超标,会危害人体健康。亚硝酸钠具有咸味,外形与食盐相似。亚硝酸钠的水溶液呈碱性,食盐的水溶液呈中性。如果请你鉴别亚硝酸钠溶液和食盐溶液,你将选用
您最近一年使用:0次
2 . Ⅰ.已知 和
和 之间发生可逆反应:
之间发生可逆反应: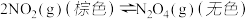 。
。
(1)如图是在一定温度下,某固定容积的密闭容器中充入一定量的 气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是
气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是___________ 。
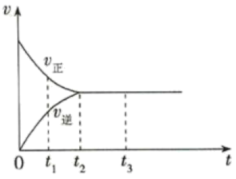
a.t1时,反应未达到平衡, 浓度在减小
浓度在减小
b.t2时,反应达到平衡,反应不再进行
c. ,各物质浓度不再变化
,各物质浓度不再变化
d. ,各物质的浓度相等
,各物质的浓度相等
e. ,
, 浓度增大
浓度增大
f.反应过程中气体的颜色不变
Ⅱ.某研究性学习小组欲研究影响锌和稀硫酸反应速率的外界条件,下表是其实验设计的有关数据:
(2)在上述5组实验中,测定锌和稀硫酸反应速率大小,最简单的方法可通过定量测定锌完全消失所需的时间 进行判断,其反应速率最快的实验是___________ (填实验序号)。
(3)对于锌和稀硫酸的反应,实验1和2表明,___________ 对反应速率有影响。
(4)进行实验2时,该小组同学根据实验过程绘制的标准状况下的气体体积V与时间t的图象如图所示。
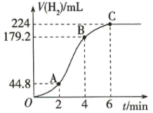
在OA、AB、BC三段中反应速率最快的是___________ ,2~4min内以硫酸的浓度变化表示的反应速率(假设溶液的体积不变)=___________ 。
 和
和 之间发生可逆反应:
之间发生可逆反应: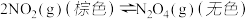 。
。(1)如图是在一定温度下,某固定容积的密闭容器中充入一定量的
 气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是
气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是
a.t1时,反应未达到平衡,
 浓度在减小
浓度在减小b.t2时,反应达到平衡,反应不再进行
c.
 ,各物质浓度不再变化
,各物质浓度不再变化d.
 ,各物质的浓度相等
,各物质的浓度相等e.
 ,
, 浓度增大
浓度增大f.反应过程中气体的颜色不变
Ⅱ.某研究性学习小组欲研究影响锌和稀硫酸反应速率的外界条件,下表是其实验设计的有关数据:
| 实验序号 | 锌的质量/g | 锌的状态 | 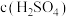 /mol·L-1 /mol·L-1 | 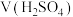 /mL /mL | 反应前溶液的温度/℃ | 添加剂 |
| 1 | 0.65 | 粒状 | 0.5 | 50 | 20 | 无 |
| 2 | 0.65 | 粉末 | 0.5 | 50 | 20 | 无 |
| 3 | 0.65 | 粒状 | 0.5 | 50 | 20 | 2滴 溶液 溶液 |
| 4 | 0.65 | 粉末 | 0.8 | 50 | 20 | 无 |
| 5 | 0.65 | 粉末 | 0.8 | 50 | 35 | 2滴 溶液 溶液 |
(3)对于锌和稀硫酸的反应,实验1和2表明,
(4)进行实验2时,该小组同学根据实验过程绘制的标准状况下的气体体积V与时间t的图象如图所示。

在OA、AB、BC三段中反应速率最快的是
您最近一年使用:0次
19-20高一·全国·单元测试
解题方法
3 . 膨松剂是一种食品添加剂,某研究小组A对膨松剂进行了如下探究(已知: ):
):
【趣味实验】
步骤1:和面,向20g面粉中加入10mL水,制得的面团编为1号;向20g面粉中加入10ml水,再加入2g膨松剂M,制得的面团编为2号。
步骤2:发面,将和好的2个面团放入微波炉中加热,几分钟后,取出面团,发现1号面团无明显胀大,2号面团明显胀大且手感比较松软。
【提出问题】膨松剂M的成分是什么?
【提出假设】
假设1:M是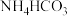 ;
;
假设2:M是 ;
;
假设3:M是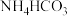 和
和 。
。
【实验探究1】
【提出新问题】实验①试管中剩余固体是什么?
【实验探究2】实验②:将实验①所得固体继续加热,无明显现象。冷却,向试管中加水,固体全部溶解,将所得溶液分为两份,向其中一份溶液中滴加稀盐酸,有气泡生成,将生成的气体通入澄清石灰水,有白色沉淀生成;向另一份溶液中滴加足量氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液不变红。
【得出结论】实验①试管中剩余固体是_______________ (填化学式)。
【反思提高】热稳定性:
_______________ (填“>”“=”或“<”) 。
。
【拓展应用】某品牌复合膨松剂N的配料为磷酸二氢钙、碳酸氢钠和玉米淀粉,N遇水会发生如下反应: 。下列叙述正确的是
。下列叙述正确的是________ (填序号)。
a 常温下的溶解度: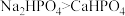
b 碳酸氢钠在水溶液中遇到某些呈酸性的物质能产生气体
c 根据上述反应,产生0.22g 至少需要
至少需要 的质量为0.42g
的质量为0.42g
 ):
):【趣味实验】
步骤1:和面,向20g面粉中加入10mL水,制得的面团编为1号;向20g面粉中加入10ml水,再加入2g膨松剂M,制得的面团编为2号。
步骤2:发面,将和好的2个面团放入微波炉中加热,几分钟后,取出面团,发现1号面团无明显胀大,2号面团明显胀大且手感比较松软。
【提出问题】膨松剂M的成分是什么?
【提出假设】
假设1:M是
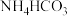 ;
;假设2:M是
 ;
;假设3:M是
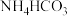 和
和 。
。【实验探究1】
| 实验① | 实验现象 | 实验结论 |
| 取少量M于试管中,加热一段时间 | 无刺激性气味;试管内壁有水珠;试管内有固体剩余 | 假设 |
【实验探究2】实验②:将实验①所得固体继续加热,无明显现象。冷却,向试管中加水,固体全部溶解,将所得溶液分为两份,向其中一份溶液中滴加稀盐酸,有气泡生成,将生成的气体通入澄清石灰水,有白色沉淀生成;向另一份溶液中滴加足量氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液不变红。
【得出结论】实验①试管中剩余固体是
【反思提高】热稳定性:

 。
。【拓展应用】某品牌复合膨松剂N的配料为磷酸二氢钙、碳酸氢钠和玉米淀粉,N遇水会发生如下反应:
 。下列叙述正确的是
。下列叙述正确的是a 常温下的溶解度:
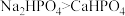
b 碳酸氢钠在水溶液中遇到某些呈酸性的物质能产生气体
c 根据上述反应,产生0.22g
 至少需要
至少需要 的质量为0.42g
的质量为0.42g
您最近一年使用:0次
4 . 煤气化是有效利用化石能源的手段之一,有关反应为
① 、②
、② ,获得的气体称为水煤气。某研究性学习小组为探究气体的成分,进行了如下实验。
,获得的气体称为水煤气。某研究性学习小组为探究气体的成分,进行了如下实验。
【实验】使水蒸气通过灼热的焦炭,收集反应后流出的气体。
【提出假设】对气体的成分提出了三种假设。
假设1:该气体是 、
、 、
、 。
。
假设2:该气体是 、
、 、
、 。
。
(1)假设3:___________________________________________ 。
【设计实验方案,验证假设】
拟用图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设3。(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)
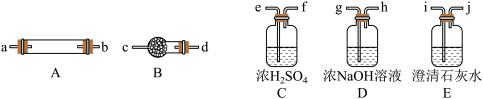
(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器可重复使用):混合气→dc→______ →______ →______ →______ →______ →ij。
(3)仪器A中需加入药品的名称是____________ ,其中反应的化学方程式可能有___________________________________________ 。
(4)仪器B中需加入药品的名称是______________ ,其作用是____________________________ 。
【思考与交流】
(5)本实验的尾气需要处理,处理的方法为_______________________________ 。
①
 、②
、② ,获得的气体称为水煤气。某研究性学习小组为探究气体的成分,进行了如下实验。
,获得的气体称为水煤气。某研究性学习小组为探究气体的成分,进行了如下实验。【实验】使水蒸气通过灼热的焦炭,收集反应后流出的气体。
【提出假设】对气体的成分提出了三种假设。
假设1:该气体是
 、
、 、
、 。
。假设2:该气体是
 、
、 、
、 。
。(1)假设3:
【设计实验方案,验证假设】
拟用图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设3。(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)

(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器可重复使用):混合气→dc→
(3)仪器A中需加入药品的名称是
(4)仪器B中需加入药品的名称是
【思考与交流】
(5)本实验的尾气需要处理,处理的方法为
您最近一年使用:0次
2020-04-10更新
|
378次组卷
|
6卷引用:第二节 资源综合利用 环境保护——A学习区 夯实基础(人教版必修2)
第二节 资源综合利用 环境保护——A学习区 夯实基础(人教版必修2)课时2 海水资源的开发利用煤、 石油和天然气的综合利用——A学习区 夯实基础(人教版(2019)第二册)(已下线)专题11 自然资源的开发利用(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)必修第二册RJ第八章 第一节 课时2 海水资源的开发利用 煤、石油和天然气的综合利用第2课时 煤、石油和天然气的综合利用2015-2016学年河北省正定中学高一下期末化学试卷
名校
5 . 废水中过量的氨氮( 和
和 )会导致水体富营养化。某科研小组用
)会导致水体富营养化。某科研小组用 氧化法处理氨氮废水。已知:①
氧化法处理氨氮废水。已知:① 的氧化性比
的氧化性比 强;②
强;② 比
比 更易被氧化;③国家相关标准要求经处理过的氨氮废水
更易被氧化;③国家相关标准要求经处理过的氨氮废水 要控制在6~9。
要控制在6~9。
(1) 时,
时, 可与
可与 反应生成
反应生成 等无污染物质,该反应的离子方程式为
等无污染物质,该反应的离子方程式为___________ 。
(2)进水 对氨氮去除率和出水pH的影响分别如图1和图2所示:
对氨氮去除率和出水pH的影响分别如图1和图2所示:

图1 图2
①进水 在1.25~2.75范围内时,氨氮去除率随
在1.25~2.75范围内时,氨氮去除率随 的升高迅速下降的原因是
的升高迅速下降的原因是__________ 。
②进水 在2.75~6范围内时,氨氮去除率随
在2.75~6范围内时,氨氮去除率随 的升高而上升的原因是
的升高而上升的原因是___________ 。
③进水 应控制在
应控制在____________ 左右为宜。
(3)为研究空气对 氢化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是
氢化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是______ (填序号)
a. 的氧化性比
的氧化性比 弱
弱
b. 氧化氨氮速率比
氧化氨氮速率比 慢
慢
c. 在废水中溶解度比较小
在废水中溶解度比较小
d.空气中的 进入废水中
进入废水中
 和
和 )会导致水体富营养化。某科研小组用
)会导致水体富营养化。某科研小组用 氧化法处理氨氮废水。已知:①
氧化法处理氨氮废水。已知:① 的氧化性比
的氧化性比 强;②
强;② 比
比 更易被氧化;③国家相关标准要求经处理过的氨氮废水
更易被氧化;③国家相关标准要求经处理过的氨氮废水 要控制在6~9。
要控制在6~9。(1)
 时,
时, 可与
可与 反应生成
反应生成 等无污染物质,该反应的离子方程式为
等无污染物质,该反应的离子方程式为(2)进水
 对氨氮去除率和出水pH的影响分别如图1和图2所示:
对氨氮去除率和出水pH的影响分别如图1和图2所示:
图1 图2
①进水
 在1.25~2.75范围内时,氨氮去除率随
在1.25~2.75范围内时,氨氮去除率随 的升高迅速下降的原因是
的升高迅速下降的原因是②进水
 在2.75~6范围内时,氨氮去除率随
在2.75~6范围内时,氨氮去除率随 的升高而上升的原因是
的升高而上升的原因是③进水
 应控制在
应控制在(3)为研究空气对
 氢化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是
氢化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是a.
 的氧化性比
的氧化性比 弱
弱b.
 氧化氨氮速率比
氧化氨氮速率比 慢
慢c.
 在废水中溶解度比较小
在废水中溶解度比较小d.空气中的
 进入废水中
进入废水中
您最近一年使用:0次
2020-03-05更新
|
718次组卷
|
5卷引用:人教版(2019)必修第二册第五章第二节 课时2 氨和铵盐



