名校
1 . CuCl2是常见的化学试剂,某小组利用废铜屑“湿法”制备CuCl2·2H2O并开展相关探究。
回答下列问题:
(1)仪器a的名称为___________ 。
(2)上述方法制备CuCl2的离子方程式为___________ 。
(3)为得到纯净的CuCl2·2H2O晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入 气体,加热蒸发浓缩,
气体,加热蒸发浓缩,___________ ,过滤,洗涤,低温干燥。持续通入 气体的目的是
气体的目的是___________ 。
(4)实验中,H2O2的实际用量要大于理论用量,可能因素为:原因1:___________ ;原因2:生成的CuCl2催化了H2O2的分解。
(5)该小组对“原因2”进行拓展探究。为验证CuCl2对H2O2分解的催化作用,该小组向5支盛有10mL5%H2O2的试管中滴加不同溶液,实验记录如下表(忽略溶液体积的微小变化;已知一定条件下,还原产物的浓度越小,氧化剂的氧化性越强):
①实验Ⅳ过程中观察到有白色沉淀(经检验为CuCl)生成,反应的机理表示为
第一步:H2O2+2Cu2++2Cl-=O2↑+2CuCl+2H+;
第二步:___________ (写离子方程式)。
②已知化学反应速率第一步<第二步,则气泡产生速率实验Ⅳ比实验Ⅲ加快的原因:___________ 。
③分析上述实验,下列说法正确的是___________ (填字母)。
A.实验Ⅰ的目的是证明仅有NaCl对H2O2分解没有催化作用
B. 对H2O2分解有显著催化作用
对H2O2分解有显著催化作用
C.Cl-增强了Cu2+对H2O2分解的催化效果,且Cl-浓度越大催化效果越强
④写出一种H2O2的用途___________ 。
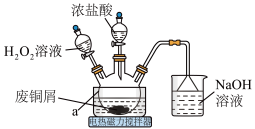
| 温度 | 15℃以下 | 15~25.7℃ | 26~42℃ | 42℃以上 |
| 结晶水合物 | CuCl2·4H2O | CuCl2·3H2O | CuCl2·2H2O | CuCl2·H2O |
(1)仪器a的名称为
(2)上述方法制备CuCl2的离子方程式为
(3)为得到纯净的CuCl2·2H2O晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入
 气体,加热蒸发浓缩,
气体,加热蒸发浓缩, 气体的目的是
气体的目的是(4)实验中,H2O2的实际用量要大于理论用量,可能因素为:原因1:
(5)该小组对“原因2”进行拓展探究。为验证CuCl2对H2O2分解的催化作用,该小组向5支盛有10mL5%H2O2的试管中滴加不同溶液,实验记录如下表(忽略溶液体积的微小变化;已知一定条件下,还原产物的浓度越小,氧化剂的氧化性越强):
| 实验 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| 滴加试剂 | 2滴1mol/LNaCl | 2滴1mol/LNa2SO4 | 2滴1mol/LCuSO4 | 2滴1mol/LCuSO4和2滴1mol/LNaCl | 2滴1mol/LCuSO4和4滴1mol/LNaCl |
| 现象 | 无气泡产生 | 无气泡产生 | 均产生气泡,且气泡速率从Ⅲ到Ⅴ依次加快 | ||
第一步:H2O2+2Cu2++2Cl-=O2↑+2CuCl+2H+;
第二步:
②已知化学反应速率第一步<第二步,则气泡产生速率实验Ⅳ比实验Ⅲ加快的原因:
③分析上述实验,下列说法正确的是
A.实验Ⅰ的目的是证明仅有NaCl对H2O2分解没有催化作用
B.
 对H2O2分解有显著催化作用
对H2O2分解有显著催化作用C.Cl-增强了Cu2+对H2O2分解的催化效果,且Cl-浓度越大催化效果越强
④写出一种H2O2的用途
您最近一年使用:0次
名校
2 . 硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]是分析化学中的重要试剂,是一种复盐,与其他复盐一样,硫酸亚铁铵在水中的溶解度比组成它的每一种盐的溶解度都小,利用这一性质可以用等物质的量的(NH4)2SO4和FeSO4混合制备。请回答以下问题:
I.硫酸亚铁铵晶体的制备
步骤一:称取一定质量铁屑,加入15mL10%Na2CO3溶液,小火加热30分钟,过滤洗涤、干燥、称量得固体mg。
步骤二:将步骤一中的mg固体转移至锥形瓶,加入一定体积3mol·L-1H2SO4充分溶解,将溶液转移入蒸发皿
步骤三:计算所得FeSO4的物质的量,计算等物质的量的(NH4)2SO4固体的质量,准确取(NH4)2SO4。
步骤四:将(NH4)2SO4固体加入步骤二蒸发皿中,缓慢加热浓缩至表面出现结晶薄膜为止,放置冷却。
步骤五:经过一系列操作,最终得到较纯净的(NH4)2FeSO4·6H2O。
(1)步骤一中加入10%Na2CO3溶液,小火加热30分钟的目的是_____
(2)关于步骤五中的一系列操作的相关表述,错误的是_____(填字母)。
II.硫酸亚铁铵的分解
已知硫酸亚铁铵在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全,确定分解产物的成分。_____
(4)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定分解产物中含有_____ 气体,写出D中发生反应的离子方程式_____ ;若去掉C,是否能得出同样结论,并解释其原因_____ 。
(5)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3而不含FeO。其预期实验现象为:_____ 。
I.硫酸亚铁铵晶体的制备
步骤一:称取一定质量铁屑,加入15mL10%Na2CO3溶液,小火加热30分钟,过滤洗涤、干燥、称量得固体mg。
步骤二:将步骤一中的mg固体转移至锥形瓶,加入一定体积3mol·L-1H2SO4充分溶解,将溶液转移入蒸发皿
步骤三:计算所得FeSO4的物质的量,计算等物质的量的(NH4)2SO4固体的质量,准确取(NH4)2SO4。
步骤四:将(NH4)2SO4固体加入步骤二蒸发皿中,缓慢加热浓缩至表面出现结晶薄膜为止,放置冷却。
步骤五:经过一系列操作,最终得到较纯净的(NH4)2FeSO4·6H2O。
(1)步骤一中加入10%Na2CO3溶液,小火加热30分钟的目的是
(2)关于步骤五中的一系列操作的相关表述,错误的是_____(填字母)。
| A.过滤时可使用玻璃棒搅拌的方式来缩短时间 |
| B.过滤和洗涤的速度都要尽可能的快,可以减少产品的氧化 |
| C.洗涤时使用无水乙醇既可以洗去晶体表面的杂质离子,又可以起到干燥作用 |
| D.所得的产品可以采取电热炉烘干的方式彻底干燥 |
II.硫酸亚铁铵的分解
已知硫酸亚铁铵在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全,确定分解产物的成分。

(4)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定分解产物中含有
(5)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3而不含FeO。其预期实验现象为:
| 实验步骤 | 预期现象 | 结论 |
| ①取少量A中残留物于试管中,加入适量稀硫酸,充分振荡便其完全溶解; ②将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶 液 | _____ | 固体残留物仅为Fe2O3 |
您最近一年使用:0次
3 . 从矿石中提取金(Au)是获取贵金属的主要来源,工业上常以 溶液、氨水和
溶液、氨水和 溶液为原料配制浸金液{含
溶液为原料配制浸金液{含 }。
}。
已知:① 在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的
在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的 。
。
②几种物质或离子的颜色如表所示:
回答下列问题:
(1) 中提供空轨道的为
中提供空轨道的为_______ (填名称,下同),配体为_______ 。配制过程中氨水需过量,其原因是_______ 。
某科研小组对该浸金液的浸金原理进行探究:
提出猜想:
猜想一: 吸附在金表面,在
吸附在金表面,在 的作用下生成
的作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 被空气中的氧气氧化成
被空气中的氧气氧化成 参与循环。
参与循环。
猜想二: 吸附在金表面,在氧气作用下生成
吸附在金表面,在氧气作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 与
与 生成的
生成的 参与循环。
参与循环。
验证猜想:
(2)俗话说“真金不怕火炼”,从化学性质的角度说明:_______ 。据此有人得出结论:猜想二不成立,但有人觉得溶液的酸碱性对物质的性质有一定影响,为验证猜想二是否成立,设计如下实验:
步骤一:用pH试纸测浸金液的pH,其操作为_______ 。
步骤二:配制与浸金液pH相同的 溶液。用
溶液。用 固体配制一定物质的量浓度的
固体配制一定物质的量浓度的 溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、
溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、_______ 。
步骤三:将一块金片放入配制的 溶液中,并通入空气,一段时间后,若观察到
溶液中,并通入空气,一段时间后,若观察到_______ ,则猜想二可能成立。
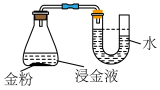
(3)某小组设计如图所示实验验证猜想一。_______ (填锥形瓶中出现的实验现象),则猜想一可能成立;打开瓶塞后的现象用离子方程式表示为_______ 。
 溶液、氨水和
溶液、氨水和 溶液为原料配制浸金液{含
溶液为原料配制浸金液{含 }。
}。已知:①
 在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的
在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的 。
。②几种物质或离子的颜色如表所示:
| 物质或离子 | Au | 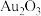 |  |  |  |
| 颜色 | 黄色 | 棕黑 | 蓝色 | 无色 | 无色 |
(1)
 中提供空轨道的为
中提供空轨道的为某科研小组对该浸金液的浸金原理进行探究:
提出猜想:
猜想一:
 吸附在金表面,在
吸附在金表面,在 的作用下生成
的作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 被空气中的氧气氧化成
被空气中的氧气氧化成 参与循环。
参与循环。猜想二:
 吸附在金表面,在氧气作用下生成
吸附在金表面,在氧气作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 与
与 生成的
生成的 参与循环。
参与循环。验证猜想:
(2)俗话说“真金不怕火炼”,从化学性质的角度说明:
步骤一:用pH试纸测浸金液的pH,其操作为
步骤二:配制与浸金液pH相同的
 溶液。用
溶液。用 固体配制一定物质的量浓度的
固体配制一定物质的量浓度的 溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、
溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、步骤三:将一块金片放入配制的
 溶液中,并通入空气,一段时间后,若观察到
溶液中,并通入空气,一段时间后,若观察到(3)某小组设计如图所示实验验证猜想一。
您最近一年使用:0次
4 . 甲醛是有毒气体,某实验小组探究能否用氨水吸收甲醛。
Ⅰ.甲醛溶液的制备与浓度测定
已知制备甲醛的反应原理如下:
①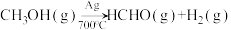
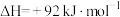
②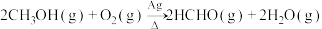
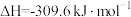
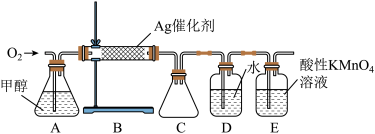
实验室制备甲醛溶液的装置如图所示。(加热装置已略去)
回答下列问题:
(1)装置A中盛放甲醇的仪器名称为___________ 。
(2)从能量利用的角度说明 的作用是
的作用是___________ ;为了防止高温下甲醛在催化剂表面吸附太久被 进一步氧化为甲酸,可采取的措施是
进一步氧化为甲酸,可采取的措施是___________ 。
(3)实验结束后,取5mL新制 悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应的化学方程式为
悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应的化学方程式为___________ 。
(4)甲醛溶液的浓度测定:装置D的溶液经预处理后,取10.00mL稀释至200mL,移取20.00mL稀释液于碘量瓶中,加入 溶液和指示剂,振荡,静置5分钟后用0.1000
溶液和指示剂,振荡,静置5分钟后用0.1000
 标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗
标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗 标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为
标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为___________  (计算结果保留四位有效数字)。(已知:
(计算结果保留四位有效数字)。(已知: )
)
Ⅱ.甲醛与氨水反应的实验探究
实验探究(ⅰ)
(5)实验1的目的是___________ 。
关于实验3褪色的原因,小组成员提出了以下猜想:
猜想①:甲醛与氨水发生反应,溶液碱性减弱,酚酞溶液褪色。
猜想②:甲醛与酚酞溶液发生反应,指示剂失效,溶液褪色。
实验探究(ⅱ)
(6)实验5的操作为___________ 。由实验4、5说明猜想___________ (填标号)正确。
Ⅰ.甲醛溶液的制备与浓度测定
已知制备甲醛的反应原理如下:
①
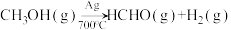
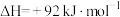
②
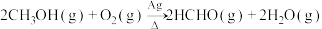
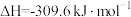
实验室制备甲醛溶液的装置如图所示。(加热装置已略去)

回答下列问题:
(1)装置A中盛放甲醇的仪器名称为
(2)从能量利用的角度说明
 的作用是
的作用是 进一步氧化为甲酸,可采取的措施是
进一步氧化为甲酸,可采取的措施是(3)实验结束后,取5mL新制
 悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应的化学方程式为
悬浊液,滴入适量的装置D的溶液,加热,有砖红色沉淀生成,反应的化学方程式为(4)甲醛溶液的浓度测定:装置D的溶液经预处理后,取10.00mL稀释至200mL,移取20.00mL稀释液于碘量瓶中,加入
 溶液和指示剂,振荡,静置5分钟后用0.1000
溶液和指示剂,振荡,静置5分钟后用0.1000
 标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗
标准溶液滴定生成的NaOH至终点,重复三次实验,平均消耗 标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为
标准溶液体积为20.00mL。则所制得的溶液中甲醛浓度为 (计算结果保留四位有效数字)。(已知:
(计算结果保留四位有效数字)。(已知: )
)Ⅱ.甲醛与氨水反应的实验探究
实验探究(ⅰ)
| 实验编号 | 操作 | 现象 |
| 1 | 取适量D的溶液,用pH计测溶液的pH | pH≈7.0 |
| 2 | 取2mL2%氨水(滴有酚酞),逐滴加入3mL10%甲醇溶液 | 没有明显变化 |
| 3 | 取2mL2%氨水(滴有酚酞),逐滴加入装置D的溶液 | 红色褪去 |
关于实验3褪色的原因,小组成员提出了以下猜想:
猜想①:甲醛与氨水发生反应,溶液碱性减弱,酚酞溶液褪色。
猜想②:甲醛与酚酞溶液发生反应,指示剂失效,溶液褪色。
实验探究(ⅱ)
| 实验编号 | 操作 | 现象 |
| 4 | 取实验3的无色溶液1mL,滴入几滴氨水 | 溶液变红 |
| 5 | 无明显变化 |
您最近一年使用:0次
名校
解题方法
5 . 某兴趣小组同学探究KMnO4溶液与草酸(H2C2O4)溶液反应速率的影响因素。配制1.0×10-3mol/LKMnO4溶液、0.40mol/L草酸溶液。将KMnO4溶液与草酸溶液按如下比例混合。
【设计实验】
(1)实验①和②的目的是___________ 。
(2)甲认为上述实验应控制pH相同,可加入的试剂是___________ (填序号)。
a.盐酸 b.硫酸 c.草酸
【实施实验】
小组同学将溶液pH调至1并进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:
i.紫色溶液转变为青色溶液,ii.青色溶液逐渐褪至无色溶液。
资料:(a) 无色,在草酸中不能形成配合物;
无色,在草酸中不能形成配合物;
(b) 无色,有强氧化性,发生反应
无色,有强氧化性,发生反应 (青绿色)后氧化性减弱;
(青绿色)后氧化性减弱;
(c) 呈绿色,在酸性条件下不稳定,迅速分解产生
呈绿色,在酸性条件下不稳定,迅速分解产生 和
和 。
。
(3)乙同学从氧化还原角度推测阶段i中可能产生 ,你认为该观点是否合理,并说明理由:
,你认为该观点是否合理,并说明理由:___________ 。
【继续探究】
进一步实验证明溶液中含有 ,反应过程中
,反应过程中 和
和 浓度随时间的变化如下图。
浓度随时间的变化如下图。
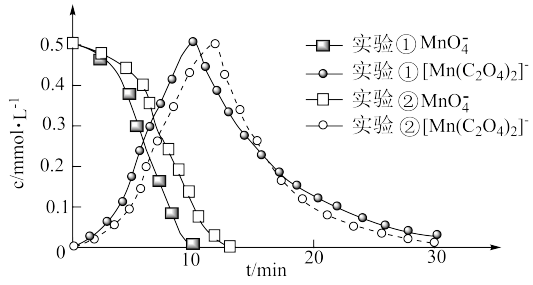
(4)第i阶段中检测到有 气体产生,反应的离子方程式为
气体产生,反应的离子方程式为___________ 。
(5)实验②在第ii阶段的反应速率较大,可能的原因是___________ 。
(6)据此推测,若在第ii阶段将 调节至
调节至 ,溶液褪至无色的时间会
,溶液褪至无色的时间会___________ (填“增加”“减少”或“不变”)。
【结论与反思】
(7)上述实验涉及的反应中,草酸的作用是___________ 。
结论:反应可能是分阶段进行的。草酸浓度的改变对不同阶段反应速率的影响可能不同。
【设计实验】
| 序号 | 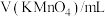 | 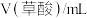 | 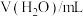 | 反应温度/℃ |
| ① | 2.0 | 2.0 | 0 | 20 |
| ② | 2.0 | 1.0 | 1.0 | 20 |
(2)甲认为上述实验应控制pH相同,可加入的试剂是
a.盐酸 b.硫酸 c.草酸
【实施实验】
小组同学将溶液pH调至1并进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:
i.紫色溶液转变为青色溶液,ii.青色溶液逐渐褪至无色溶液。
资料:(a)
 无色,在草酸中不能形成配合物;
无色,在草酸中不能形成配合物;(b)
 无色,有强氧化性,发生反应
无色,有强氧化性,发生反应 (青绿色)后氧化性减弱;
(青绿色)后氧化性减弱;(c)
 呈绿色,在酸性条件下不稳定,迅速分解产生
呈绿色,在酸性条件下不稳定,迅速分解产生 和
和 。
。(3)乙同学从氧化还原角度推测阶段i中可能产生
 ,你认为该观点是否合理,并说明理由:
,你认为该观点是否合理,并说明理由:【继续探究】
进一步实验证明溶液中含有
 ,反应过程中
,反应过程中 和
和 浓度随时间的变化如下图。
浓度随时间的变化如下图。
(4)第i阶段中检测到有
 气体产生,反应的离子方程式为
气体产生,反应的离子方程式为(5)实验②在第ii阶段的反应速率较大,可能的原因是
(6)据此推测,若在第ii阶段将
 调节至
调节至 ,溶液褪至无色的时间会
,溶液褪至无色的时间会【结论与反思】
(7)上述实验涉及的反应中,草酸的作用是
结论:反应可能是分阶段进行的。草酸浓度的改变对不同阶段反应速率的影响可能不同。
您最近一年使用:0次
2022-04-01更新
|
1366次组卷
|
8卷引用:超重点8 碳酸盐、草酸盐的创新考查
超重点8 碳酸盐、草酸盐的创新考查(已下线)北京市海淀区2022届高三一模(实验探究题)北京市海淀区2022届高三一模化学试题(已下线)必刷卷03-2022年高考化学考前信息必刷卷(河北专用)北京市第二中学2022-2023学年高二上学期10月月考化学试题北京第一零一中学2023届高三10月月考化学试题北京市第二十中学2022-2023学年高三上学期12月月考化学试题北京师范大学附属中学2022-2023学年高二上学期10月月考化学试题
2021高一·全国·专题练习
6 . 四个化学小组的同学测定某Na2CO3固体样品(仅含NaCl杂质)的纯度,他们提出了各自的气体分析法。


(1)第一小组用图 Ⅰ 所示装置,把m1 g的混合物与足量稀硫酸反应后,测定产生CO2气体的体积。实验开始时需检查该装置气密性,具体的操作方法是_______ 。
(2)第二小组用图Ⅱ装置测量CO2的质量。该装置存在的明显缺陷是_______ 。
(3)第三小组在第二小组装置的基础上,解决了第二小组装置的问题。所用到的仪器如图Ⅲ,装置的连接顺序是a→_______ (填写接口字母,图中仪器可重复使用)。实验中取了样品m1 g,称量干燥管质量为m2 g;与足量稀硫酸反应后称量干燥管质量为m3 g,则Na2CO3的纯度表达式为_______ 。
(4)第四小组设计用沉淀法来测量。方案是滴加沉淀剂使碳酸钠转化为沉淀,然后过滤、洗涤、干燥后称量沉淀质量。经讨论认为需要用Ba(OH)2溶液代替澄清石灰水来作沉淀剂的原因是_______ (填字母)。
a.Ba(OH)2比Ca(OH)2便宜
b.Ba(OH)2溶解度大于Ca(OH)2,可以增大Ba(OH)2浓度,无需加入过大体积的沉淀剂
c.相同条件下,CaCO3的溶解度明显小于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小


(1)第一小组用图 Ⅰ 所示装置,把m1 g的混合物与足量稀硫酸反应后,测定产生CO2气体的体积。实验开始时需检查该装置气密性,具体的操作方法是
(2)第二小组用图Ⅱ装置测量CO2的质量。该装置存在的明显缺陷是
(3)第三小组在第二小组装置的基础上,解决了第二小组装置的问题。所用到的仪器如图Ⅲ,装置的连接顺序是a→
(4)第四小组设计用沉淀法来测量。方案是滴加沉淀剂使碳酸钠转化为沉淀,然后过滤、洗涤、干燥后称量沉淀质量。经讨论认为需要用Ba(OH)2溶液代替澄清石灰水来作沉淀剂的原因是
a.Ba(OH)2比Ca(OH)2便宜
b.Ba(OH)2溶解度大于Ca(OH)2,可以增大Ba(OH)2浓度,无需加入过大体积的沉淀剂
c.相同条件下,CaCO3的溶解度明显小于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
您最近一年使用:0次
名校
7 . 铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。
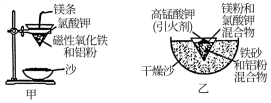
(1)某校化学兴趣小组同学,取磁性氧化铁按如图甲中的实验装置进行铝热反应,现象很壮观。指明使用镁条和氯酸钾的目的是__ ;
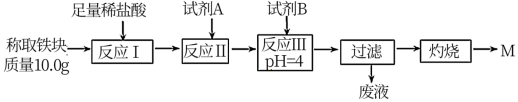
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见红色。为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示。
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
①试剂A为 溶液,写出反应II的离子方程式
溶液,写出反应II的离子方程式_______ ;
②反应III调节溶液 的目的是
的目的是_______ ;
③设计简单实验证明M的成分是 而非
而非 。
。
(限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水)
④若最终红棕色粉未M的质量为12.0g,则该“铁块”的纯度是_______ ;

(1)某校化学兴趣小组同学,取磁性氧化铁按如图甲中的实验装置进行铝热反应,现象很壮观。指明使用镁条和氯酸钾的目的是
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见红色。为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示。

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
 |  |  |  | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完成时的pH | 9.0 | 4.0 | 5 | 11 |
 溶液,写出反应II的离子方程式
溶液,写出反应II的离子方程式②反应III调节溶液
 的目的是
的目的是③设计简单实验证明M的成分是
 而非
而非 。
。(限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水)
| 操作 | 预期现象 |
| 取少量M固体于试管中,向其中加入 | 固体完全溶解,溶液呈黄色 |
| 继续向上述溶液中滴入 |
您最近一年使用:0次
2021-04-28更新
|
522次组卷
|
5卷引用:第08讲 铝、镁及其重要化合物(精练)-2022年高考化学一轮复习讲练测
(已下线)第08讲 铝、镁及其重要化合物(精练)-2022年高考化学一轮复习讲练测(已下线)第4讲 镁、铝及其化合物江苏省常熟市2020-2021学年高一下学期期中化学试题江西省宁冈中学2021-2022学年高三上学期9月份开学考化学试题 上海交通大学附属中学2022-2023学年高二上学期开学摸底考试化学试题
8 . 以下是生活中常用的几种消毒剂。
i.“84”消毒液,有效成分是NaClO。
ii.消毒液A,其有效成分的结构简式为 (简称PCMX)。
(简称PCMX)。
ⅲ.双氧水消毒液,是质量分数为3%~25%的 溶液。
溶液。
(1)“84”消毒液需要在阴暗处密封保存,否则容易失效,用化学用语解释其原因:
① ;②
;②___________ 。
(2)实验室通过测定不同pH环境中不同浓度NaClO溶液的细菌杀灭率(%),以探究“84”消毒液杀菌能力的影响因素,实验结果如下表。
①结合表中数据可推断,相同条件下,HClO的杀菌能力___________ (填“强于”“弱于”或“相当于”)NaClO的杀菌能力。
②下列关于“84”消毒液及其使用方法的描述中,正确的是___________ (填字母序号)。
a.“84”消毒液的杀菌能力与其浓度有关
b.长期用于对金属制品消毒,不会使金属腐蚀
c.不能与清厕灵(含HCl)混合使用,可能会导致安全事故
d.喷洒在物品表面后适当保持一段时间,以达到消毒杀菌效果
(3)消毒液A常用于家庭衣物消毒。
①PCMX分子中的含氧官能是___________ (写名称)。
②若将消毒液A与“84”消毒液混合使用,会大大降低消毒效果,从物质性的角度解释其原因为____ 。
(4)研究小组将某“84”消毒液与双氧水消毒液等体积混合,有大量无色气体生成,经检验为氧气。用离子方程式表示生成氧气的可能原因: 、
、____ 。
i.“84”消毒液,有效成分是NaClO。
ii.消毒液A,其有效成分的结构简式为
 (简称PCMX)。
(简称PCMX)。 ⅲ.双氧水消毒液,是质量分数为3%~25%的
 溶液。
溶液。(1)“84”消毒液需要在阴暗处密封保存,否则容易失效,用化学用语解释其原因:
①
 ;②
;②(2)实验室通过测定不同pH环境中不同浓度NaClO溶液的细菌杀灭率(%),以探究“84”消毒液杀菌能力的影响因素,实验结果如下表。
| NaClO溶液浓度(mg/L) | 不同pH下的细菌杀灭率(%) | ||
| pH=4.5 | pH=7.0 | pH=9.5 | |
| 250 | 98.90 | 77.90 | 53.90 |
| 500 | 99.99 | 97.90 | 65.54 |
②下列关于“84”消毒液及其使用方法的描述中,正确的是
a.“84”消毒液的杀菌能力与其浓度有关
b.长期用于对金属制品消毒,不会使金属腐蚀
c.不能与清厕灵(含HCl)混合使用,可能会导致安全事故
d.喷洒在物品表面后适当保持一段时间,以达到消毒杀菌效果
(3)消毒液A常用于家庭衣物消毒。
①PCMX分子中的含氧官能是
②若将消毒液A与“84”消毒液混合使用,会大大降低消毒效果,从物质性的角度解释其原因为
(4)研究小组将某“84”消毒液与双氧水消毒液等体积混合,有大量无色气体生成,经检验为氧气。用离子方程式表示生成氧气的可能原因:
 、
、
您最近一年使用:0次
2021-04-09更新
|
719次组卷
|
3卷引用:第九章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测
名校
解题方法
9 . 某学习小组探究某浓度浓硝酸和稀硝酸与铁的反应。
(1)Ⅰ中液面上方气体由无色变为红棕色的化学方程式为_______ 。
(2)取少量Ⅰ中溶液,加入KSCN溶液,_______ (填现象),说明产生了Fe3+。
(3)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明硝酸具有_______ 性。
(4)Ⅲ中,连接导线后体系形成了原电池。为分析反应过程,在Fe、Cu之间连接电流计,实验如下。
①用方程式解释现象ⅳ:_______ 。
②推测现象ⅰ中被还原的是_______ 。
③解释现象ii中指针左右偏转,往复多次的原因_______ 。
④现象ⅲ中,Fe一直做负极,难以形成氧化层,可能的原因是_______ 。
| 实验 | 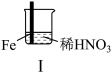 | 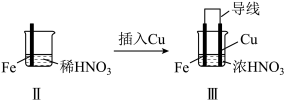 | |
| 现象 | Ⅰ中:Fe表面产生大量无色气泡,液面上方变为红棕色 | Ⅱ中:Fe表面产生红棕色气泡,过一会儿停止 | Ⅲ中:连接导线,一段时间后Fe表面产生红棕色气泡,而后停止;随即又产生红棕色气泡,而后停止,……如此往复多次。Cu表面始终产生红棕色气泡 |
(2)取少量Ⅰ中溶液,加入KSCN溶液,
(3)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明硝酸具有
(4)Ⅲ中,连接导线后体系形成了原电池。为分析反应过程,在Fe、Cu之间连接电流计,实验如下。
| 实验 | 现象 |
 | ⅰ.K闭合时,指针向左偏转(Cu做负极),Fe表面无明显现象 ⅱ.过一会儿指针向右偏,Fe表面产生红棕色气体;后又迅速向左偏,Fe表面停止产生气泡,……如此往复多次 ⅲ.一段时间后,指针一直处于右端,Fe表面持续产生红棕色气体 ⅳ.Cu表面始终产生红棕色气泡 |
②推测现象ⅰ中被还原的是
③解释现象ii中指针左右偏转,往复多次的原因
④现象ⅲ中,Fe一直做负极,难以形成氧化层,可能的原因是
您最近一年使用:0次
2021-04-05更新
|
841次组卷
|
5卷引用:押山东卷第20题 化学实验综合题-备战2021年高考化学临考题号押题(山东卷)
(已下线)押山东卷第20题 化学实验综合题-备战2021年高考化学临考题号押题(山东卷)北京市朝阳区2021届高三一模化学试题2021年北京高考化学试题变式题11-19辽宁省葫芦岛市普通高中2021-2022学年高三上学期期末学业质量监测化学试题北京市顺义区第一中学2023-2024学年高三上学期期中考试化学试题
10 . 某小组为探究Mg与NH4Cl溶液反应机理,常温下进行以下实验。实验中所取镁粉质量均为0.5g,分别加入到选取的实验试剂中。
资料:①CH3COONH4溶液呈中性。
②Cl-对该反应几乎无影响。
(1)经检验实验2中刺激性气味气体为NH3,检验方法是____ 。用排水法收集一小试管产生的气体,经检验小试管中气体为H2。
(2)已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有____ ,灰白色固体可能是____ (填化学式)。
(3)甲同学认为实验2比实验1反应剧烈的原因是NH4Cl溶液中c(H+)大,与Mg反应快。用化学用语解释NH4Cl溶液显酸性的原因是_____ 。
(4)乙同学通过实验3证明甲同学的说法不合理 。
①试剂X是_______ 。
②由实验3获取的证据为_______ 。
(5)为进一步探究实验2反应剧烈的原因,进行实验4。
依据上述实验,可以得出Mg能与 反应生成H2。乙同学认为该方案不严谨,需要补充的实验方案是
反应生成H2。乙同学认为该方案不严谨,需要补充的实验方案是_______ 。
(6)由以上实验可以得出的结论是_______ 。
资料:①CH3COONH4溶液呈中性。
②Cl-对该反应几乎无影响。
| 实验 | 实验试剂 | 实验现象 |
| 1 | 5mL蒸馏水 | 反应缓慢,有少量气泡产生(经检验为H2) |
| 2 | 5mL 1.0 mol/L NH4Cl溶液(pH=4.6) | 剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
(2)已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有
(3)甲同学认为实验2比实验1反应剧烈的原因是NH4Cl溶液中c(H+)大,与Mg反应快。用化学用语解释NH4Cl溶液显酸性的原因是
(4)乙同学通过实验3证明甲同学的说法
| 实验 | 实验装置 |
| 3 | 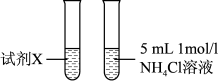 |
②由实验3获取的证据为
(5)为进一步探究实验2反应剧烈的原因,进行实验4。
| 实验 | 实验试剂 | 实验现象 |
| 4 | 5 mL NH4Cl乙醇溶液 | 有无色无味气体产生(经检验为H2) |
 反应生成H2。乙同学认为该方案不严谨,需要补充的实验方案是
反应生成H2。乙同学认为该方案不严谨,需要补充的实验方案是(6)由以上实验可以得出的结论是
您最近一年使用:0次



