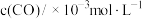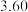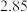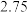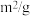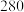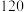名校
1 . 利用催化技术可将汽车尾气中的CO和NO转化为 和
和 ,化学方程式:
,化学方程式: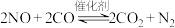 。
。
(1)某温度下,在恒容的密闭容器中通入CO和NO,测得不同时间CO的浓度如下表:
用CO的浓度变化表示0-2s的平均反应速率为______  。
。
(2)下列可说明反应达到平衡状态的是______ 。
a.CO的浓度不再改变
b.容器中的气体质量保持不变
c.NO、CO、 、
、 的浓度之比为2∶2∶2∶1
的浓度之比为2∶2∶2∶1
d.相同时间内,反应消耗2molNO同时消耗
(3)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
【实验分析与结论】
①补全表格a.______ ,b.______ ,c.______ 。
②测得 ,对比实验Ⅰ、Ⅲ,可得结论:
,对比实验Ⅰ、Ⅲ,可得结论:______ 。
③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验Ⅰ、Ⅱ,
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 和
和 ,化学方程式:
,化学方程式: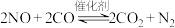 。
。(1)某温度下,在恒容的密闭容器中通入CO和NO,测得不同时间CO的浓度如下表:
时间 |
|
|
|
| …… |
|
|
|
|
| …… |
 。
。(2)下列可说明反应达到平衡状态的是
a.CO的浓度不再改变
b.容器中的气体质量保持不变
c.NO、CO、
 、
、 的浓度之比为2∶2∶2∶1
的浓度之比为2∶2∶2∶1d.相同时间内,反应消耗2molNO同时消耗

(3)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
实验编号 | 实验目的 |
| 同种催化剂的比表面积 | 达平衡时所用的时间 |
Ⅰ | 对照实验 |
|
|
|
Ⅱ |
|
|
|
|
Ⅲ | 研究温度对尾气转化速率的影响 |
|
|
|
①补全表格a.
②测得
 ,对比实验Ⅰ、Ⅲ,可得结论:
,对比实验Ⅰ、Ⅲ,可得结论:③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验Ⅰ、Ⅱ,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
2024-05-08更新
|
99次组卷
|
5卷引用:北京市西城区2020-2021学年高一下学期期末联考化学试题
北京市西城区2020-2021学年高一下学期期末联考化学试题(已下线)重难点02 速率与平衡综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)北京市第十四中学2022-2023学年高一下学期期中化学试题北京市第三中学2022-2023学年高一下学期期中考试化学试题北京市第二十二中学2023-2024学年高一下学期期中考试化学试题
名校
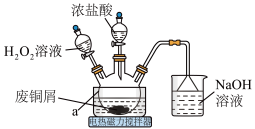
2 . CuCl2是常见的化学试剂,某小组利用废铜屑“湿法”制备CuCl2·2H2O并开展相关探究。
回答下列问题:
(1)仪器a的名称为___________ 。
(2)上述方法制备CuCl2的离子方程式为___________ 。
(3)为得到纯净的CuCl2·2H2O晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入 气体,加热蒸发浓缩,
气体,加热蒸发浓缩,___________ ,过滤,洗涤,低温干燥。持续通入 气体的目的是
气体的目的是___________ 。
(4)实验中,H2O2的实际用量要大于理论用量,可能因素为:原因1:___________ ;原因2:生成的CuCl2催化了H2O2的分解。
(5)该小组对“原因2”进行拓展探究。为验证CuCl2对H2O2分解的催化作用,该小组向5支盛有10mL5%H2O2的试管中滴加不同溶液,实验记录如下表(忽略溶液体积的微小变化;已知一定条件下,还原产物的浓度越小,氧化剂的氧化性越强):
①实验Ⅳ过程中观察到有白色沉淀(经检验为CuCl)生成,反应的机理表示为
第一步:H2O2+2Cu2++2Cl-=O2↑+2CuCl+2H+;
第二步:___________ (写离子方程式)。
②已知化学反应速率第一步<第二步,则气泡产生速率实验Ⅳ比实验Ⅲ加快的原因:___________ 。
③分析上述实验,下列说法正确的是___________ (填字母)。
A.实验Ⅰ的目的是证明仅有NaCl对H2O2分解没有催化作用
B. 对H2O2分解有显著催化作用
对H2O2分解有显著催化作用
C.Cl-增强了Cu2+对H2O2分解的催化效果,且Cl-浓度越大催化效果越强
④写出一种H2O2的用途___________ 。
| 温度 | 15℃以下 | 15~25.7℃ | 26~42℃ | 42℃以上 |
| 结晶水合物 | CuCl2·4H2O | CuCl2·3H2O | CuCl2·2H2O | CuCl2·H2O |
(1)仪器a的名称为
(2)上述方法制备CuCl2的离子方程式为
(3)为得到纯净的CuCl2·2H2O晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入
 气体,加热蒸发浓缩,
气体,加热蒸发浓缩, 气体的目的是
气体的目的是(4)实验中,H2O2的实际用量要大于理论用量,可能因素为:原因1:
(5)该小组对“原因2”进行拓展探究。为验证CuCl2对H2O2分解的催化作用,该小组向5支盛有10mL5%H2O2的试管中滴加不同溶液,实验记录如下表(忽略溶液体积的微小变化;已知一定条件下,还原产物的浓度越小,氧化剂的氧化性越强):
| 实验 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| 滴加试剂 | 2滴1mol/LNaCl | 2滴1mol/LNa2SO4 | 2滴1mol/LCuSO4 | 2滴1mol/LCuSO4和2滴1mol/LNaCl | 2滴1mol/LCuSO4和4滴1mol/LNaCl |
| 现象 | 无气泡产生 | 无气泡产生 | 均产生气泡,且气泡速率从Ⅲ到Ⅴ依次加快 | ||
第一步:H2O2+2Cu2++2Cl-=O2↑+2CuCl+2H+;
第二步:
②已知化学反应速率第一步<第二步,则气泡产生速率实验Ⅳ比实验Ⅲ加快的原因:
③分析上述实验,下列说法正确的是
A.实验Ⅰ的目的是证明仅有NaCl对H2O2分解没有催化作用
B.
 对H2O2分解有显著催化作用
对H2O2分解有显著催化作用C.Cl-增强了Cu2+对H2O2分解的催化效果,且Cl-浓度越大催化效果越强
④写出一种H2O2的用途
您最近一年使用:0次
解题方法
3 . 某小组同学探究实验室配制银氨溶液并检验醛基的方法。
资料:i.AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的 。
。
ii.向硝酸银溶液中加入氨水,转化为 的
的 占参加反应的
占参加反应的 总量的百分比最大不超过10%。
总量的百分比最大不超过10%。
Ⅰ.在实验室配制银氨溶液的过程中,小组同学发现,所用试剂的配制方式和存放时间不同,实验现象不同。(注:以下试剂若无特殊说明,均为新制)
(1)NH3分子空间构型为_______ 。
(2)结合资料ii,写出实验1中加入少量氨水时发生的主要反应的离子方程式_______ 。
(3)已知,实验2中白色沉淀加硝酸产生能使澄清石灰水变浑浊的无色气体,实验2中白色沉淀的主要成分是_______ 。
(4)对比实验1和3,分析实验3中“溶液始终澄清”的原因是_______ 。
Ⅱ.用实验1配制出的银氨溶液检验醛基。
资料:可从电极反应角度分析物质氧化性和还原性的变化。
(5)银氨溶液与CH3CHO的反应中,电极反应式:
还原反应:Ag++e-=Ag;氧化反应:_______ (碱性条件下)。
在此基础上设计并实施了以下实验。
(6)实验5产生银镜比实验4快的可能原因是_______ 。按照实验5的方法,将乙醛换成丙酮,水浴加热后也能产生银镜。
综合上述实验,实验4是检验醛基的最合理方法。
资料:i.AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的
 。
。ii.向硝酸银溶液中加入氨水,转化为
 的
的 占参加反应的
占参加反应的 总量的百分比最大不超过10%。
总量的百分比最大不超过10%。Ⅰ.在实验室配制银氨溶液的过程中,小组同学发现,所用试剂的配制方式和存放时间不同,实验现象不同。(注:以下试剂若无特殊说明,均为新制)
| 序号 | 实验操作 | 实验现象 |
| 1 | 向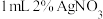 溶液中逐滴加入2%氨水 溶液中逐滴加入2%氨水 | 先产生棕色沉淀,后溶液变澄清 |
| 2 | 向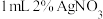 溶液中逐滴加入在空气中存放一段时间的2%氨水 溶液中逐滴加入在空气中存放一段时间的2%氨水 | 先产生白色沉淀,后溶液变澄清 |
| 3 | 向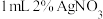 ( ( 酸化)溶液中逐滴加入2%氨水至过量 酸化)溶液中逐滴加入2%氨水至过量 | 溶液始终澄清 |
(2)结合资料ii,写出实验1中加入少量氨水时发生的主要反应的离子方程式
(3)已知,实验2中白色沉淀加硝酸产生能使澄清石灰水变浑浊的无色气体,实验2中白色沉淀的主要成分是
(4)对比实验1和3,分析实验3中“溶液始终澄清”的原因是
Ⅱ.用实验1配制出的银氨溶液检验醛基。
资料:可从电极反应角度分析物质氧化性和还原性的变化。
(5)银氨溶液与CH3CHO的反应中,电极反应式:
还原反应:Ag++e-=Ag;氧化反应:
在此基础上设计并实施了以下实验。
| 序号 | 实验操作 | 实验现象 |
| 4 | 向银氨溶液中加入3滴 ,水浴加热 ,水浴加热 | 产生银镜 |
| 5 | 向银氨溶液中加入1滴10% NaOH溶液后,滴入3滴 | 产生银镜比实验4快 |
综合上述实验,实验4是检验醛基的最合理方法。
您最近一年使用:0次
4 . H2O2被称为“最清洁的消毒剂”,国家卫生健康委办公厅印发了《消毒剂使用指南),其中明确指定过氧化氢为新冠病毒消毒剂之一, 适用于物体表面、室内空气的消毒等。
(1)写出H2O2的结构式:___________ 。
Fe3+可用作H2O2分解的催化剂,反应的机理为:
①Fe3++ H2O2=Fe2++H++·OOH
②H2O2+X=Y+Z+W
③Fe2++·OH=Fe3++OH-
④H++OH-=H2O
根据上述机理推导步骤②中的化学方程式为___________ 。
(2)①H2O2是一种二元弱酸,它与少量的Ba (OH)2反应的化学方程式为___________ 。
②H2O2还能使酸性KMnO4溶液褪色,写出反应的离子方程式_____ 。
(3)现一种制备H2O2的一种工艺简单、能耗低的方法,反应原理如图所示,该制备反应的总反应方程式为_____ 。

(4)科学家对H2O2分子结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲: 、乙:H−O−O−H,甲式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的分子结构,设计并完成了下列实验:
、乙:H−O−O−H,甲式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的分子结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5) 2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式):___________ 。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d, 请设计d的实验方案______ 。
(1)写出H2O2的结构式:
Fe3+可用作H2O2分解的催化剂,反应的机理为:
①Fe3++ H2O2=Fe2++H++·OOH
②H2O2+X=Y+Z+W
③Fe2++·OH=Fe3++OH-
④H++OH-=H2O
根据上述机理推导步骤②中的化学方程式为
(2)①H2O2是一种二元弱酸,它与少量的Ba (OH)2反应的化学方程式为
②H2O2还能使酸性KMnO4溶液褪色,写出反应的离子方程式
(3)现一种制备H2O2的一种工艺简单、能耗低的方法,反应原理如图所示,该制备反应的总反应方程式为

(4)科学家对H2O2分子结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲:
 、乙:H−O−O−H,甲式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的分子结构,设计并完成了下列实验:
、乙:H−O−O−H,甲式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的分子结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5) 2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式):
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d, 请设计d的实验方案
您最近一年使用:0次
5 . 某实验小组自制如图水果电池,探究影响电池效果的因素有哪些,制成记录表格如下:

请回答下列问题:
(1)水果电池中,水果的作用是_______ 。
(2)实验③④⑤的目的是探究_______ ;对比实验③④⑤得出结论是_______ 。
(3)欲得出“水果种类对电池效果有影响”的结论需要对比实验_______ 。

| 序号 | 电极 | 电极间距( ) ) | 水果种类 | 电流表(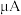 ) ) |
| ① |  | 1.0 | 柠檬 | 98.4 |
| ② |  | 2.0 | 柠檬 | 45.7 |
| ③ |  | 2.0 | 西红柿 | 78.8 |
| ④ |  | 2.0 | 西红柿 | 70.3 |
| ⑤ |  | 2.0 | 西红柿 | 0 |
(1)水果电池中,水果的作用是
(2)实验③④⑤的目的是探究
(3)欲得出“水果种类对电池效果有影响”的结论需要对比实验
您最近一年使用:0次
6 . 以下是生活中常用的几种消毒剂。
i.“84”消毒液,有效成分是NaClO。
ii.消毒液A,其有效成分的结构简式为 (简称PCMX)。
(简称PCMX)。
ⅲ.双氧水消毒液,是质量分数为3%~25%的 溶液。
溶液。
(1)“84”消毒液需要在阴暗处密封保存,否则容易失效,用化学用语解释其原因:
① ;②
;②___________ 。
(2)实验室通过测定不同pH环境中不同浓度NaClO溶液的细菌杀灭率(%),以探究“84”消毒液杀菌能力的影响因素,实验结果如下表。
①结合表中数据可推断,相同条件下,HClO的杀菌能力___________ (填“强于”“弱于”或“相当于”)NaClO的杀菌能力。
②下列关于“84”消毒液及其使用方法的描述中,正确的是___________ (填字母序号)。
a.“84”消毒液的杀菌能力与其浓度有关
b.长期用于对金属制品消毒,不会使金属腐蚀
c.不能与清厕灵(含HCl)混合使用,可能会导致安全事故
d.喷洒在物品表面后适当保持一段时间,以达到消毒杀菌效果
(3)消毒液A常用于家庭衣物消毒。
①PCMX分子中的含氧官能是___________ (写名称)。
②若将消毒液A与“84”消毒液混合使用,会大大降低消毒效果,从物质性的角度解释其原因为____ 。
(4)研究小组将某“84”消毒液与双氧水消毒液等体积混合,有大量无色气体生成,经检验为氧气。用离子方程式表示生成氧气的可能原因: 、
、____ 。
i.“84”消毒液,有效成分是NaClO。
ii.消毒液A,其有效成分的结构简式为
 (简称PCMX)。
(简称PCMX)。 ⅲ.双氧水消毒液,是质量分数为3%~25%的
 溶液。
溶液。(1)“84”消毒液需要在阴暗处密封保存,否则容易失效,用化学用语解释其原因:
①
 ;②
;②(2)实验室通过测定不同pH环境中不同浓度NaClO溶液的细菌杀灭率(%),以探究“84”消毒液杀菌能力的影响因素,实验结果如下表。
| NaClO溶液浓度(mg/L) | 不同pH下的细菌杀灭率(%) | ||
| pH=4.5 | pH=7.0 | pH=9.5 | |
| 250 | 98.90 | 77.90 | 53.90 |
| 500 | 99.99 | 97.90 | 65.54 |
②下列关于“84”消毒液及其使用方法的描述中,正确的是
a.“84”消毒液的杀菌能力与其浓度有关
b.长期用于对金属制品消毒,不会使金属腐蚀
c.不能与清厕灵(含HCl)混合使用,可能会导致安全事故
d.喷洒在物品表面后适当保持一段时间,以达到消毒杀菌效果
(3)消毒液A常用于家庭衣物消毒。
①PCMX分子中的含氧官能是
②若将消毒液A与“84”消毒液混合使用,会大大降低消毒效果,从物质性的角度解释其原因为
(4)研究小组将某“84”消毒液与双氧水消毒液等体积混合,有大量无色气体生成,经检验为氧气。用离子方程式表示生成氧气的可能原因:
 、
、
您最近一年使用:0次
2021-04-09更新
|
719次组卷
|
3卷引用:广东省广州市第六中学021-2022学年高一下学期期末考试化学试题
名校
解题方法
7 . 某学习小组探究某浓度浓硝酸和稀硝酸与铁的反应。
(1)Ⅰ中液面上方气体由无色变为红棕色的化学方程式为_______ 。
(2)取少量Ⅰ中溶液,加入KSCN溶液,_______ (填现象),说明产生了Fe3+。
(3)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明硝酸具有_______ 性。
(4)Ⅲ中,连接导线后体系形成了原电池。为分析反应过程,在Fe、Cu之间连接电流计,实验如下。
①用方程式解释现象ⅳ:_______ 。
②推测现象ⅰ中被还原的是_______ 。
③解释现象ii中指针左右偏转,往复多次的原因_______ 。
④现象ⅲ中,Fe一直做负极,难以形成氧化层,可能的原因是_______ 。
| 实验 | 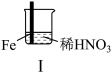 | 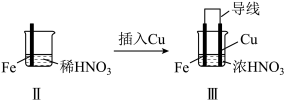 | |
| 现象 | Ⅰ中:Fe表面产生大量无色气泡,液面上方变为红棕色 | Ⅱ中:Fe表面产生红棕色气泡,过一会儿停止 | Ⅲ中:连接导线,一段时间后Fe表面产生红棕色气泡,而后停止;随即又产生红棕色气泡,而后停止,……如此往复多次。Cu表面始终产生红棕色气泡 |
(2)取少量Ⅰ中溶液,加入KSCN溶液,
(3)Ⅱ中现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应。说明硝酸具有
(4)Ⅲ中,连接导线后体系形成了原电池。为分析反应过程,在Fe、Cu之间连接电流计,实验如下。
| 实验 | 现象 |
 | ⅰ.K闭合时,指针向左偏转(Cu做负极),Fe表面无明显现象 ⅱ.过一会儿指针向右偏,Fe表面产生红棕色气体;后又迅速向左偏,Fe表面停止产生气泡,……如此往复多次 ⅲ.一段时间后,指针一直处于右端,Fe表面持续产生红棕色气体 ⅳ.Cu表面始终产生红棕色气泡 |
②推测现象ⅰ中被还原的是
③解释现象ii中指针左右偏转,往复多次的原因
④现象ⅲ中,Fe一直做负极,难以形成氧化层,可能的原因是
您最近一年使用:0次
2021-04-05更新
|
841次组卷
|
5卷引用:辽宁省葫芦岛市普通高中2021-2022学年高三上学期期末学业质量监测化学试题
辽宁省葫芦岛市普通高中2021-2022学年高三上学期期末学业质量监测化学试题北京市朝阳区2021届高三一模化学试题(已下线)押山东卷第20题 化学实验综合题-备战2021年高考化学临考题号押题(山东卷)2021年北京高考化学试题变式题11-19北京市顺义区第一中学2023-2024学年高三上学期期中考试化学试题
解题方法
8 . 2020年新冠肺炎(COVID-19)疫情肆虐全球,含氯消毒剂、过氧化物等均能有效灭活病毒。请回答下列问题:
(1)下列消毒剂中,被称为绿色氧化剂的是_______ (填序号)。
A. B.
B.  C.
C. 
(2) 保存不当会变质生成
保存不当会变质生成 ,某兴趣小组为了探究过氧化钠样品是否变质进行如下操作:取少量样品,用蒸馏水溶解,加入
,某兴趣小组为了探究过氧化钠样品是否变质进行如下操作:取少量样品,用蒸馏水溶解,加入 溶液,振荡,
溶液,振荡,_______ (填现象),证明 已变质;否则,
已变质;否则, 未变质。
未变质。
(3)某兴趣小组设计如图所示实验装置制取少量漂白液。
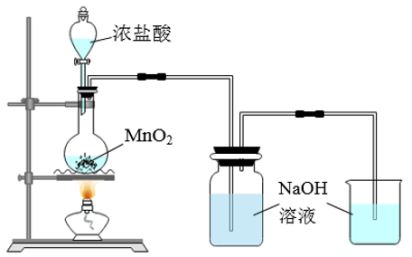
①写出制取漂白液反应的离子方程式:_______ 。
②此实验所得漂白液的有效成分 含量偏低,该小组经分析并查阅资料发现,主要原因是还存在两个副反应:一个副反应是氯气与
含量偏低,该小组经分析并查阅资料发现,主要原因是还存在两个副反应:一个副反应是氯气与 溶液反应放热,温度较高时生成
溶液反应放热,温度较高时生成 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是_______ ;另一个副反应是_______ (写化学方程式)。
(1)下列消毒剂中,被称为绿色氧化剂的是
A.
 B.
B.  C.
C. 
(2)
 保存不当会变质生成
保存不当会变质生成 ,某兴趣小组为了探究过氧化钠样品是否变质进行如下操作:取少量样品,用蒸馏水溶解,加入
,某兴趣小组为了探究过氧化钠样品是否变质进行如下操作:取少量样品,用蒸馏水溶解,加入 溶液,振荡,
溶液,振荡, 已变质;否则,
已变质;否则, 未变质。
未变质。(3)某兴趣小组设计如图所示实验装置制取少量漂白液。

①写出制取漂白液反应的离子方程式:
②此实验所得漂白液的有效成分
 含量偏低,该小组经分析并查阅资料发现,主要原因是还存在两个副反应:一个副反应是氯气与
含量偏低,该小组经分析并查阅资料发现,主要原因是还存在两个副反应:一个副反应是氯气与 溶液反应放热,温度较高时生成
溶液反应放热,温度较高时生成 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是
您最近一年使用:0次
9 . 在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20g已研磨成粉末的Ba(OH)2⋅8H2O,将小烧杯放在事先已滴有3∼4滴水的玻璃片上,然后向烧杯中加入约10gNH4Cl晶体,根据实验步骤,填写下表,并回答问题。

(4)写出实验过程中发生反应的化学方程式:______________________________ ;
(5)该反应在常温下就可进行,说明:____________________________________ 。

| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 |
(5)该反应在常温下就可进行,说明:
您最近一年使用:0次
10 . 染料化工企业产生的废水中含有高浓度的氨氮(氨和铵盐)成分,直接排放会造成环境污染。实验小组探索下列方法对氨氮废水进行处理。

(1)实验室检测上述废水中是否含有氨氮的方法是___ 。
(2)“吹脱”步骤中,在废水池的底部吹入大量热气泡,其目的是___ 。
(3)“氧化”步骤中加入了微生物,NH3被氧化为N2。反应的化学方程式为___ 。
(4)“沉淀"步骤中将剩余的NH3·H2O转化为NH4MgPO4•6H2O沉淀,发生反应的离子方程式为___ 。NH4MgPO4•6H2O在农业生产中具有重要应用价值,其原因是___ 。

(1)实验室检测上述废水中是否含有氨氮的方法是
(2)“吹脱”步骤中,在废水池的底部吹入大量热气泡,其目的是
(3)“氧化”步骤中加入了微生物,NH3被氧化为N2。反应的化学方程式为
(4)“沉淀"步骤中将剩余的NH3·H2O转化为NH4MgPO4•6H2O沉淀,发生反应的离子方程式为
您最近一年使用:0次
2020-07-18更新
|
183次组卷
|
2卷引用:江苏省无锡市普通高中2019-2020学年高一下学期期终调研考试化学试题