名校
解题方法
1 . 加热条件下,硅单质和 反应生成
反应生成 是粗硅提纯的重要步骤,某小组欲用以下装置完成上述转化(夹持装置略去)。
是粗硅提纯的重要步骤,某小组欲用以下装置完成上述转化(夹持装置略去)。

已知: 的沸点为33.0℃,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化,
的沸点为33.0℃,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化, 的沸点为76.8℃。
的沸点为76.8℃。
请回答下列问题:
(1)装置A中浓硫酸体现出的性质是______ 。
(2)g管的作用是______ 。
(3)从装置 所得的液体混合物分离得到
所得的液体混合物分离得到 的实验操作方法是
的实验操作方法是______ 。
(4)以上各个装置的组装顺序为
______ (部分装置可重复使用)。
(5) 在潮湿的空气中被氧化生成一种氧化物和一种无氧酸,该反应的化学方程式为
在潮湿的空气中被氧化生成一种氧化物和一种无氧酸,该反应的化学方程式为______ 。
 反应生成
反应生成 是粗硅提纯的重要步骤,某小组欲用以下装置完成上述转化(夹持装置略去)。
是粗硅提纯的重要步骤,某小组欲用以下装置完成上述转化(夹持装置略去)。
已知:
 的沸点为33.0℃,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化,
的沸点为33.0℃,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化, 的沸点为76.8℃。
的沸点为76.8℃。请回答下列问题:
(1)装置A中浓硫酸体现出的性质是
(2)g管的作用是
(3)从装置
 所得的液体混合物分离得到
所得的液体混合物分离得到 的实验操作方法是
的实验操作方法是(4)以上各个装置的组装顺序为

(5)
 在潮湿的空气中被氧化生成一种氧化物和一种无氧酸,该反应的化学方程式为
在潮湿的空气中被氧化生成一种氧化物和一种无氧酸,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
2 .  溶液是一种铜电路板的蚀刻剂,蚀刻后的废液经过检测其中含有
溶液是一种铜电路板的蚀刻剂,蚀刻后的废液经过检测其中含有 。由该酸性废液X回收
。由该酸性废液X回收 的流程如图所示。下列说法中
的流程如图所示。下列说法中不正确 的是
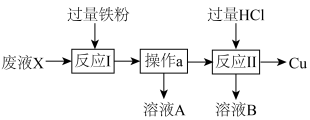
 溶液是一种铜电路板的蚀刻剂,蚀刻后的废液经过检测其中含有
溶液是一种铜电路板的蚀刻剂,蚀刻后的废液经过检测其中含有 。由该酸性废液X回收
。由该酸性废液X回收 的流程如图所示。下列说法中
的流程如图所示。下列说法中
A.废液X中一定存在 |
| B.“反应I”中有1种或2种氧化剂与铁粉反应 |
| C.“操作a”为过滤 |
| D.收集溶液A、B,再通入足量氯气,可实现蚀刻剂的再生 |
您最近一年使用:0次
2023-11-19更新
|
296次组卷
|
4卷引用:浙江省浙南名校2023-2024学年高一下学期开学化学试题
名校
3 . 以MgO、C、Cl2为原料在加热条件下制取无水氯化镁,产物之一为可燃性气体。已知氯化镁冷却过程中易吸收水蒸气生成结晶水合物。
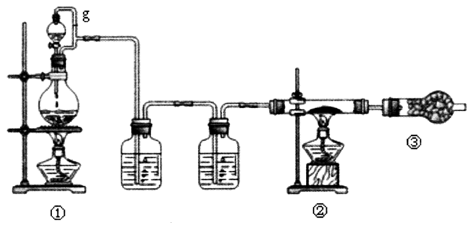
(1)①装置发生反应的离子方程式___ 。②装置中发生反应的化学方程式___ 。
(2)装置①中导管g的作用__ ,装置③干燥管中碱石灰的作用除了吸收多余的氯气之外还有__ 的作用。
(3)尾气处理装置存在缺陷,请提出改进方案__ 。
(4)①装置反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,有同学提出下列具体方案。请你从下列实验方案中选择合理的实验方法__ 。
A.将Cl-转化为AgCl沉淀,测定沉淀的质量
B.与足量锌反应,测量生成气体在标准状况下的体积
C.与足量NaHCO3反应,将得到的气体直接用碱石灰吸收,测定生成气体的质量
D.与足量NaHCO3反应,将得到的气体通入足量澄清石灰水,测定生成沉淀的质量

(1)①装置发生反应的离子方程式
(2)装置①中导管g的作用
(3)尾气处理装置存在缺陷,请提出改进方案
(4)①装置反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,有同学提出下列具体方案。请你从下列实验方案中选择合理的实验方法
A.将Cl-转化为AgCl沉淀,测定沉淀的质量
B.与足量锌反应,测量生成气体在标准状况下的体积
C.与足量NaHCO3反应,将得到的气体直接用碱石灰吸收,测定生成气体的质量
D.与足量NaHCO3反应,将得到的气体通入足量澄清石灰水,测定生成沉淀的质量
您最近一年使用:0次
2020-12-27更新
|
244次组卷
|
2卷引用:浙江省吴兴高级中学2021-2022学年高一下学期返校学情检测化学试题
4 . 实验室用干燥而纯净 的氯气和二氧化硫合成硫酰氯(SO2Cl2),原理为SO2+Cl2 SO2Cl2,装置如图所示(夹持仪器已省略):
SO2Cl2,装置如图所示(夹持仪器已省略):
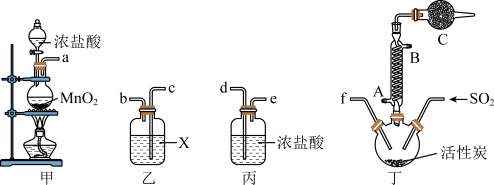
已知有关物质的部分性质如表:
请回答下列问题:
(1)写出甲中制取Cl2的化学方程式___ 。
(2)利用图中甲、乙、丙装置制取干燥纯净的Cl2,并在丁装置合成硫酰氯,要完成实验目的,按气流从左到右,各接口正确的连接顺序是___ 。
A.abcdef B.abcedf C.acbdef D.acbedf
乙中试剂X是___ 。
(3)丁中冷凝管进水口为___ (填“A”或“B”)。装置C的作用是___ 。
(4)硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是___ 。
 SO2Cl2,装置如图所示(夹持仪器已省略):
SO2Cl2,装置如图所示(夹持仪器已省略):
已知有关物质的部分性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易与水反应,产生大量白雾 ②易分解:SO2Cl2  SO2↑+Cl2↑ SO2↑+Cl2↑ |
| H2SO4 | 10.4 | 338 | 不易分解 |
(1)写出甲中制取Cl2的化学方程式
(2)利用图中甲、乙、丙装置制取干燥纯净的Cl2,并在丁装置合成硫酰氯,要完成实验目的,按气流从左到右,各接口正确的连接顺序是
A.abcdef B.abcedf C.acbdef D.acbedf
乙中试剂X是
(3)丁中冷凝管进水口为
(4)硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是
您最近一年使用:0次
名校
解题方法
5 . 某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。
已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。
②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO3-+3H2O
5Cl-+ClO3-+3H2O
该兴趣小组设计了下列实验装置,进行实验。
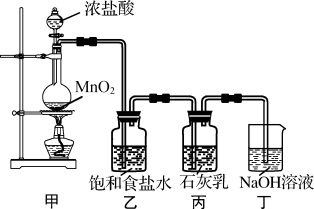
请回答下列问题:
(1)①甲装置用于制备氯气,乙装置的作用是____________________ 。
②该兴趣小组用100mL 12mol/L盐酸与8.7g MnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2____________ g。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,部分氯气未与石灰乳反应而逸出,以及温度升高是可能原因。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。
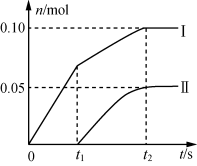
①图中曲线I表示_____________ 离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________ mol。
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37mol,则产物中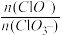 =
=______________ 。
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:_____________ 。
已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。
②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-
 5Cl-+ClO3-+3H2O
5Cl-+ClO3-+3H2O该兴趣小组设计了下列实验装置,进行实验。

请回答下列问题:
(1)①甲装置用于制备氯气,乙装置的作用是
②该兴趣小组用100mL 12mol/L盐酸与8.7g MnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,部分氯气未与石灰乳反应而逸出,以及温度升高是可能原因。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。

①图中曲线I表示
②所取石灰乳中含有Ca(OH)2的物质的量为
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37mol,则产物中
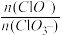 =
=(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:
您最近一年使用:0次
2018-09-10更新
|
161次组卷
|
3卷引用:【浙江新东方】62



