名校
解题方法
1 . 某小组研究不同pH下用NaClO氧化废水中的氨氮(用硝酸铵模拟),使其转化为无污染的气体,设计试剂用量如下表。已知HClO的氧化性比ClO-的氧化性更强,以下说法错误的是
| pH | 0.100mol·L-1 NH4NO3溶液/(mL) | 0.100mol·L-1 NaClO溶液/(mL) | 0.200mol·L-1 硫酸/(mL) | 蒸馏水 /(mL) | 氨氮去除率 /(%) |
| 1.0 | 10.00 | 10.00 | 10.00 | 10.00 | 89 |
| 2.0 | 10.00 | 10.00 | V1 | V2 | 75 |
| 6.0 | …… | …… | …… | …… | 85 |
| A.V1=2.00 |
B.pH=1反应的离子方程式:3ClO-+2NH =3Cl-+N2↑+3H2O+2H+ =3Cl-+N2↑+3H2O+2H+ |
| C.pH从1升高到2,氨氮去除率降低的原因是更多的HClO转化为ClO- |
| D.将氨氮废水的pH控制在6再进行处理更容易达到排放标准 |
您最近一年使用:0次
名校
2 . 利用下列装置进行实验,能达到实验目的的是


A.用甲制备并收集纯净的 |
| B.用乙比较碳元素与硫元素的非金属性强弱 |
| C.用丙提取溴水中的溴单质 |
D.用丁蒸发 溶液制备 溶液制备 |
您最近一年使用:0次
名校
3 . 下列制取NH3、验证其溶解性、收集并验证氨水挥发性的装置和原理能达到目的的是
A.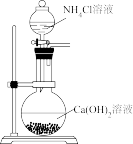 | B. | C. | D. |
您最近一年使用:0次
4 . 关于下列实验,实验现象或结论错误的是
| 实验 | 实验现象或结论 | |
| A | 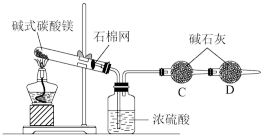 | 可以准确测量碱式碳酸镁分解生成的水和二氧化碳的量 |
| B | 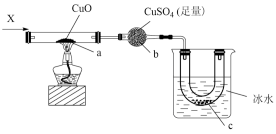 | 若a、b中均有颜色变化,则X只能为单质气体 |
| C | 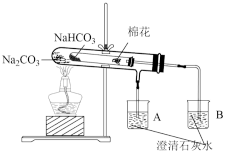 | 比较碳酸钠和碳酸氢钠的稳定性 |
| D | 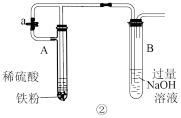 | 该装置利用正压制备氢氧化亚铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 某学习小组用如图所示装置测定生铁中铁的质量分数。
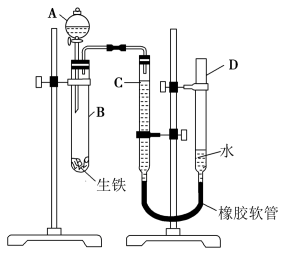
(1)仪器A的名称为__ 。
(2)试管B中发生反应的离子方程式为__ 。
(3)检查装置气密性,将药品(稀硫酸和生铁)和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂。
上述操作的顺序是__ (填标号);记录C的液面位置时,除视线平视外,还应__ 。
(4)若实验所用生铁的质量为ag,测得氢气体积为bmL(已换算为标准状况),则生铁中铁元素的质量分数为__ 。
(5)若将试管B中溶液倒入烧杯,再加入足量的氢氧化钠溶液,可观察到的现象为__ ,用化学方程式解释其原因:__ 。

(1)仪器A的名称为
(2)试管B中发生反应的离子方程式为
(3)检查装置气密性,将药品(稀硫酸和生铁)和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂。
上述操作的顺序是
(4)若实验所用生铁的质量为ag,测得氢气体积为bmL(已换算为标准状况),则生铁中铁元素的质量分数为
(5)若将试管B中溶液倒入烧杯,再加入足量的氢氧化钠溶液,可观察到的现象为
您最近一年使用:0次
6 . 铁粉与硝酸反应可制备硝酸铁,硝酸铁溶液可用于刻蚀银器。铁粉用量和硝酸浓度都会影响反应产物。
I.常温下过量铁粉与不同浓度硝酸反应的还原产物的探究。利用如图装置进行实验,其中装置A为氮气氛围。

(1)实验一:硝酸初始浓度为12.0mol•L-1时,硝酸的还原产物主要是NO2。装置B中NO2发生反应的化学方程式为___ 。
(2)实验二:硝酸浓度为6.0mol•L-1时,硝酸的还原产物主要是NO。利用上述装置进行实验时,证明还原产物主要是NO的现象是___ 。
(3)实验三:硝酸浓度为0.5mol•L-1时,过量铁粉与硝酸反应产生H2,充分反应后所得溶液几乎无色。取装置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝。过量铁粉与0.5mol•L-1硝酸混合发生反应的离子方程式有:①Fe+2H+=Fe2++H2↑;②___ 。
II.硝酸铁溶液刻蚀银器的原理探究。
(4)已知:①0.1mol•L-1硝酸铁溶液pH的为1.6。
②将5mL0.1mol•L-1硝酸铁溶液滴加到有银镜的试管中,1min银镜完全溶解。
提出猜想猜想a:Fe3+具有氧化性,能氧化Ag。
猜想b:酸性条件下NO ,能氧化Ag。
,能氧化Ag。
设计实验,验证猜想
实验结论:硝酸铁溶液刻蚀银器原理是0.1mol•L-1硝酸铁溶液中的Fe3+和NO 均能氧化Ag。
均能氧化Ag。
I.常温下过量铁粉与不同浓度硝酸反应的还原产物的探究。利用如图装置进行实验,其中装置A为氮气氛围。

(1)实验一:硝酸初始浓度为12.0mol•L-1时,硝酸的还原产物主要是NO2。装置B中NO2发生反应的化学方程式为
(2)实验二:硝酸浓度为6.0mol•L-1时,硝酸的还原产物主要是NO。利用上述装置进行实验时,证明还原产物主要是NO的现象是
(3)实验三:硝酸浓度为0.5mol•L-1时,过量铁粉与硝酸反应产生H2,充分反应后所得溶液几乎无色。取装置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝。过量铁粉与0.5mol•L-1硝酸混合发生反应的离子方程式有:①Fe+2H+=Fe2++H2↑;②
II.硝酸铁溶液刻蚀银器的原理探究。
(4)已知:①0.1mol•L-1硝酸铁溶液pH的为1.6。
②将5mL0.1mol•L-1硝酸铁溶液滴加到有银镜的试管中,1min银镜完全溶解。
提出猜想猜想a:Fe3+具有氧化性,能氧化Ag。
猜想b:酸性条件下NO
 ,能氧化Ag。
,能氧化Ag。设计实验,验证猜想
| 序号 | 实验方案 | 实验现象 | 结论 |
| 猜想a | ①将5mLpH约为1.6的0.05mol•L-1 ②将5mLpH约为1.6的硫酸溶液滴加到有银镜的试管乙中 | 猜想a成立 | |
| 猜想b | 将5mL | 1.2min试管丙中银镜完全溶解 | 猜想b成立 |
 均能氧化Ag。
均能氧化Ag。
您最近一年使用:0次
7 . 下列选用的相关装置符合实验要求的是
| A | B | C | D |
 |  |  |  |
| 高温煅烧石灰石 | 存放新制氯水 | 用电解法精炼Mg | 除去SO2中的HCl杂质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列实验操作或装置中,能达到相应实验目的的是
| 实验方案 |  |  |  |  |
| 目的 | A.制备乙酸乙酯的装置 | B.除去乙烯中的二氧化硫 | C.配制0.10mol/LNaOH溶液 | D.吸收CO2中的HCl杂质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 下列操作能达到相应实验目的的是
| 实验目的 | 操作 | |
| A | 检验溶液中的 | 用洁净的玻璃棒蘸取溶液,在酒精灯外焰上灼烧,观察颜色 |
| B | 溶液中的 | 取少量溶液,滴加足量氨水,观察现象 |
| C | 测定“84”消毒液的 | 用洁净的玻璃棒取少量“84”消毒液滴在 试纸上,与标准比色卡对比读数 试纸上,与标准比色卡对比读数 |
| D | 溶液中的 | 取少量溶液,加入 浓溶液并加热,用湿润的蓝色石蕊试纸放在试管口检验生成的气体 浓溶液并加热,用湿润的蓝色石蕊试纸放在试管口检验生成的气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-12-03更新
|
310次组卷
|
3卷引用:天津市第一中学2021-2022学年高三上学期第二次月考化学试题
名校
10 . 下列装置或操作能达到实验目的的是


| A.用图1所示装置用于实验室制取Cl2时除去Cl2中含有的少量HCl |
| B.用图2所示装置用于提纯混有少量KNO3的KCl固体的实验方案中的某一步操作 |
| C.用图3所示装置用于简便快速制取的CO2气体 |
| D.用图4所示装置用于实验室制取氯气 |
您最近一年使用:0次
2021-12-03更新
|
211次组卷
|
2卷引用:江苏省响水中学2021-2022学年高一上学期期中考试化学试题



