名校
1 . 下列实验装置,相关使用正确的是

| A.利用装置①进行蒸发结晶操作时,将水全部蒸干后停止加热 |
| B.装置②可以用于从海水中获得蒸馏水 |
| C.装置③可以用作实验室制备氧气的发生装置 |
| D.利用装置④进行反应:Na2CO3+ 2HCl = 2NaCl+ H2O+CO2↑ |
您最近一年使用:0次
23-24高三上·北京·阶段练习
2 . 某研究小组查阅资料发现 与
与 的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在
的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在 ,并据此设计实验1(如右图所示),实验中
,并据此设计实验1(如右图所示),实验中 约为2,实验结果溶液未变红。
约为2,实验结果溶液未变红。
【资料】 为不溶于水的白色固体。
为不溶于水的白色固体。___________ 。
(2)分析产生试管a中实验现象的原因,提出如下假设:
i.可能是 氧化了
氧化了 ;
;
ii.可能是___________ 或___________ 氧化了 。
。
iii.体系中可能产生了较多的 (从平衡移动原理的角度分析其产生原因:
(从平衡移动原理的角度分析其产生原因:___________ ),是 氧化了
氧化了 。
。
(3)设计、实施实验3、4,实验记录如下表。
①试剂a是___________ 。
②依据实验3,结论是:___________ 。
(4)试管b中,加入 溶液后所产生实验现象的原因是
溶液后所产生实验现象的原因是___________ 。
(5)实验1中溶液未变红的原因是___________ 。
 与
与 的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在
的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在 ,并据此设计实验1(如右图所示),实验中
,并据此设计实验1(如右图所示),实验中 约为2,实验结果溶液未变红。
约为2,实验结果溶液未变红。
【资料】
 为不溶于水的白色固体。
为不溶于水的白色固体。实验2:
(2)分析产生试管a中实验现象的原因,提出如下假设:
i.可能是
 氧化了
氧化了 ;
;ii.可能是
 。
。iii.体系中可能产生了较多的
 (从平衡移动原理的角度分析其产生原因:
(从平衡移动原理的角度分析其产生原因: 氧化了
氧化了 。
。(3)设计、实施实验3、4,实验记录如下表。
| 编号 | 实验操作 | 实验现象 |
| 3 | 在试管中加入1滴 溶液, 溶液, 蒸馏水,1滴试剂a,一段时间后加入1滴 蒸馏水,1滴试剂a,一段时间后加入1滴 溶液 溶液 | 溶液不变红 |
| 4 | 在试管中加入1滴 溶液, 溶液, 蒸馏水,1滴 蒸馏水,1滴 溶液和1滴 溶液和1滴 ,一段时间后加入1滴 ,一段时间后加入1滴 溶液 溶液 | 溶液不变红 |
②依据实验3,结论是:
(4)试管b中,加入
 溶液后所产生实验现象的原因是
溶液后所产生实验现象的原因是(5)实验1中溶液未变红的原因是
您最近一年使用:0次
名校
3 . I.某研究性学习小组向一定量的 溶液(加入少量淀粉)中加入稍过量的
溶液(加入少量淀粉)中加入稍过量的 溶液,一段时间后,溶液突然变蓝。为进一步研究有关因素对反应速率的影响,探究如下:
溶液,一段时间后,溶液突然变蓝。为进一步研究有关因素对反应速率的影响,探究如下:
(1)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响记录如表:
实验①②是探究_______ 对反应速率的影响,表中
_______ ,
_______  (填“>”、“=”或“<”);实验②③是探究温度对反应速率的影响,表中
(填“>”、“=”或“<”);实验②③是探究温度对反应速率的影响,表中
_______ 。
II.现对某一葡萄酒进行二氧化硫含量检测,取300.00mL葡萄酒,通过适当的方法使所含 全部逸出并用
全部逸出并用 将其全部氧化
将其全部氧化 ,然后用
,然后用 标准溶液进行滴定。
标准溶液进行滴定。
(2)写出上述氧化还原反应的化学方程式:___________ 。
(3)滴定终点读数时俯视刻度线,则测量结果比实际值___________ (填“偏高”“偏低”或“无影响”)。
(4)该滴定若用酚酞作指示剂,滴定终点的判断方法为:当滴入最后半滴标准液时,_______ 。
(5)我国规定葡萄酒中 最大含量为
最大含量为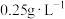 。根据以下检测数据,该葡萄酒是否达标
。根据以下检测数据,该葡萄酒是否达标___________ 。(填“是”或者“否”)
 溶液(加入少量淀粉)中加入稍过量的
溶液(加入少量淀粉)中加入稍过量的 溶液,一段时间后,溶液突然变蓝。为进一步研究有关因素对反应速率的影响,探究如下:
溶液,一段时间后,溶液突然变蓝。为进一步研究有关因素对反应速率的影响,探究如下:(1)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响记录如表:
| 编号 |   溶液 溶液 |  溶液 溶液 | 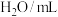 | 反应温度 | 液变蓝所用时间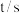 |
| ① | 4.0 | 14.0 | b | 15 |  |
| ② | 6.0 | 14.0 | 0 | 15 |  |
| ③ | 6.0 | a | 0 | 25 |  |


 (填“>”、“=”或“<”);实验②③是探究温度对反应速率的影响,表中
(填“>”、“=”或“<”);实验②③是探究温度对反应速率的影响,表中
II.现对某一葡萄酒进行二氧化硫含量检测,取300.00mL葡萄酒,通过适当的方法使所含
 全部逸出并用
全部逸出并用 将其全部氧化
将其全部氧化 ,然后用
,然后用 标准溶液进行滴定。
标准溶液进行滴定。(2)写出上述氧化还原反应的化学方程式:
(3)滴定终点读数时俯视刻度线,则测量结果比实际值
(4)该滴定若用酚酞作指示剂,滴定终点的判断方法为:当滴入最后半滴标准液时,
(5)我国规定葡萄酒中
 最大含量为
最大含量为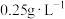 。根据以下检测数据,该葡萄酒是否达标
。根据以下检测数据,该葡萄酒是否达标| 实验编号 |  溶液的浓度 溶液的浓度 | 滴定完成时, 溶液滴入的体积 溶液滴入的体积 | 待测溶液的体积 |
| 1 | 0.0900 | 22.12 | 20.00 |
| 2 | 0.0900 | 22.08 | 20.00 |
| 3 | 0.0900 | 22.80 | 20.00 |
您最近一年使用:0次
名校
解题方法
4 . 下列设计的实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究化学反应的限度 | 取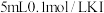 溶液,滴加 溶液,滴加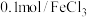 溶液 溶液 滴,充分反应,可根据溶液中既含 滴,充分反应,可根据溶液中既含 又含 又含 的实验事实判断该反应是可逆反应 的实验事实判断该反应是可逆反应 |
| B | 比较Mg与Al的金属活动性 | 常温下,将Mg、Al与NaOH溶液组成原电池 |
| C | 探究不同催化剂对同一反应速率的影响 | 相同条件下,向两支盛有等体积等浓度 溶液的试管中分别加入少量 溶液的试管中分别加入少量 粉末和5滴 粉末和5滴 的 的 溶液 溶液 |
| D | 证明在相同温度下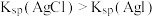 | 向盛有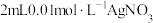 溶液的试管中滴加2滴 溶液的试管中滴加2滴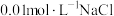 溶液,有白色沉淀生成,再向其中滴加2滴 溶液,有白色沉淀生成,再向其中滴加2滴 溶液,产生黄色沉淀 溶液,产生黄色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列实验操作和现象,得出的相应结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有 和 和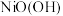 的试管中分别滴加相同浓度的浓盐酸 的试管中分别滴加相同浓度的浓盐酸 | 只有盛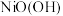 的试管中产生黄绿色气体 的试管中产生黄绿色气体 | 氧化性: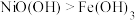 |
| B | 取   溶液于试管中,加入 溶液于试管中,加入   溶液,充分反应后滴入5滴15% 溶液,充分反应后滴入5滴15% 溶液 溶液 | 溶液变为血红色 |  与 与 的反应有一定限度 的反应有一定限度 |
| C | 乙醇和浓硫酸共热至170℃,将产生的气体通入溴水中 | 溴水褪色 | 乙烯发生了加成反应 |
| D | 向 溶液中滴加 溶液中滴加 溶液 溶液 | 出现黄色沉淀 |  发生了水解反应 发生了水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
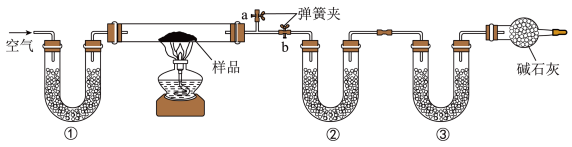
6 . 为了测定NaCl、 和
和 的混合物中各组分的含量,某同学设计如图实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法正确的是
的混合物中各组分的含量,某同学设计如图实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法正确的是
 和
和 的混合物中各组分的含量,某同学设计如图实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法正确的是
的混合物中各组分的含量,某同学设计如图实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法正确的是
| A.实验过程中先停止通入空气,再停止加热 |
| B.若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏大 |
C.②可以用浓 替代 替代 |
| D.硬质玻璃管加热前,应关闭b,打开a,通入空气,直至a处出来的空气不再使澄清石灰水变浑浊为止 |
您最近一年使用:0次
7 . 离子反应和氧化还原反应是高中阶段两种重要的化学反应类型,在工业生产、环保及科研领域中广泛涉及。回答下列问题:
I.亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。将 通入到
通入到 和
和 的混合溶液中可得到亚氯酸钠(NaClO2)溶液,经减压
的混合溶液中可得到亚氯酸钠(NaClO2)溶液,经减压 蒸发溶剂得到
蒸发溶剂得到 晶体。
晶体。
(1)写出上述生成 的化学方程式:
的化学方程式:___________
(2)上述反应中 作
作___________ (填“氧化剂”或“还原剂”), 属于二元弱酸,写出
属于二元弱酸,写出 的第一步电离方程式:
的第一步电离方程式:___________ 。
(3)减压 蒸发而不直接常压蒸发的原因为
蒸发而不直接常压蒸发的原因为___________ 。
II.硫代硫酸钠(Na2S2O3)俗称大苏打,易溶于水,溶于水后呈碱性,遇酸不稳定, 与硫酸的反应常用于定性分析影响化学反应速率的因素;
与硫酸的反应常用于定性分析影响化学反应速率的因素; 在“碘量法”氧化还原滴定中常作标准试剂,用于定量测量碘的含量。
在“碘量法”氧化还原滴定中常作标准试剂,用于定量测量碘的含量。
(4)写出 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:___________ 。
(5)利用“碘量法”测定芒硝( ,含
,含 杂质)中
杂质)中 的质量分数。称取
的质量分数。称取 样品,置于碘量瓶中,移取
样品,置于碘量瓶中,移取 溶液(含
溶液(含 )置于其中,并加入乙酸溶液,密闭并置于暗处充分反应
)置于其中,并加入乙酸溶液,密闭并置于暗处充分反应 ,有单质硫析出,以淀粉为指示剂,过量的
,有单质硫析出,以淀粉为指示剂,过量的 用
用 溶液滴定,测定消耗
溶液滴定,测定消耗 溶液的体积为VmL。已知:
溶液的体积为VmL。已知: 。
。
①“密闭并置于暗处充分反应 ”过程中采用密闭的目的是
”过程中采用密闭的目的是___________ 。
②滴定终点的现象为___________ 。
③样品中 的质量分数为
的质量分数为___________ (写出表达式)。
I.亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。将
 通入到
通入到 和
和 的混合溶液中可得到亚氯酸钠(NaClO2)溶液,经减压
的混合溶液中可得到亚氯酸钠(NaClO2)溶液,经减压 蒸发溶剂得到
蒸发溶剂得到 晶体。
晶体。(1)写出上述生成
 的化学方程式:
的化学方程式:(2)上述反应中
 作
作 属于二元弱酸,写出
属于二元弱酸,写出 的第一步电离方程式:
的第一步电离方程式:(3)减压
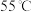 蒸发而不直接常压蒸发的原因为
蒸发而不直接常压蒸发的原因为II.硫代硫酸钠(Na2S2O3)俗称大苏打,易溶于水,溶于水后呈碱性,遇酸不稳定,
 与硫酸的反应常用于定性分析影响化学反应速率的因素;
与硫酸的反应常用于定性分析影响化学反应速率的因素; 在“碘量法”氧化还原滴定中常作标准试剂,用于定量测量碘的含量。
在“碘量法”氧化还原滴定中常作标准试剂,用于定量测量碘的含量。(4)写出
 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:(5)利用“碘量法”测定芒硝(
 ,含
,含 杂质)中
杂质)中 的质量分数。称取
的质量分数。称取 样品,置于碘量瓶中,移取
样品,置于碘量瓶中,移取 溶液(含
溶液(含 )置于其中,并加入乙酸溶液,密闭并置于暗处充分反应
)置于其中,并加入乙酸溶液,密闭并置于暗处充分反应 ,有单质硫析出,以淀粉为指示剂,过量的
,有单质硫析出,以淀粉为指示剂,过量的 用
用 溶液滴定,测定消耗
溶液滴定,测定消耗 溶液的体积为VmL。已知:
溶液的体积为VmL。已知: 。
。①“密闭并置于暗处充分反应
 ”过程中采用密闭的目的是
”过程中采用密闭的目的是②滴定终点的现象为
③样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2023-10-30更新
|
465次组卷
|
2卷引用:河南省名校青桐鸣大联考2024届高三上学期10月联考化学试题
解题方法
8 . 检验甲醛含量的方法有很多,其中银-Ferrozine法灵敏度较高。测定原理为甲醛与银氨溶液反应生成Ag,产生的Ag与Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪(Ferrozine)形成有色配合物,通过测定吸光度计算出甲醛的含量。某学习小组类比此原理设计如图装置,测定新装修居室内空气中甲醛的含量(夹持装置略去)。根据国家GB/T18883-2002《室内空气质量标准》,室内甲醛的达标标准为:在密闭门窗时间不少于12小时以后,测得甲醛含量不超过0.1mg/m³。

已知:①B装置中间导管所连接的尾气处理装置在上图中已省略;
②毛细管内径不超过1mm。
回答下列问题:
(1)下列哪些制备气体的装置与A装置不同___________ 。
a.Cu和浓硫酸制SO2 b.CaCO3和稀盐酸制CO2 c.实验室制乙炔
用饱和食盐水代替水制备NH3的原因是___________ 。
(2)银氨溶液的制备。
关闭K1、K2,打开K3.先打开分液漏斗上方的玻璃塞,再打开分液漏斗的___________ ,使饱和食盐水慢慢滴入圆底烧瓶中,将产生的气体通入已加入适量硝酸银溶液的B中,当观察到B中___________ ,停止通入NH3。
(3)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K1,将滑动隔板慢慢由最右端抽到最左端,吸入1L室内空气(在密闭门窗时间超过12小时以后),关闭K1;打开K2,向右缓慢推动滑动隔板,将气体全部排出,再关闭___________ (填“K1”、“K2”或“K3”);重复上述操作4次。上述过程,空气中甲醛与B中银氨溶液反应的化学方程式为___________ 。对比普通玻璃导管,使用毛细管的优点是___________ 。
②待装置B中溶液充分反应后,向其中加入适量稀硫酸调节溶液pH=1,再加入足量Fe2(SO4)3溶液,充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562nm处测定吸光度,测得生成1.12mg Fe2+,则该室内空气中甲醛的含量为___________ mg·L-1。通过计算可知该新居室内甲醛含量___________ (填“达标”或“不达标”)。

已知:①B装置中间导管所连接的尾气处理装置在上图中已省略;
②毛细管内径不超过1mm。
回答下列问题:
(1)下列哪些制备气体的装置与A装置不同
a.Cu和浓硫酸制SO2 b.CaCO3和稀盐酸制CO2 c.实验室制乙炔
用饱和食盐水代替水制备NH3的原因是
(2)银氨溶液的制备。
关闭K1、K2,打开K3.先打开分液漏斗上方的玻璃塞,再打开分液漏斗的
(3)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K1,将滑动隔板慢慢由最右端抽到最左端,吸入1L室内空气(在密闭门窗时间超过12小时以后),关闭K1;打开K2,向右缓慢推动滑动隔板,将气体全部排出,再关闭
②待装置B中溶液充分反应后,向其中加入适量稀硫酸调节溶液pH=1,再加入足量Fe2(SO4)3溶液,充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562nm处测定吸光度,测得生成1.12mg Fe2+,则该室内空气中甲醛的含量为
您最近一年使用:0次
9 . 探究Na2S2O3 + H2SO4 = Na2SO4 + SO2↑ + S↓ + H2O化学反应速率的影响因素,设计了以下实验,下列说法正确的是
| 锥形瓶 | 0.1 mol/LNa2S2O3溶液的体积/mL | 0.1 mol/LH2SO4溶液的体积/mL | 蒸馏水的体积/mL | 反应温度 | 浑浊出现时间/s | 备注 |
| 1 | 10 | 10 | 0 | 20 ℃ | 10 | |
| 2 | 10 | 5 | V1 | 20℃ | 16 | |
| 3 | 10 | 10 | V2 | 50℃ | 5 | 10秒后浑浊不再增多 |
| 4 | 10 | 4 | V3 | 50 ℃ | 8 |
| A.V1=5, V2=0, V3=6 |
| B.10秒内,3号瓶中Na2S2O3的平均反应速率为0.01mol/(L·s) |
| C.该反应也可通过比较相同时间内生成SO2体积的多少来判断化学反应的快慢 |
| D.由2号瓶和3号瓶的实验结果可推知温度越高反应速率越快 |
您最近一年使用:0次
名校
10 . 利用下列装置进行实验,能达到实验目的的是


A.用甲制备并收集纯净的 |
| B.用乙比较碳元素与硫元素的非金属性强弱 |
| C.用丙提取溴水中的溴单质 |
D.用丁蒸发 溶液制备 溶液制备 |
您最近一年使用:0次



