1 . 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净 的氯气。进行此实验,所用仪器如下图:

(1)连接上述仪器的正确顺序是(填各接口处的字母):E接_______ ,_______ 接_______ ,_______ 接_______ ,_______ 接F。
(2)产生氯气的离子方程式为:_______ ,氧化剂与还原剂之比为_______ 。
(3)在装置中:饱和食盐水起的作用是_______ 。
(4)将所制得氯气配成新制氯水,其中含有多种成分,因而具有多种性质。根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
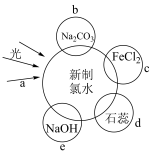
①久置的氯水变质,原因是_______ 。(用化学反应方程式表示)
②c过程中溶液变为黄色,反应的离子方程式是_______ 。
③d的现象为_______ 。
④世界环保联盟建议采用具有强氧化性的广谱高效消毒剂二氧化氯(ClO2),我国广泛采用经干燥空气稀释的氯气通入填有固体氯酸钠(NaClO3)的柱内制得ClO2和另一种有漂白性的物质。这一反应中生成1mol ClO2是转移的电子数是_______ 。

(1)连接上述仪器的正确顺序是(填各接口处的字母):E接
(2)产生氯气的离子方程式为:
(3)在装置中:饱和食盐水起的作用是
(4)将所制得氯气配成新制氯水,其中含有多种成分,因而具有多种性质。根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。

①久置的氯水变质,原因是
②c过程中溶液变为黄色,反应的离子方程式是
③d的现象为
④世界环保联盟建议采用具有强氧化性的广谱高效消毒剂二氧化氯(ClO2),我国广泛采用经干燥空气稀释的氯气通入填有固体氯酸钠(NaClO3)的柱内制得ClO2和另一种有漂白性的物质。这一反应中生成1mol ClO2是转移的电子数是
您最近一年使用:0次
名校
解题方法
2 . 化学学习小组进行如下实验。
I.【探究反应速率的影响因素】设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 H2C2O4 溶液、0.010
H2C2O4 溶液、0.010
 溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
(1)上述实验①、②是探究____________ 对化学反应速率的影响;
(2)若上述实验②、③是探究浓度对化学反应速率的影响,则a为____________ ;
(3)乙是实验需要测量的物理量,则表格中“乙”应填写__________________ 。
II.【测定 中 x值】已知:
中 x值】已知:
① 称取 1.260g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液;
②取 25.00mL 待测液放入锥形瓶中,再加入适的稀 ;
;
③用浓度为 0.05 000 的
的  标准溶液进行滴定。
标准溶液进行滴定。
(4)某学生的滴定方式(夹持部分略去)如下,最合理的是___________ (选填 a、b)。

(5)滴定终点的现象为_________________
(6)通过上述数据,求得x=_______________ 。以标准 溶液滴定样品溶液的浓度,未用标准
溶液滴定样品溶液的浓度,未用标准 溶液润洗滴定管,引起实验结果
溶液润洗滴定管,引起实验结果_______________ (偏大、偏小或没有影响)。
I.【探究反应速率的影响因素】设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20
 H2C2O4 溶液、0.010
H2C2O4 溶液、0.010
 溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽物理量 |
|
|  (0.010 (0.010  溶液)/mL 溶液)/mL | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 50 | |
② | 2.0 | 0 | 4.0 | 25 | |
③ | 1.0 | a | 4.0 | 25 |
(2)若上述实验②、③是探究浓度对化学反应速率的影响,则a为
(3)乙是实验需要测量的物理量,则表格中“乙”应填写
II.【测定
 中 x值】已知:
中 x值】已知:
① 称取 1.260g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液;
②取 25.00mL 待测液放入锥形瓶中,再加入适的稀
 ;
;③用浓度为 0.05 000
 的
的  标准溶液进行滴定。
标准溶液进行滴定。(4)某学生的滴定方式(夹持部分略去)如下,最合理的是

(5)滴定终点的现象为
(6)通过上述数据,求得x=
 溶液滴定样品溶液的浓度,未用标准
溶液滴定样品溶液的浓度,未用标准 溶液润洗滴定管,引起实验结果
溶液润洗滴定管,引起实验结果
您最近一年使用:0次
2023-02-22更新
|
142次组卷
|
2卷引用:广西桂林市第十八中学2022-2023学年高二上学期期中考试化学试题
22-23高一上·浙江·阶段练习
解题方法
3 . 根据维生素C能够使淀粉碘溶液褪色的原理,应用如图实验可以测定果汁中维生素C含量的多少,要得出正确结论,实验过程中不需要进行控制的条件是
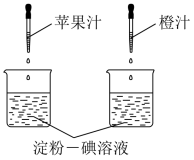

| A.烧杯中溶液的体积 |
| B.两个胶头滴管滴出的每滴果汁的体积 |
| C.烧杯中淀粉-碘溶液的浓度 |
| D.胶头滴管滴出的果汁的滴数 |
您最近一年使用:0次
名校
4 . 小组同学探究盐溶液对反应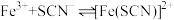 (血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
(血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
已知:ⅰ.溶液血红色越深,透光率越小,其它颜色对透光率的影响可忽略。
ⅱ. (黄色)
(黄色)
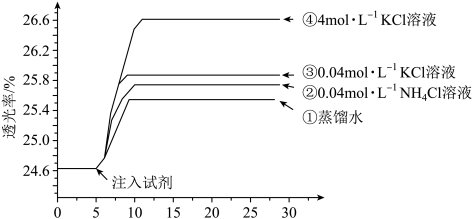
下列说法不正确的是
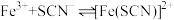 (血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
(血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。已知:ⅰ.溶液血红色越深,透光率越小,其它颜色对透光率的影响可忽略。
ⅱ.
 (黄色)
(黄色)
下列说法不正确的是
A.注入试剂①后溶液透光率增大,一定是由于 平衡逆向移动引起的 平衡逆向移动引起的 |
| B.透光率③比②高,可能是阳离子种类或溶液pH导致的 |
C.透光率④比③高,可能发生了反应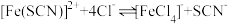 |
D.若要证明试剂③中Cl—对平衡体系有影响,还应使用与试剂③等体积的0.04mol/L的KNO3溶液进行对比实验(已知NO 对实验无影响) 对实验无影响) |
您最近一年使用:0次
2023-01-13更新
|
653次组卷
|
9卷引用:北京市海淀区2021-2022学年高三上学期期末考试化学试题
名校
解题方法
5 . 下列实验及其结论都正确的是
| 实验 | 结论 | |
| A | 分别向 的酸性 的酸性 和 和 的酸性 的酸性 溶液中滴加 溶液中滴加 的草酸溶液 的草酸溶液 ,用秒表记录褪色时间 ,用秒表记录褪色时间 | 反应物的浓度越大,反应速率越快 |
| B | 室温下,用 试纸测定浓度均为 试纸测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 | 比较 和 和 的酸性强弱 的酸性强弱 |
| C | 等体积、 的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 | 酸性HA比HB弱 |
| D | 向某钠盐中滴加浓盐酸,将产生的气体通入品红溶液 | 根据品红溶液褪色判断该钠盐为 或 或 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 化学是实验的科学,下列有关实验设计不能达到目的的是。
| A | B | C | D |
 |  | 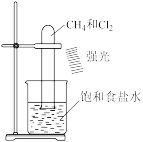 |  |
制备 胶体 胶体 | 配制溶液时移液 | 探究 与 与 的取代反应 的取代反应 | 进行喷泉实验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-16更新
|
868次组卷
|
4卷引用:湖南省九校联盟2023届高三上学期第一次联考化学试题
解题方法
7 . 三氯化六氨合钴(III){ }是制备其它三价钴配合物的重要试剂,实验室以含钴单质(杂质不溶于盐酸)为原料经三氯化钴制备[
}是制备其它三价钴配合物的重要试剂,实验室以含钴单质(杂质不溶于盐酸)为原料经三氯化钴制备[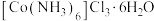 ]晶体。已知:
]晶体。已知:
① 不易被氧化,
不易被氧化, 具有强氧化性;
具有强氧化性; 具有较强还原性,
具有较强还原性, 性质稳定。
性质稳定。
②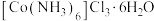 在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。
在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。
(1)溶解。将钴单质溶于稀盐酸,过滤除去杂质,得到 溶液。写出该反应的化学方程式
溶液。写出该反应的化学方程式_______ 。
(2)混合。向 溶液中加入少量
溶液中加入少量 溶液,加入活性炭作催化剂。加入的
溶液,加入活性炭作催化剂。加入的 溶液有利于后续
溶液有利于后续 与
与 的配合反应。在制备
的配合反应。在制备 时,不采用先氧化
时,不采用先氧化 的原因是
的原因是_____ 。
(3)配合、氧化。如图装置,先向三颈烧瓶滴加过量氨水、 中的一种,充分反应,再向混合溶液中滴加另一种溶液,加热,充分搅拌,生成的
中的一种,充分反应,再向混合溶液中滴加另一种溶液,加热,充分搅拌,生成的 吸附在活性炭上。
吸附在活性炭上。
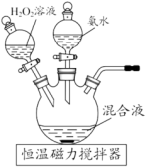
①另一种溶液是_______ 。
②控制三颈烧瓶中溶液温度为60℃的原因是_______ 。
③加入 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_______ 。
(4)已知:稀盐酸可将吸附在活性炭上的 溶解。实验中须使用的试剂:稀盐酸、浓盐酸、无水乙醇。制备
溶解。实验中须使用的试剂:稀盐酸、浓盐酸、无水乙醇。制备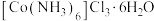 请补充完整实验方案:将三颈烧瓶中所得混合物充分搅拌、过滤,
请补充完整实验方案:将三颈烧瓶中所得混合物充分搅拌、过滤,_______ 低温干燥。
 }是制备其它三价钴配合物的重要试剂,实验室以含钴单质(杂质不溶于盐酸)为原料经三氯化钴制备[
}是制备其它三价钴配合物的重要试剂,实验室以含钴单质(杂质不溶于盐酸)为原料经三氯化钴制备[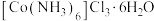 ]晶体。已知:
]晶体。已知:①
 不易被氧化,
不易被氧化, 具有强氧化性;
具有强氧化性; 具有较强还原性,
具有较强还原性, 性质稳定。
性质稳定。②
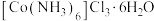 在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。
在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。(1)溶解。将钴单质溶于稀盐酸,过滤除去杂质,得到
 溶液。写出该反应的化学方程式
溶液。写出该反应的化学方程式(2)混合。向
 溶液中加入少量
溶液中加入少量 溶液,加入活性炭作催化剂。加入的
溶液,加入活性炭作催化剂。加入的 溶液有利于后续
溶液有利于后续 与
与 的配合反应。在制备
的配合反应。在制备 时,不采用先氧化
时,不采用先氧化 的原因是
的原因是(3)配合、氧化。如图装置,先向三颈烧瓶滴加过量氨水、
 中的一种,充分反应,再向混合溶液中滴加另一种溶液,加热,充分搅拌,生成的
中的一种,充分反应,再向混合溶液中滴加另一种溶液,加热,充分搅拌,生成的 吸附在活性炭上。
吸附在活性炭上。
①另一种溶液是
②控制三颈烧瓶中溶液温度为60℃的原因是
③加入
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(4)已知:稀盐酸可将吸附在活性炭上的
 溶解。实验中须使用的试剂:稀盐酸、浓盐酸、无水乙醇。制备
溶解。实验中须使用的试剂:稀盐酸、浓盐酸、无水乙醇。制备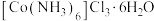 请补充完整实验方案:将三颈烧瓶中所得混合物充分搅拌、过滤,
请补充完整实验方案:将三颈烧瓶中所得混合物充分搅拌、过滤,
您最近一年使用:0次
名校
解题方法
8 . 下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 结论 |
A | 溶液X的焰色反应呈黄色 | X中含钠盐 |
B | 向固体Y中加入稀盐酸,生成使澄清石灰水变浑浊的气体 | Y是碳酸盐 或亚硫酸盐 |
C | 向溶液Z中 | Z一定含有 |
D | 向固体W中加入浓 | W一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18g/cm3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用如图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴水(表面覆盖少量水)。
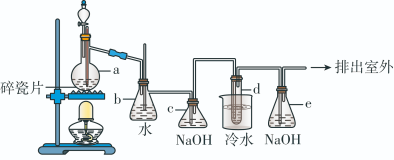
(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速升高到170℃,否则容易发生副反应。请写出乙醇发生消去反应的方程式_______ 。
(2)写出制备1,2-二溴乙烷的化学方程式:_______ 。
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请回答发生堵塞时瓶b中的现象:_______ 。
(4)容器c中NaOH溶液的作用是:_______ ,e中NaOH的作用是_______
(5)d处烧杯中用冷水浴的目的_______
(6)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因_______ 。

(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速升高到170℃,否则容易发生副反应。请写出乙醇发生消去反应的方程式
(2)写出制备1,2-二溴乙烷的化学方程式:
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请回答发生堵塞时瓶b中的现象:
(4)容器c中NaOH溶液的作用是:
(5)d处烧杯中用冷水浴的目的
(6)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因
您最近一年使用:0次
2022-11-16更新
|
200次组卷
|
2卷引用:宁夏石嘴山市第三中学2022-2023学年高二上学期期中考试化学(理)试题
名校
解题方法
10 . 某实验小组以H2O2分解为例,探究化学反应速率的影响因素。
【实验Ⅰ】小组同学进行以下对比实验,并记录实验现象。

【实验Ⅱ】另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液,均未观察到有明显的气泡产生。
(1)实验Ⅰ的目的是_______ 。
(2)实验Ⅱ未观察到预期现象,为了达到该实验的目的,可采取的改进措施是_______ 。
【实验Ⅲ】为了探究Fe3+和Cu2+对H2O2分解的催化效果:在两支试管中各加入2mL5%的H2O2溶液,再向其中分别滴入1mL浓度均为0.1mol/L的FeCl3溶液和CuSO4溶液。
(3)有同学建议将CuSO4改为CuCl2溶液,理由是_______ ;还有同学认为即使改用了CuCl2溶液,仍不严谨,建议补做对比实验:向2mL5%的H2O2溶液中滴入的试剂及其用量是_______ 。
【探究Ⅳ】某同学查阅文献资料发现在含有少量I-的溶液中,H2O2分解的机理为:H2O2+I-=H2O+IO-(慢);H2O2+IO-=H2O+O2↑+I-(快)。
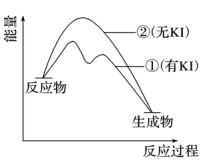
(4)下列有关该反应的说法错误的是 _______。
(5)已知 I2+2S2O = S4O
= S4O +2I-,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。( 假定Na2S2O3溶液足量)
+2I-,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。( 假定Na2S2O3溶液足量)
表中V1 =_______ mL,V2 =_______ mL,t1、t2、t3的大小关系是_______ 。
【实验Ⅰ】小组同学进行以下对比实验,并记录实验现象。

【实验Ⅱ】另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液,均未观察到有明显的气泡产生。
(1)实验Ⅰ的目的是
(2)实验Ⅱ未观察到预期现象,为了达到该实验的目的,可采取的改进措施是
【实验Ⅲ】为了探究Fe3+和Cu2+对H2O2分解的催化效果:在两支试管中各加入2mL5%的H2O2溶液,再向其中分别滴入1mL浓度均为0.1mol/L的FeCl3溶液和CuSO4溶液。
(3)有同学建议将CuSO4改为CuCl2溶液,理由是
【探究Ⅳ】某同学查阅文献资料发现在含有少量I-的溶液中,H2O2分解的机理为:H2O2+I-=H2O+IO-(慢);H2O2+IO-=H2O+O2↑+I-(快)。

(4)下列有关该反应的说法错误的是 _______。
| A.在该反应中,H2O2既做氧化剂,又做还原剂 |
| B.H2O2+I-=H2O+IO-是放热反应 |
| C.IO- 是该反应的催化剂 |
| D.反应速率与I-浓度有关 |
 = S4O
= S4O +2I-,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。( 假定Na2S2O3溶液足量)
+2I-,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。( 假定Na2S2O3溶液足量)| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | V1 | 4.0 | V2 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | 4.0 | t3 |
您最近一年使用:0次

 溶液)/mL
溶液)/mL 溶液,产生白色沉淀,再加入稀盐酸,沉淀不溶解
溶液,产生白色沉淀,再加入稀盐酸,沉淀不溶解
 溶液,产生的气体能使湿润的红色石蕊试纸变蓝
溶液,产生的气体能使湿润的红色石蕊试纸变蓝


