1 . 用离子交换法从海带中提取碘是一种较为先进的制碘工艺应用技术。
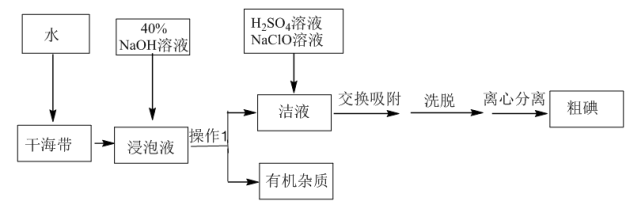
已知: 交换吸附原理:
交换吸附原理: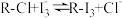 。试回答下列问题:
。试回答下列问题:
(1)操作Ⅰ的正确图示为_______。
(2)在清液中加入 和
和 溶液后,溶液最终变为棕红色,该步骤中
溶液后,溶液最终变为棕红色,该步骤中 的量要适中,请说明原因
的量要适中,请说明原因_______ 。
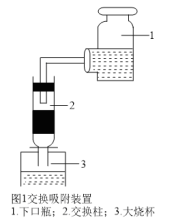
(3)其中交换吸附装置如图1所示,交换柱内装有氯型阴离子交换树脂( 表示),待溶液转化原理为:
表示),待溶液转化原理为: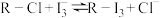 ,全部通过后,树脂颜色变为黑红色,再通过洗脱,离心分离后得到粗碘。已知洗脱分两步进行
,全部通过后,树脂颜色变为黑红色,再通过洗脱,离心分离后得到粗碘。已知洗脱分两步进行
第一步:取8~10%的 溶液
溶液 注入交换柱中。碱性洗脱原理为:
注入交换柱中。碱性洗脱原理为:
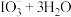 。往碱性洗脱液中滴加
。往碱性洗脱液中滴加 溶液,烧杯底部会析出一层泥状粗碘。
溶液,烧杯底部会析出一层泥状粗碘。
第二步:取10%的 溶液
溶液 注入上述交换柱中。氯化钠洗脱原理为:
注入上述交换柱中。氯化钠洗脱原理为: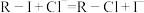 。再往氯化钠洗脱液中滴加
。再往氯化钠洗脱液中滴加 溶液使之酸化,再滴加
溶液使之酸化,再滴加 溶液,溶液由无色转变棕黑色浑浊。
溶液,溶液由无色转变棕黑色浑浊。
①根据交换吸附及洗脱过程可知强碱性阴离子交换树脂也可以对 进行交换吸附,那实验中将
进行交换吸附,那实验中将 转化成
转化成 的原因可能是
的原因可能是_______ 。
②往氯化钠洗脱液中滴加 溶液使之酸化,再滴加
溶液使之酸化,再滴加 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(4)置换碘量法是分析氧化性试剂的一种常用分析方法,基本过程如下:
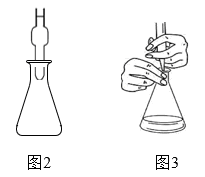
a.取3只碘量瓶,用移液管分别量取一定体积的供试品(氧化性物质)溶液于碘量瓶(图2)中
b.加入稍过量的碘化钾溶液,盖上盖子,并加纯水液封,静置或微热一段时间
c.打开瓶塞,按图3方式用标准 溶液进行滴定,重复3次
溶液进行滴定,重复3次
d.另取3只碘量瓶,用移液管分别量取一定体积准确浓度的基准液 溶液于其中
溶液于其中
e.计算标准液的浓度
f.空白实验
过程中涉及的反应过程如下:
供试品(氧化性物质)
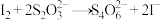

①上述操作合理的顺序是:_______ 。
 _______
_______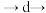 _______
_______ _______
_______ _______
_______ _______
_______ (部分步骤可以重复)
(部分步骤可以重复)
②碘量瓶加盖并加纯水液封的主要目的是_______ 。
③已知 易受空气和微生物作用而分解,若无上述操作中的d步骤及相关操作,则测定的供试品的含量会
易受空气和微生物作用而分解,若无上述操作中的d步骤及相关操作,则测定的供试品的含量会_______ 。(填“偏大”、“偏小”或“不变”)

已知:
 交换吸附原理:
交换吸附原理: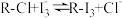 。试回答下列问题:
。试回答下列问题:(1)操作Ⅰ的正确图示为_______。
A.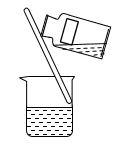 | B.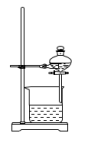 | C.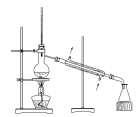 | D.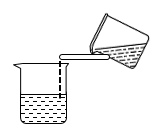 |
 和
和 溶液后,溶液最终变为棕红色,该步骤中
溶液后,溶液最终变为棕红色,该步骤中 的量要适中,请说明原因
的量要适中,请说明原因(3)其中交换吸附装置如图1所示,交换柱内装有氯型阴离子交换树脂(
 表示),待溶液转化原理为:
表示),待溶液转化原理为: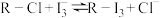 ,全部通过后,树脂颜色变为黑红色,再通过洗脱,离心分离后得到粗碘。已知洗脱分两步进行
,全部通过后,树脂颜色变为黑红色,再通过洗脱,离心分离后得到粗碘。已知洗脱分两步进行第一步:取8~10%的
 溶液
溶液 注入交换柱中。碱性洗脱原理为:
注入交换柱中。碱性洗脱原理为:
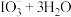 。往碱性洗脱液中滴加
。往碱性洗脱液中滴加 溶液,烧杯底部会析出一层泥状粗碘。
溶液,烧杯底部会析出一层泥状粗碘。第二步:取10%的
 溶液
溶液 注入上述交换柱中。氯化钠洗脱原理为:
注入上述交换柱中。氯化钠洗脱原理为: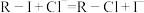 。再往氯化钠洗脱液中滴加
。再往氯化钠洗脱液中滴加 溶液使之酸化,再滴加
溶液使之酸化,再滴加 溶液,溶液由无色转变棕黑色浑浊。
溶液,溶液由无色转变棕黑色浑浊。
①根据交换吸附及洗脱过程可知强碱性阴离子交换树脂也可以对
 进行交换吸附,那实验中将
进行交换吸附,那实验中将 转化成
转化成 的原因可能是
的原因可能是②往氯化钠洗脱液中滴加
 溶液使之酸化,再滴加
溶液使之酸化,再滴加 溶液反应的离子方程式
溶液反应的离子方程式(4)置换碘量法是分析氧化性试剂的一种常用分析方法,基本过程如下:
a.取3只碘量瓶,用移液管分别量取一定体积的供试品(氧化性物质)溶液于碘量瓶(图2)中
b.加入稍过量的碘化钾溶液,盖上盖子,并加纯水液封,静置或微热一段时间
c.打开瓶塞,按图3方式用标准
 溶液进行滴定,重复3次
溶液进行滴定,重复3次d.另取3只碘量瓶,用移液管分别量取一定体积准确浓度的基准液
 溶液于其中
溶液于其中e.计算标准液的浓度
f.空白实验

过程中涉及的反应过程如下:
供试品(氧化性物质)

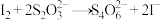

①上述操作合理的顺序是:
 _______
_______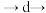 _______
_______ _______
_______ _______
_______ _______
_______ (部分步骤可以重复)
(部分步骤可以重复)②碘量瓶加盖并加纯水液封的主要目的是
③已知
 易受空气和微生物作用而分解,若无上述操作中的d步骤及相关操作,则测定的供试品的含量会
易受空气和微生物作用而分解,若无上述操作中的d步骤及相关操作,则测定的供试品的含量会
您最近一年使用:0次
名校
解题方法
2 . 下列说法不正确的是
| A.提取海带中碘元素时,为保证I-完全被氧化为I2,最好加入过量的氧化剂(H2O2或新制氯水) |
| B.在醋酸总酸含量测定实验中,用标准NaOH溶液滴定醋酸时,最好选用酚酞作指示剂 |
| C.当锌完全溶解后,产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 |
| D.在层析实验操作时,不能让滤纸上的试样点接触展开剂 |
您最近一年使用:0次
19-20高三·浙江·期中
3 . 下列说法不正确的是
| A.用铜丝燃烧法可定性确定有机物中是否存在卤素 |
| B.海水中碘的含量可达8×1010t,目前工业上直接用海水提取碘 |
| C.1828年,德国化学家维勒在制备无机盐氰酸铵时得到了一种结晶物尿素 |
| D.苯酚与水形成的油液静置后会分层,上层是溶有苯的水层,下层是溶有水的苯酚层。当温度高于65℃时,苯酚能与水以任意比例互溶 |
您最近一年使用:0次
名校
4 . 下列说法不正确的是
| A.用铜丝燃烧法可定性确定有机物中是否存在卤素 |
| B.海水中碘的含量可达8×1010t,目前工业上直接用海水提取碘 |
| C.1828年,德国化学家维勒在制备无机盐氰酸铵时得到了一种结晶物尿素 |
| D.苯酚与水形成的油液静置后会分层,上层是溶有苯酚的水层,下层是溶有水的苯酚层。当温度高于65℃时,苯酚能与水以任意比例互溶 |
您最近一年使用:0次
5 . 下列说法不正确的是
| A.海水中碘的含量可达8×1010 t,目前工业上直接用海水提取碘 |
| B.次氯酸能使染料等有机色素褪色,有漂白性 |
| C.石灰石在高温下可用于除去铁矿石中的二氧化硅 |
| D.通过一定的方法来增加铝表面氧化膜的厚度,以加强对铝的保护 |
您最近一年使用:0次
名校
解题方法
6 . 某兴趣小组设计了如下实验测定海带中碘元素的含量,依次经过以下四个步骤,下列图示装置和原理能达到实验目的的是
A.灼烧海带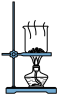 |
B.将海带灰溶解后分离出不溶性杂质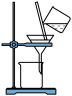 |
C.制备Cl2,并将I-氧化为I2 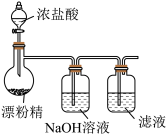 |
D.以淀粉为指示剂,用Na2SO3标准溶液滴定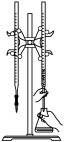 |
您最近一年使用:0次
2020-04-19更新
|
332次组卷
|
5卷引用:浙江省浙北G2(湖州中学、嘉兴一中)2019-2020学年高二下学期期中考试化学试题
7 . 下列说法正确的是
| A.海洋中氯元素含量很大,因此氯元素被称为“海洋元素” |
| B.SO2有漂白性因而可使品红溶液、溴水褪色. |
| C.实验室从海带中提取单质碘的过程:取样→灼烧→溶解→过滤→萃取 |
| D.将植物的秸秆加入沼气发酵池中生成沼气属于生物质能的生物化学转换 |
您最近一年使用:0次
2020-01-05更新
|
169次组卷
|
3卷引用:浙江省9+1高中联盟2020届高三上学期期中考试化学试题
18-19高一·浙江·期末
8 . 海水中有丰富的资源,多种多样的海洋动物、植物、矿藏等。如图是从海水中提取某些物质的示意图。已知:海水中含量最高的几种离子的浓度依次为

请根据以上信息回答下列问题:
(1)写出步骤②的操作名称_______ ;实验室中步骤⑤所需的玻璃仪器除烧杯外,还需要的仪器是___________ 。
(2)D具有杀菌消毒的作用,请写出反应④的离子方程式___________ 。
(3)初步提纯后的粗盐中含有等Ca2+、Mg2+、 等杂质,精制得到精盐的步骤顺序为
等杂质,精制得到精盐的步骤顺序为________ 。(用字母序号填空)
a.加适量盐酸;b.加稍过量的氯化钡溶液,再加稍过量的NaOH溶液;c.过滤;d.蒸发结晶;e.加稍过量碳酸钠溶液
(4)____________ (填“能”或“不能”)用 一种试剂替代步骤②中两种试剂,理由是
一种试剂替代步骤②中两种试剂,理由是________ 。
| 微粒种类 | Cl- | Na+ | Mg2+ |  | Ca2+ |
| 微粒浓度 | 0.55mol·L-1 | 0.47mol·L-1 | 0.054mol·L-1 | 0.027mol·L-1 | 0.01mol·L-1 |

请根据以上信息回答下列问题:
(1)写出步骤②的操作名称
(2)D具有杀菌消毒的作用,请写出反应④的离子方程式
(3)初步提纯后的粗盐中含有等Ca2+、Mg2+、
 等杂质,精制得到精盐的步骤顺序为
等杂质,精制得到精盐的步骤顺序为a.加适量盐酸;b.加稍过量的氯化钡溶液,再加稍过量的NaOH溶液;c.过滤;d.蒸发结晶;e.加稍过量碳酸钠溶液
(4)
 一种试剂替代步骤②中两种试剂,理由是
一种试剂替代步骤②中两种试剂,理由是
您最近一年使用:0次
名校
9 . 某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定
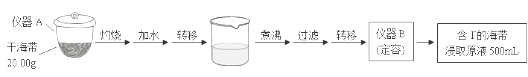
取0.0100 mol·Lˉ1的AgNO3标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
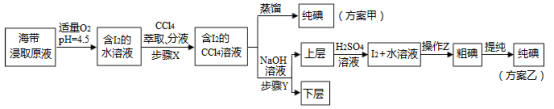
已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
请回答:
(1)①实验(一) 中的仪器名称:仪器A_________ , 仪器 B_________ 。
②该次滴定终点时用去AgNO3溶液的体积为_____ mL,计算得海带中碘的百分含量为_______ %。
(2)①步骤X中,萃取后分液漏斗内观察到的现象是_______________ 。
②下列有关步骤Y的说法,正确的是___________________ 。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
③实验(二) 中操作Z的名称是______________________ 。
(3)方案甲中采用蒸馏不合理,理由是_____________________ 。
实验(一) 碘含量的测定

取0.0100 mol·Lˉ1的AgNO3标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
请回答:
(1)①实验(一) 中的仪器名称:仪器A
②该次滴定终点时用去AgNO3溶液的体积为
(2)①步骤X中,萃取后分液漏斗内观察到的现象是
②下列有关步骤Y的说法,正确的是
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
③实验(二) 中操作Z的名称是
(3)方案甲中采用蒸馏不合理,理由是
您最近一年使用:0次



