名校
解题方法
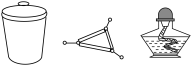
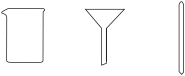
1 . 为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:______ (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤⑤的实验操作名称是______ 。
(3)操作⑤选用苯做萃取剂,苯可以做萃取剂是因为______。
(4)④过程的离子方程式__________________
(5)从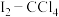 溶液中提取碘可用反萃取法,其流程如下:
溶液中提取碘可用反萃取法,其流程如下:
①操作1中向装有 的
的 溶液加入少量
溶液加入少量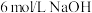 溶液,反应的离子方程式为
溶液,反应的离子方程式为______ ;
②振荡至溶液的______ 色消失,静置、分层,则______ (填“上”、“下”)层为 ;
;
③将含碘的碱溶液从仪器的______ (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴45% 溶液,溶液立即转为棕黄色,并析出碘晶体,若生成
溶液,溶液立即转为棕黄色,并析出碘晶体,若生成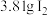 转移
转移______ mol电子。
(6) 溶液浓度越大吸光度越大。用色度计测得溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度为横坐标的标准曲线图,可以得出被测溶液浓度其结果如图所示。海带灼热(灰化)时间超过40min,测得碘的含量逐渐降低,原因是
溶液浓度越大吸光度越大。用色度计测得溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度为横坐标的标准曲线图,可以得出被测溶液浓度其结果如图所示。海带灼热(灰化)时间超过40min,测得碘的含量逐渐降低,原因是____________ 。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤⑤的实验操作名称是
(3)操作⑤选用苯做萃取剂,苯可以做萃取剂是因为______。
| A.苯不溶于水 | B.苯的密度比水小 |
| C.碘在苯中比在水中溶解度更大 | D.苯与碘水不反应 |
(4)④过程的离子方程式
(5)从
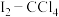 溶液中提取碘可用反萃取法,其流程如下:
溶液中提取碘可用反萃取法,其流程如下: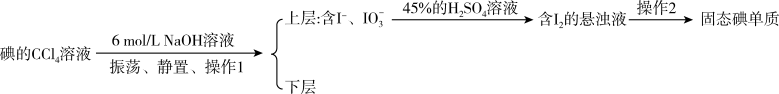
①操作1中向装有
 的
的 溶液加入少量
溶液加入少量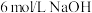 溶液,反应的离子方程式为
溶液,反应的离子方程式为②振荡至溶液的
 ;
;③将含碘的碱溶液从仪器的
④边搅拌边加入几滴45%
 溶液,溶液立即转为棕黄色,并析出碘晶体,若生成
溶液,溶液立即转为棕黄色,并析出碘晶体,若生成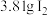 转移
转移(6)
 溶液浓度越大吸光度越大。用色度计测得溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度为横坐标的标准曲线图,可以得出被测溶液浓度其结果如图所示。海带灼热(灰化)时间超过40min,测得碘的含量逐渐降低,原因是
溶液浓度越大吸光度越大。用色度计测得溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度为横坐标的标准曲线图,可以得出被测溶液浓度其结果如图所示。海带灼热(灰化)时间超过40min,测得碘的含量逐渐降低,原因是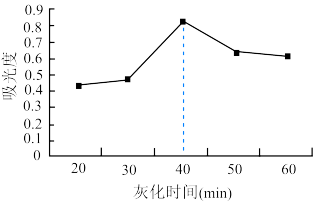
您最近一年使用:0次
名校
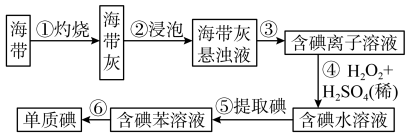
2 . 某同学设计如图实验方案,从海带中提取 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是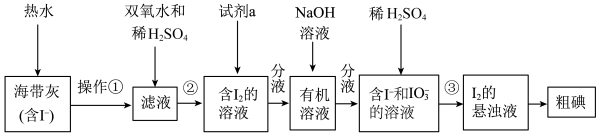
| A.操作①是萃取 |
| B.②中双氧水作还原剂 |
C.③的离子方程式是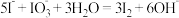 |
D.含 的溶液经3步转化为 的溶液经3步转化为 的悬浊液,其目的是富集,便于分离提纯 的悬浊液,其目的是富集,便于分离提纯 |
您最近一年使用:0次
名校
3 . 从干海带中提取碘的实验流程如下:
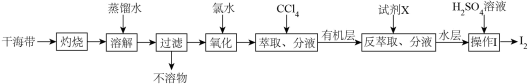
| A.氧化过程可以用过氧化氢代替氯水 |
B.试剂X可以选择使用NaOH溶液,发生的反应为:3I2+6OH‒=5I‒+IO +3H2O +3H2O |
| C.萃取时可使用无水乙醇代替CCl4以节约成本 |
| D.整个过程中的操作是利用了物质的溶解性实现了碘元素的富集、分离与提纯 |
您最近一年使用:0次
名校
4 . 从海带提取碘的实验中,各步选用的实验用品不必都用到的是
选项 | 实验步骤 | 实验用品 |
| A | 步骤1:将海带灼烧灰化 |
|
| B | 步骤2:将海带灰溶解、过滤 |
|
| C | 步骤3:氧化滤液中的I— |
|
| D | 步骤4:检验碘单质 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-30更新
|
116次组卷
|
6卷引用:【全国百强校】北京四中2018-2019学年高一下学期期中测试化学试题
【全国百强校】北京四中2018-2019学年高一下学期期中测试化学试题2015届北京市朝阳区高三4月第一次综合练习理综化学试卷“江淮十校”2018届高三第一次联考化学试题福建省武平县第一中学2021届高三月考化学试题(已下线)第10周 晚练题-备战2022年高考化学周测与晚练(新高考专用)河北省石家庄市2022-2023学年高一下学期期末考试化学试题
名校
5 . 海洋植物如海带,海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:(已知: )。
)。
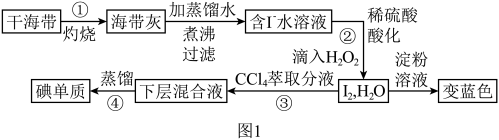
(1)以上步骤不需要用到的仪器是_______。
(2)选用试剂 的理由是_______。
的理由是_______。
(3)写出步骤②中反应的离子方程式_______ 。
(4)工业制备过程中,步骤④很难达到目的,常对图1步骤④进行如下改进:
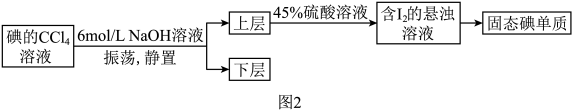
写出上述流程中加入45%硫酸溶液一步反应的离子方程式_______ 。
(5)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
①已知碘元素最终变为无色HIO3。上述整个过程中的还原剂有_______ 。
②若把KI成KBr,则CCl4层变为_______ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
 )。
)。
(1)以上步骤不需要用到的仪器是_______。
A.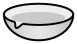 | B. | C. | D. |
 的理由是_______。
的理由是_______。A. 不溶于水 不溶于水 | B. 的密度比水大 的密度比水大 |
C.碘在 中比在水中溶解度更大 中比在水中溶解度更大 | D. 与碘水不反应 与碘水不反应 |
(4)工业制备过程中,步骤④很难达到目的,常对图1步骤④进行如下改进:

写出上述流程中加入45%硫酸溶液一步反应的离子方程式
(5)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
①已知碘元素最终变为无色HIO3。上述整个过程中的还原剂有
②若把KI成KBr,则CCl4层变为
您最近一年使用:0次
名校
解题方法
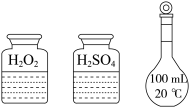
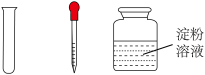
6 . 某同学检验海带中是否含有碘元素,进行了如下实验。
步骤Ⅰ:灼烧干海带得到海带灰;
步骤Ⅱ:将海带灰加蒸馏水溶解、过滤,得到海带灰浸取液;
步骤Ⅲ:取少量浸取液于试管中,加入淀粉溶液,溶液未变蓝;再加入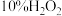 溶液(硫酸酸化),溶液变为蓝色;
溶液(硫酸酸化),溶液变为蓝色;
步骤Ⅳ:将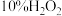 溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
步骤Ⅴ:向步骤Ⅳ所得溶液中通入 ,溶液迅速变为蓝色。
,溶液迅速变为蓝色。
下列说法不正确的是
步骤Ⅰ:灼烧干海带得到海带灰;
步骤Ⅱ:将海带灰加蒸馏水溶解、过滤,得到海带灰浸取液;
步骤Ⅲ:取少量浸取液于试管中,加入淀粉溶液,溶液未变蓝;再加入
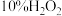 溶液(硫酸酸化),溶液变为蓝色;
溶液(硫酸酸化),溶液变为蓝色;步骤Ⅳ:将
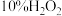 溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;步骤Ⅴ:向步骤Ⅳ所得溶液中通入
 ,溶液迅速变为蓝色。
,溶液迅速变为蓝色。下列说法不正确的是
| A.步骤Ⅰ中,灼烧干海带的目的是除去有机化合物,获得可溶性碘化物 |
B.步骤Ⅲ中,反应的离子方程式: |
C.若将步骤Ⅴ中的 替换为 替换为 溶液,也可能观察到溶液变为蓝色 溶液,也可能观察到溶液变为蓝色 |
D.对比步骤Ⅲ、Ⅳ和Ⅴ中实验现象,说明该条件下 氧化性比氯水强 氧化性比氯水强 |
您最近一年使用:0次
2023-04-29更新
|
553次组卷
|
4卷引用:北京市顺义区第一中学2023-2024学年高三上学期期中考试化学试题
7 . 海洋资源的利用具有非常广阔的前景。
I.利用空气吹出法从海水(弱碱性)中提取溴的流程如图。

已知:溴单质的沸点为58.5℃。
(1)溴元素在元素周期表中的位置是_______ 。
(2)“吸收塔”中发生反应的离子方程式为_______ 。
(3)“蒸馏塔”中温度应控制在_______ (填序号)。
A.40~50℃ B.70~80℃ C.100℃以上
(4)物质A_______ (填化学式)可以循环利用,降低成本。
(5)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的Br-的百分含量如图:

注: 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。
①“氧化”的适宜条件为_______ 。
②已知:海水中溴的浓度是64 mg/L ,经该方法处理后1m3海水最终得到 38.4g Br2,则溴的总提取率为_______ 。
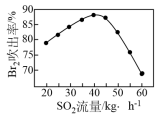
③吸收后的空气进行循环利用。吹出时,Br2 吹出率与吸收塔中SO2流量的关系如图所示。SO2 流量过大,Br2 吹出率反而下降的原因是:___________ 。
Ⅱ.离子交换法从海带中提取碘是一种较为先进的制碘工艺。如图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。

已知:①I2 + I- I
I ;
;
②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I )有很强的交换吸附能力;
)有很强的交换吸附能力;
③步骤“交换吸附”发生的反应:R-Cl+I =R-I3+Cl-。
=R-I3+Cl-。
试回答下列问题:
(6)下列各步反应中,属于氧化还原反应的有:_______(填序号)
(7)酸性条件下,原料被H2O2氧化时发生的反应有:①_______ ;②I2+I- I
I 。
。
(8)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则添加氧化剂与NaI的质量比应不少于_______ 。
I.利用空气吹出法从海水(弱碱性)中提取溴的流程如图。

已知:溴单质的沸点为58.5℃。
(1)溴元素在元素周期表中的位置是
(2)“吸收塔”中发生反应的离子方程式为
(3)“蒸馏塔”中温度应控制在
A.40~50℃ B.70~80℃ C.100℃以上
(4)物质A
(5)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的Br-的百分含量如图:

注:
 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。①“氧化”的适宜条件为
②已知:海水中溴的浓度是64 mg/L ,经该方法处理后1m3海水最终得到 38.4g Br2,则溴的总提取率为
③吸收后的空气进行循环利用。吹出时,Br2 吹出率与吸收塔中SO2流量的关系如图所示。SO2 流量过大,Br2 吹出率反而下降的原因是:

Ⅱ.离子交换法从海带中提取碘是一种较为先进的制碘工艺。如图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。

已知:①I2 + I-
 I
I ;
;②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I
 )有很强的交换吸附能力;
)有很强的交换吸附能力;③步骤“交换吸附”发生的反应:R-Cl+I
 =R-I3+Cl-。
=R-I3+Cl-。试回答下列问题:
(6)下列各步反应中,属于氧化还原反应的有:_______(填序号)
| A.交换吸附 | B.洗脱 | C.酸化氧化 | D.NaCl洗脱 |
 I
I 。
。(8)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则添加氧化剂与NaI的质量比应不少于
您最近一年使用:0次
名校
8 . 从海带中提取 的实验方案如下。下列说法中
的实验方案如下。下列说法中不正确 的是
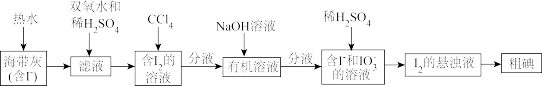
 的实验方案如下。下列说法中
的实验方案如下。下列说法中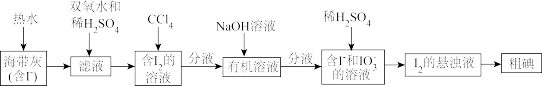
| A.实验方案中2次使用到过滤操作 |
B.向滤液中加入双氧水的作用是将 氧化为 氧化为 |
C. 和 和 在酸性条件下发生反应的离子方程式为 在酸性条件下发生反应的离子方程式为 |
D.含 的溶液经3步转化为 的溶液经3步转化为 的悬浊液,其目的是富集碘元素 的悬浊液,其目的是富集碘元素 |
您最近一年使用:0次
2022-05-24更新
|
341次组卷
|
3卷引用:北京市第十二中学2021-2022学年高一下学期期中考试化学试题
21-22高一下·北京西城·期中
名校
9 . 海洋是一个巨大的化学资源宝库。下列物质中不需要发生化学变化就能够从海水中获得的是
| A.液溴 | B.碘单质 | C.淡水 | D.金属镁 |
您最近一年使用:0次
名校
10 . 下列叙述不正确的是
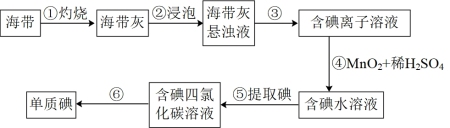

| A.步骤③的分离操作为过滤 |
| B.步骤④中理论上每产生1molI2,需要1molMnO2被氧化 |
| C.步骤⑥操作可以为先加入浓碱过滤,向水层再加入45%硫酸溶液分液,将碘提取出来 |
| D.步骤⑤中加入萃取剂后现象是溶液分层,下层为四氯化碳层呈紫色 |
您最近一年使用:0次
2022-05-15更新
|
195次组卷
|
3卷引用:北京市昌平区第一中学2021-2022学年高一下学期线上期中学情调研化学试题
北京市昌平区第一中学2021-2022学年高一下学期线上期中学情调研化学试题北京市昌平区第一中学2022-2023学年高一上学期期中考试化学试题(已下线)第13练 自然资源的开发利用-2022年【暑假分层作业】高一化学(人教版2019必修第二册)